手术机器人风险分析及质量评价探讨
引言
手术机器人是医疗机器人的典型代表,机器人技术的应用将手术的精度和可行性提升到了全新的高度,引起国内外学术界和产业界的广泛关注。手术机器人本身属于三类高风险的有源医疗器械,作为一种综合性交叉学科的新型医疗器械,其产品质量、会直接影响到产品的使用效果。因此,开展手术机器人的质量评价和风险分析显得尤为重要。
达芬奇机器人作为手术机器人的代表,由于其具有精度高、操作灵活以及消除生理性颤抖等优点,已经广泛应用于临床[1-3]。截至2017 年底,中国大陆地区累计装机69 台,68 台为临床应用,1 台为培训专用,且国内全年完成手术26765 例,平均每台达芬奇手术机器人完成手术393.5 例/年、7.6 例/周,较2016 年增长48.9% [4]。
由于手术机器人使用过程中的复杂性和高风险性,国内外研究机构一直密切关注此类设备临床应用中产生的不良事件[5]。本研究针对不良事件进行分析,为今后手术机器人的产品质控工作提供参考意见。
1 风险分析
Homa 等[6]研究并梳理了2000 至2013 年达芬奇机器人的临床使用不良事件,发现临床使用中造成患者死伤的不良事件起因大致可归为以下几类:手术固有风险、患者自身有基础疾病,机器本身存在技术问题以及手术团队操作问题,机器的技术问题主要包含有软件问题、电缆电源等问题以及手术附件引起的问题等,主要技术问题的分析如下表1 所示。
表1 达芬奇手术机器人主要不良事件起因分析表
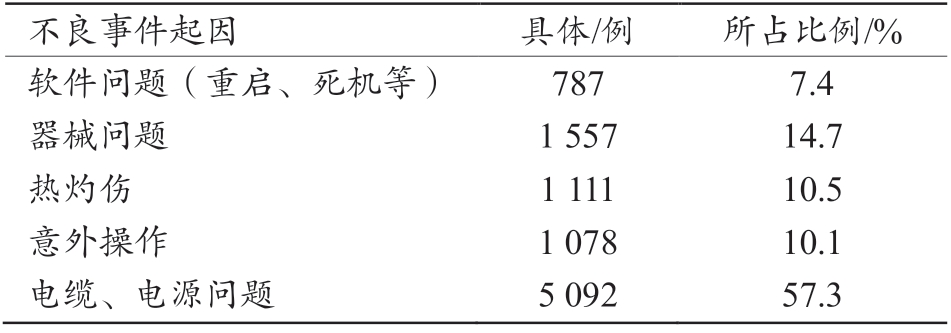
不良事件起因 具体/例 所占比例/%软件问题(重启、死机等) 787 7.4器械问题 1 557 14.7热灼伤 1 111 10.5意外操作 1 078 10.1电缆、电源问题 5 092 57.3
南京总医院等团队研究了2015 年的241 例达芬奇机器人外科手术,术中出现的设备故障主要包括机械臂故障、图像模糊以及操作中无报警等问题[7]。虽然国内外对不良事件的分析较多,但是基于此类风险点大多是给出术前准备、人员培训以及器械洗消方面的建议和改进,关于产品本身的技术问题如何改进并未提及。然而,提高机器人产品本身的有效性和安全性是降低手术机器人术中故障率的根本,对手术的成功具有很大的影响。鉴于此,本文重点结合实际手术机器人检验工作中发现的问题,针对上述风险点考虑质控对策,以期为今后的手术机器人标准化工作提供思路。
2 质量评价
2.1 质量评价问题
手术机器人适用的质控标准主要包括国家标准以及医疗器械行业标准等[8-9]。我国对手术机器人的标准研究尚处于起步阶段,目前通用的标准如表2 所示。此外,针对高频手术器械、内窥镜等设备附件还需要满足GB 9706.4-2009《医用电气设备 第2-2 部分:高频手术设备安全专用要求》、YY 0068.1-2008《医用内窥镜 硬性内窥镜 第1 部分:光学性能及测试方法》等标准。
表2 手术机器人常用标准列表
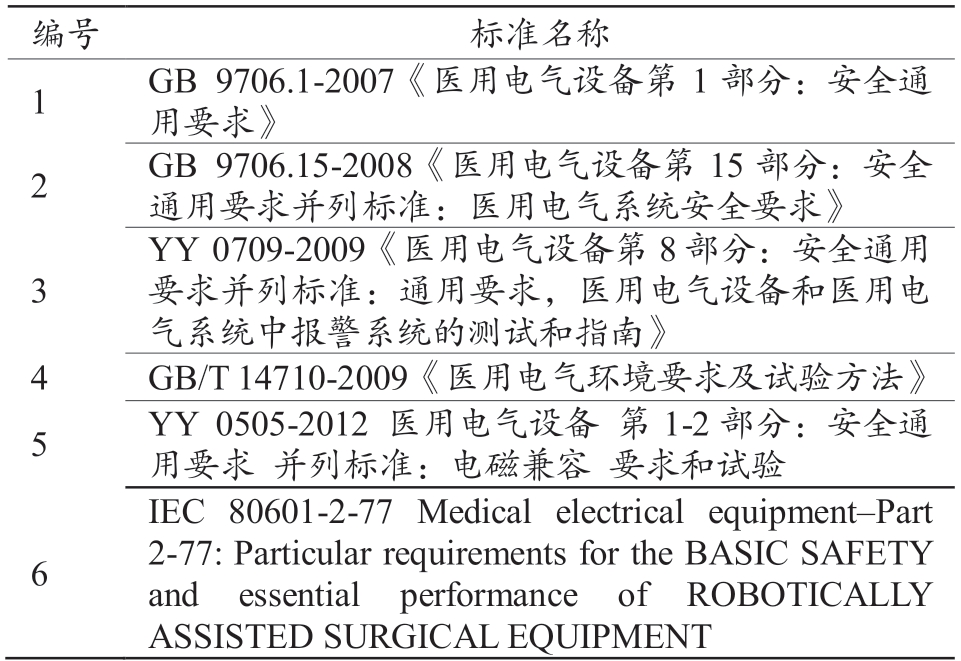
编号 标准名称1 GB 9706.1-2007《医用电气设备第1 部分:安全通用要求》2 GB 9706.15-2008《医用电气设备第15 部分:安全通用要求并列标准:医用电气系统安全要求》3 YY 0709-2009《医用电气设备第8 部分:安全通用要求并列标准:通用要求,医用电气设备和医用电气系统中报警系统的测试和指南》4 GB/T 14710-2009《医用电气环境要求及试验方法》5 YY 0505-2012 医用电气设备 第1-2 部分:安全通用要求 并列标准:电磁兼容 要求和试验6 IEC 80601-2-77 Medical electrical equipment-Part 2-77: Particular requirements for the BASIC SAFETY and essential performance of ROBOTICALLY ASSISTED SURGICAL EQUIPMENT
由于手术机器人具有操作精度高、灵活性强、不受疲劳和情绪影响的特点,大大提升了手术质量,在临床上的应用越来越广泛。我国近几年有多家科研机构关注并投入到手术机器人设备的研究开发中去,在国家项目支撑及市场需求的驱动下,不少机构已经研发出了比较成熟的产品,甚至投入临床[10-13]。考虑到手术机器人是交叉学科的新型产品,与传统的医疗器械相比,其精密度和复杂程度更高,在检验和质量控制方面面临的挑战更大。
日常检验中,我们发现手术机器人往往存在如下安全问题。
2.1.1 保护接地阻抗超限
保护接地是防止人身触电事故、保证医用电气设备正常运行的重要技术措施,对于有保护接地的医用电气设备,为了保证故障电流下保护接地路径的通畅以及过流保护装置的及时触发,保护接地阻抗必须不能超过规定值[14]。
手术机器人由于结构复杂,临床功能多样化,往往不是单一设备而是通过医用电气系统的形式进行工作。医用电气系统是指多台设备的组合,其中至少有一台为医用电气设备,并通过功能连接或使用可移式多孔插座互联。这就涉及系统保护接地的要求,制造商应在设计阶段综合考虑系统装配后的整体安全问题,必要时需要增加附加保护接地,主要形式见图1。
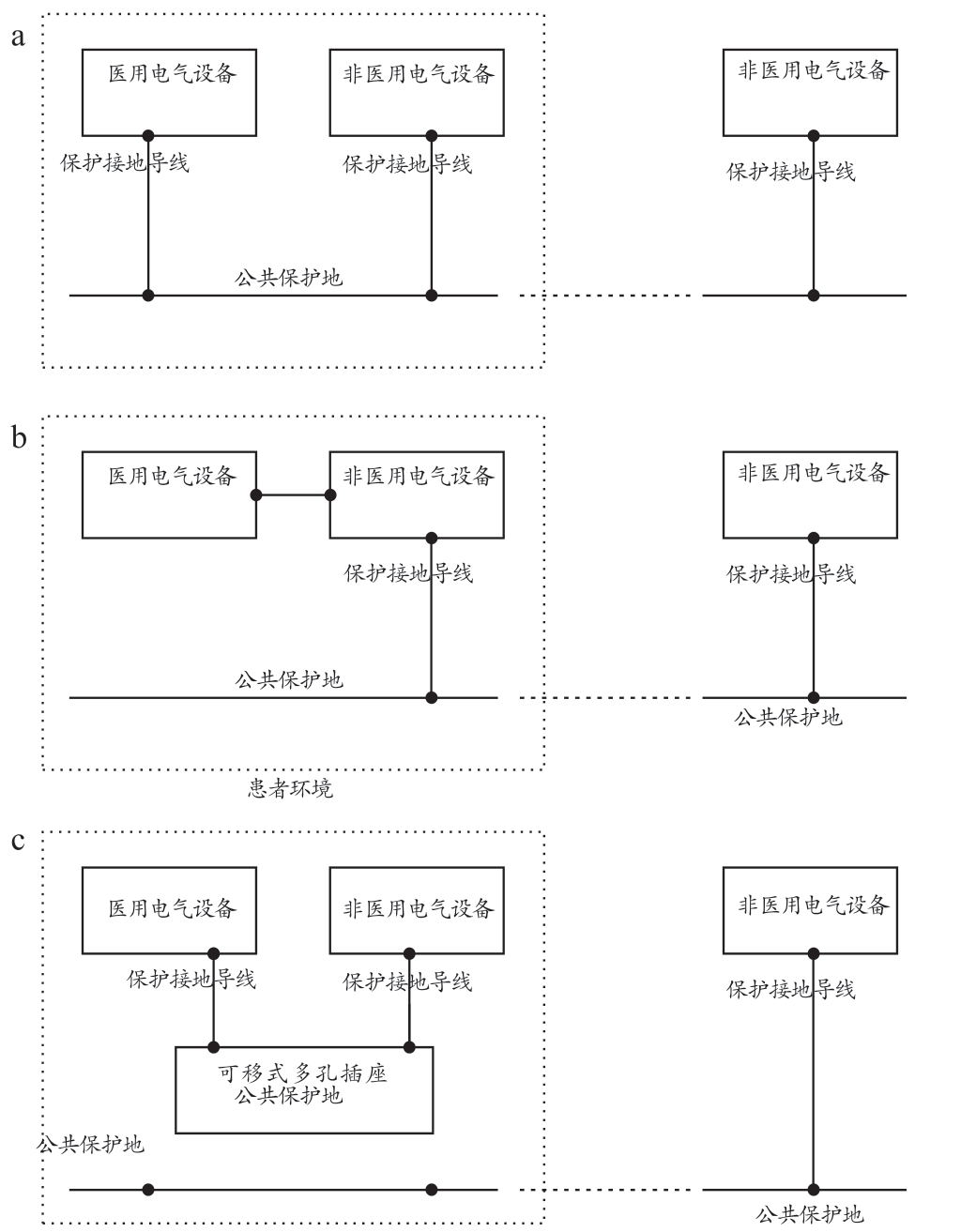
图1 系统保护接地的几种形式
注:a. 患者环境内的保护接地并联形式;b. 患者环境内的保护接地串联形式;c. 通过可移式多孔插座连接到公共电网。
2.1.2 关键元器件选型不合理
手术机器人作为高精尖的医疗器械通常应用于大型手术,对于电源质量的要求比一般设备要严格很多。如果术中电源波动较大或者突发外部电源中断等情况而导致手术机器人停止工作,将会给医生和患者带来不可估量的风险。因此,多数手术机器人采用网电源供电,同时配置不间断电源(Uninterruptible Power Supply,UPS)为设备供电。
UPS 一般由整流器、逆变器、电池和控制电路等组成,能在有限时间里提供纯净、稳定的电源。当网电异常或供电中断时,逆变器改由电池提供能量继续工作,这样逆变器始终处于工作状态,保证无间断地给用电设备供电[15-16]。为了保证电源质量,有的UPS 在内部结构上还包含有隔离变压器,实现对网电的隔离和净化。另外一些手术机器人采用外置隔离变压器的方式来实现同样的目的,具体结构见下图2。
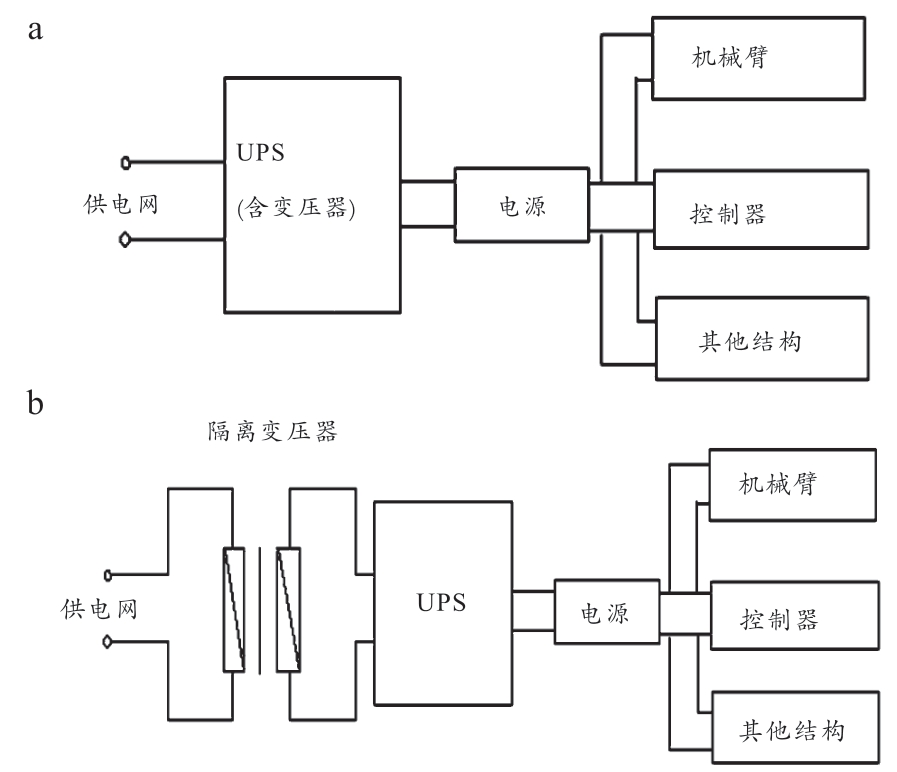
图2 UPS与变压器、电源关系结构图
注:a. 隔离变压器在UPS内;b. 隔离变压器在UPS外。
需要注意的是,隔离变压器如果包含在UPS 内,该隔离变压器作为医用电气设备的一部分,必须要满足医用电气安全标准GB 9706.1-2007 的相关要求;如果单独在UPS外配备隔离变压器,其仅作为医用电气系统的组成部分而非医用电气设备,则仅需要满足相关行业标准即可。
2.1.3 电磁兼容问题
由于机器人属于新兴综合性的医疗器械,制造商在生产和研发环节往往重点关注于产品的性能及功能实现,而对于整体系统的安全性和合规性考虑不足。如前所述,手术机器人结构组成相对复杂,一般包括控制器、显示器、定位装置、机械臂以及手术附件等。各部件之间的连接关系、连接线以及系统中计算机、手术器械的选择都会影响整体系统的安全性能[17-20]。如果不能整体考量,往往设备单独测试均可满足要求,系统连接完成后由于增加线缆或者组件连接器导致出现辐射超限等不合格现象。图2 所示为实际工作中发现的某企业手术机器人在两次辐射发射试验中的测试结果。第一次测试采用关键部件单独测试,第二次测试采用整个系统进行。在系统测试中产品表现出的整体电磁骚扰性能与部件级测试结果差异较大,见图3。
2.2 质量评价的进一步思考
上文分析了日常检验工作在电气安全及电池兼容测试中手术机器人的常见问题,作为手术机器人产品的质量控制还需要加强以下方面。

图3 某手术机器人辐射发射试验结果对比
注:a. 第一次辐射发射测试结果;b. 第二次辐射发射测试结果。
2.2.1 加强手术机器人软件性能评价
本文通过对手术机器人不良事件的分析,发现软件故障造成的不良事件占比较大。相对于传统医疗器械产品而言,我国对于医疗器械软件的管理稍显滞后[21],标准规范尚不成熟。针对手术机器人中的软件组件,目前现行有效的标准、规定有YY/T 0664-2008《医疗器械软件生存周期过程》以及《医疗器械软件注册技术审查指导原则》(以下简称指导原则)等,其中,YY/T 0664-2008 标准主要考虑软件的生命周期及风险等级,指导原则主要关注于软件基本信息、实现过程及核心算法。此外,IEC 80601-2-77标准中明确软件部分适用通用标准中可编程医用电气系统(Portable Emission Measurement System,PEMS)的相关条款。考虑到通用标准中要求对PEMS 整个开发周期过程风险管理和生命周期活动应当被执行,且过程要被记录。对于不能完全执行的情况,也要采取专业的风险管理控制措施。
2.2.2 增加手术机器人可用性方面的评价
手术机器人常常应用于长时间、复杂的大型手术,诸如操作面板和操作手柄的设计、指示灯的颜色选择、急停按钮和手术器械接口的增加等可用性设计都是降低术中风险的重要方面[22]。手术机器人设备在术前需要开展大量的准备工作,术中也往往需要医护人员多人协作共同使用。因此,人因工程方面的设计在保证手术机器人术中表现方面起到了重要的作用。可用性评价方式主要包括形成性可用性和总结性可用性,二者协同合作保证产品的设计生产与预期效果。我们在终产品评价中要特别关注总结性可用性的验证。
3 总结
虽然我国的医疗器械机器人质量评价工作虽然起步比较晚,但是近年来随着医疗器械机器人标准化技术委员会的筹建,相关标准法规都在逐步完善,与国际上的差距正在逐渐缩小。本文总结手术机器人不良事件反馈,结合此类产品临床中容易出现的设备风险点,列举了日常检测中的典型案例加以分析,并给出预防或整改建议。希望为今后该类产品的研发提供思路,也为更好的开展质量评价工作提供参考。
[1] 张和华,魏安海,杨勇.达·芬奇手术机器人应用质量分析与风险控制[J].中国医学装备,2018,15(10):110-112.
[2] 申培培,张琼,吕雪青,等.达·芬奇手术机器人术中故障发生原因及改进措施[J].护理学杂志,2017,32(12):50-51.
[3] 李军,房爱玲.达芬奇智能手术机器人的概况及临床应用[J].中国医疗器械信息,2019,25(16):32-33.
[4] Swerdlow DR,Cleary K,Wilson E,et al.Robotic arm-assisted sonography:review of technical developments and potential clinical applications[J].AJR Am J Roentgenol,2017,208(4):733-738.
[5] 赵飞,高明献,刘璞,等.136例国际医疗器械严重不良事件的统计与分析[J].中国医疗器械杂志,2020,44(2):166-171.
[6] Homa A,Jaishankar R,Nancy L,et al.Adverse events in robotic surgery: a retrospective study of 14 years of FDA data[J].PloS One,2016,11(4):e0151470.
[7] 申培培,张琼,吕雪青,等.达芬奇手术机器人术中故障发生原因及改进措施[J].护理学杂志,2017,32(12):50-51.
[8] 司玮,华文,卞蓉蓉,等.国内手术机器人的标准研究及风险控制要点[J].中国标准化,2019,(4):219-220.
[9] 茅龚丹.手术机器人技术标准的现状与发展[J].上海电气技术,2019,12(4):60-63.
[10] 梁晓雄,余国瑞,黄莉.手术机器人的检测方法[J].上海计量测试,2019,46(3):50-51.
[11] 陈英耀,厉传琳,葛智馨,等.手术机器人技术的安全性和有效性评估[J].中国卫生质量管理,2010,17(6):43-46.
[12] 王恩运,吴学谦,薛莉,等.外科手术机器人的国内外发展概况及应用[J].中国医疗设备,2018,33(8):115-119.
[13] 李治非,杨阳,苏月,等.我国外科手术机器人研究应用现状与思考[J].中国医学装备,2019,16(11):177-181.
[14] 刘继广,王伟,邓振进,等.医用电气设备可触及金属部件保护接地要求分析[J].医疗卫生装备,2017,38(2):95-97.
[15] 王燕妮,李传伟.UPS供电系统在医疗设备上的应用[J].中国医疗器械信息,2010,16(4):25-29.
[16] 于树新.医疗设备不间断电源的监控管理[J].电源技术,2018,42(3):442-444.
[17] 王权,李澍,张超,等.医用机器人电磁兼容检测研究[J].中国医疗设备,2019,34(9):30-34.
[18] 李佳戈,张艳丽,苏宗文.医疗器械电磁兼容标准关键细节解析[J].中国医疗设备,2014,(8):70-72.
[19] 张超,苏宗文,李澍,等.电磁兼容抗扰度试验布置验证的研究[J].中国医疗设备,2019,34(9):20-23.
[20] 王权,李澍,苏宗文,等.电源在医用电气设备电磁兼容性测试中的影响分析[J].中国医疗设备,2015,30(8):127-129.
[21] 王晨希,任海萍.医疗器械软件概述[J].中国药事,2012,26(11):1210-1213.
[22] 司玮,华文,卞蓉蓉,等.国内手术机器人的标准研究及风险控制要点[J].中国标准化,2019,(4):219-220.
Discussion on Risk Analysis and Quality Evaluation of Surgical Robot