两种放疗技术治疗难治性瘢痕疙瘩的剂量学比较
引言
放射治疗是治疗瘢痕疙瘩的公认选择。1909年,Sequeira首次对其进行了描述[1]。根据国际瘢痕管理咨询小组的报告,目前被认为是最有效的治疗方式[2]。据报道,治疗有效率一般在67%~98%之间[3]。手术切除瘢痕后,成纤维细胞增生活跃,术后放射治疗通过诱导成纤维细胞凋亡以及破坏内皮细胞来防止复发。
瘢痕术后所采用的放疗技术分为外照射(External Beam Radiotherapy,EBRT)和近距离放射治疗。外照射需要直线加速器,首选的射线种类是电子线。与外照射相比,近距离治疗是将放射源通过施源器直接置于真皮内或皮肤的外表面,根据施治技术不同,可分为组织间插植和表面敷贴两种方式;根据放射源剂量率不同,又可以进一步分为低剂量率(Low Dose Rate,LDR)和高剂量率(High Dose Rate,HDR)两种方式。LDR 近距离放射治疗因使用低剂量率放射源,治疗周期较长,已被HDR近距离放射治疗所取代。
根据我科既往数据显示,部分难治性瘢痕,如部分面颈、胸背部及较长的瘢痕,电子线外照射后控制率仅在70%~80%[4]。本研究主要目的是比较电子线外照射和铱192(192Ir)HDR 表面敷贴近距离治疗(192Ir HDR Superficial Brachytherapy, 192Ir HDR-SB)的剂量分布,以找到可以进一步提高部分难治性瘢痕控制率的更优的治疗技术。
1 材料及方法
1.1 材料
在CIRS公司的头颈部仿真模体和CIRS公司的固体水模体(30 cm×30 cm×10 cm)上,模拟下颌及胸背部常见瘢痕切口位置,使用飞利浦大孔径CT模拟定位机行CT扫描(层厚3 mm),得到如下4套CT图像:① 在头颈仿真模体右侧下颌区,铅丝标注常见瘢痕切口位置,进行CT扫描(图1a);② 在图1a基础上沿铅丝走形表面敷贴医科达公司的 flap管状施源器,再进行CT扫描(图1b);③固体水模体模拟胸背部等处瘢痕切口(较平坦),进行CT平扫;④ 在上述固体水模体上表面敷贴 flap管状施源器再进行CT扫描(图1c)。

图1 CT模体扫描示意图
注:a. 在头颈部仿真模体上标注铅丝模拟下颌瘢痕切口;b. 在图1a基础上铅丝位置敷贴flap管状施源器;c. 在固体水模拟上敷贴 flap管状施源器。
1.2 方法
将上述4套CT图像分别导入瓦里安公司Eclipse V13.6治疗计划系统,皮肤表面加0.5 cm组织等效物,使用瓦里安TrueBeam直线加速器的6 MeV电子线模拟源皮距照射,进行计划设计,照射野为模拟瘢痕切口周围均匀外放1 cm,固体水使用3 cm宽照射野,18 Gy/2f(1 f/w)。192Ir HDR-SB时,采用医科达近距离治疗机,将商用flap管状施源器敷贴于照射区域表面,其管道平行于瘢痕切口方向,固有的管道至皮肤表面距离0.5 cm,使用医科达Oncentra近距离治疗计划系统模拟计划设计,以皮下0.5 cm作为剂量参考点,参考点剂量18 Gy/2f(1 f/w)。分别使用电子线和近距离治疗模拟以下三种部位的瘢痕切口剂量分布:① 平整表面,长度小于25 cm的瘢痕切口;② 平整表面,长度大于25 cm的瘢痕切口;③下颌等凹凸不平表面的瘢痕切口。平整表面,长度大于25 cm的瘢痕切口:在电子线外照射时,单独一野很难进行照射,大部分情况下需要分野后进行照射,为了避免皮肤表面瘢痕切口低剂量,临床治疗中多采用两野无缝衔接照射技术。故本研究模拟一30 cm长切口,分两部分(22 cm、8 cm)照射,在25 cm×25 cm限光筒和10 cm×10 cm限光筒上放置23 cm×3 cm和9 cm×3 cm挡铅(切口两端各放1 cm,衔接处不外放),两野无缝衔接,模拟测量两野衔接处的剂量分布。
2 结果
2.1 在平整表面、不需要分野照射的瘢痕切口(长度25 cm以内)
(1)6 MeV电子线照射:考虑到0.5 cm组织等效物,85%等剂量曲线的照射深度达皮下1.3 cm,皮肤表面剂量为处方剂量的92%左右(图2)。
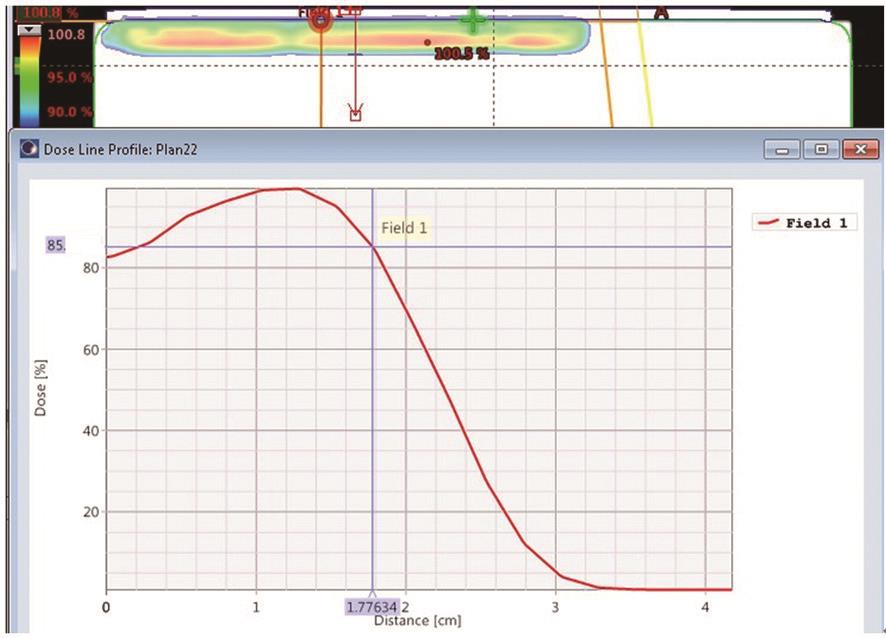
图2 长度<25 cm瘢痕切口电子线照射剂量分布
(2)192Ir HDR-SB照射:皮下0.5 cm为处方剂量,在皮下0.5 cm处方剂量照射宽度为1.2 cm左右;在皮肤表面处方剂量照射宽度为2 cm左右,皮肤表面剂量接近处方剂量180%(图3)。
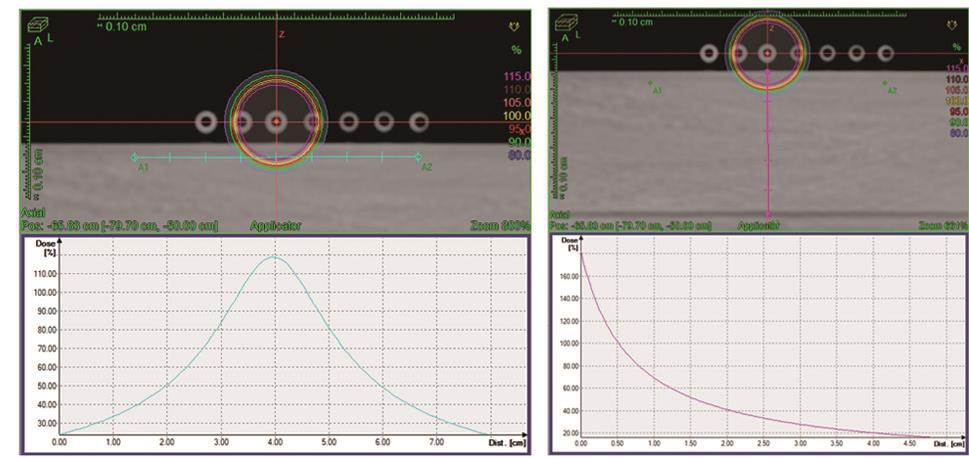
图3 长度<25 cm瘢痕切口192Ir HDR-SB剂量分布
2.2 平整表面,长度大于25 cm的瘢痕切口
(1)6 MeV 电子线照射:需分野照射,两野无缝衔接处在皮下1 cm处有大于120%的高剂量区(图4)。
(2)192Ir HDR-SB 照射:可以根据瘢痕切口长度调整施源器管道长度,故不存在射野衔接问题,在参考点层面,剂量仍较为一致(图5)。
2.3 下颌等凹凸不平的表面瘢痕切口
(1)6 MeV 电子线照射:射野中心处85%等剂量深度仍在1.8 cm(含0.5 cm组织等效物),见图6。但是随着表面曲度变化,上下各层面照射深度变化明显(随着源皮距增加,照射深度变浅),沿切口方向,射野中心±1.2 cm处,85%剂量深度分别为1.91 cm和1.65 cm(图7)。
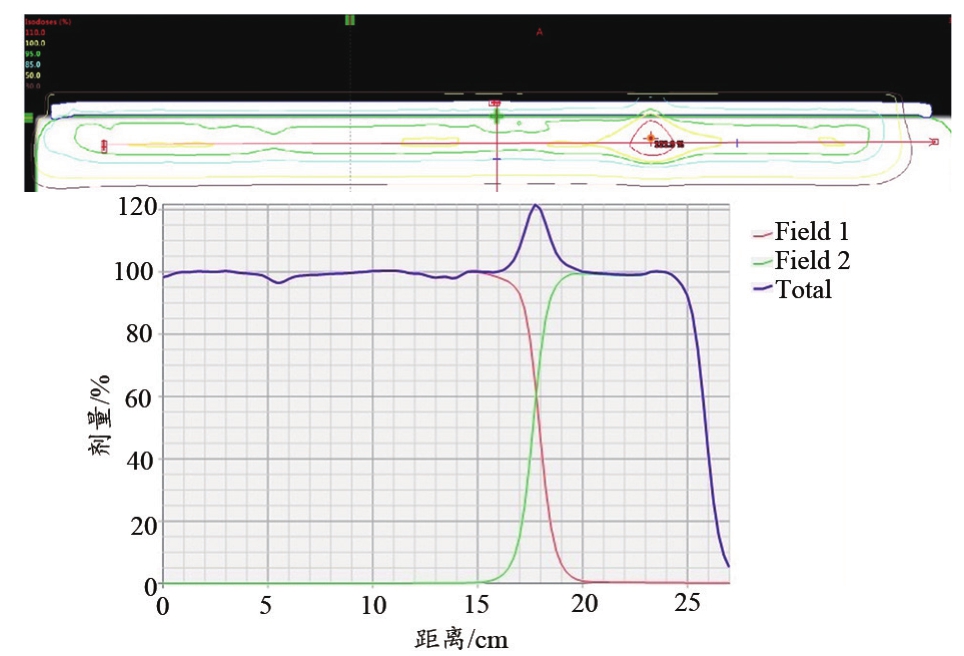
图4 两个电子线照射野无缝衔接区域的剂量分布

图5 192Ir HDR-SB治疗较长瘢痕切口的剂量分布
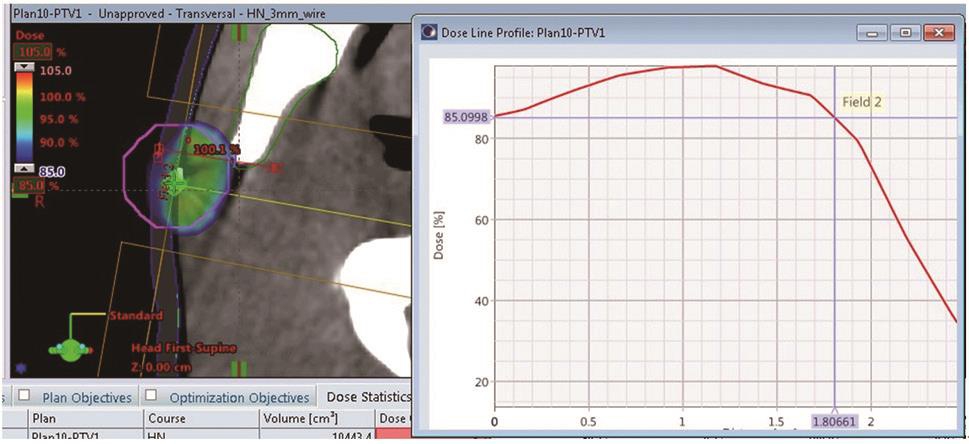
图6 下颌区瘢痕切口射野中心层面电子线剂量分布

图7 下颌区瘢痕切口各层面电子线剂量分布(显示85%等剂量曲线照射范围)
(2)192Ir HDR-SB 照射:施源器敷贴于瘢痕切口,随切口曲度变化,在参考点层面,剂量依旧较为一致(图8)。
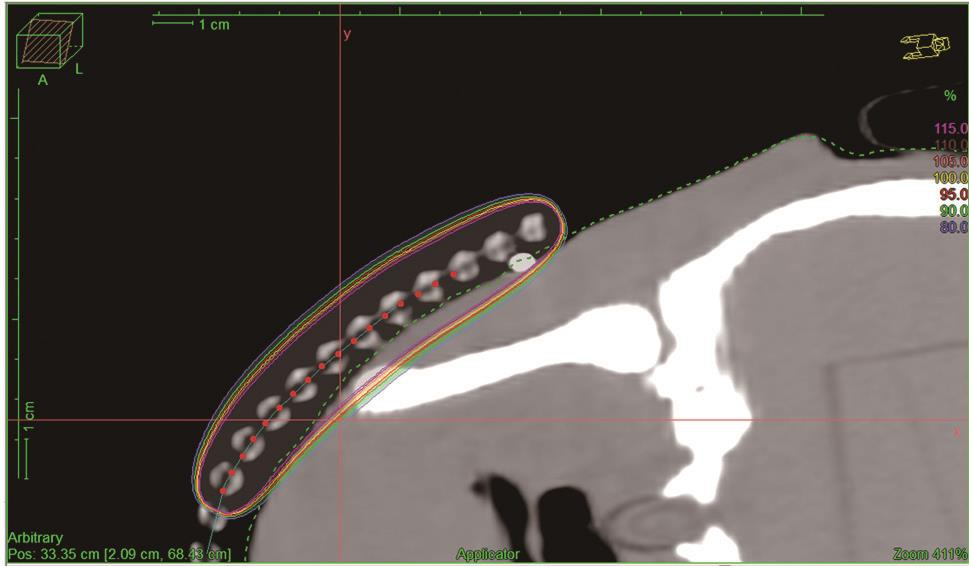
图8 下颌区瘢痕切口192Ir HDR-SB剂量分布
3 讨论
目前术后放疗已被认为是防止瘢痕疙瘩再形成的最有效的治疗方法。本研究比较了电子线外照射和192Ir HDRSB的剂量分布,为临床不同情况下采用何种技术提供了明确的剂量解析。
外照射通常采用源皮距照射技术,照射切口两侧外放1 cm左右大小的区域,相对于其他射线种类而言,电子线对于瘢痕术后治疗更加合适,目前作为外照射治疗的首选。但是,从上述剂量分布结果可以看出,因为其能量及照射方式所致,照射深度较深,周围正常组织不可避免受照,包括腺体或骨组织,从而带来相应的不良反应。另外,对于较长的瘢痕切口及不平整皮肤表面的切口,采用电子线外照射时皮下同一照射深度剂量分布不一致,可能导致瘢痕控制率下降或美容效果不佳。
近距离治疗,1967年由Nicolettis等[5]首次在国际文献中介绍。在部分文献的因素分析显示在近距离治疗后,瘢痕控制较高,瘢痕疙瘩长度与复发已没有相关性。甚至部分学者认为,近距离治疗是瘢痕治疗的最佳放疗技术之一,作为首选[6-7]。
瘢痕术后HDR近距离治疗分为组织间插植和表面敷贴两种方式。组织间插植照射是手术时将空心针管植入闭合切口皮下,再导入步进源进行照射。其特点是治疗时间较短,适用于门诊治疗。但因为是有创操作,治疗尽可能集中在短期内完成;另外,创口护理要求较高,文献报道伤口感染、红肿、裂开等为主要的并发症;部分病例在治疗过程中出现导管脱落的情况,直接影响治疗疗效。表面敷贴治疗可以在一定程度上减少这些情况的发生率[8]。
表面敷贴治疗已经应用多年,在镭治疗年代就用于皮肤癌的治疗,并发展了著名的Quimby和Paterson-Parker系统,对镭模步源制定了严格的规范。至今,使用程控步进源,并有先进的计划系统,可根据巴黎剂量学原则按单平面插植条件步源,为降低靶区剂量变化梯度,需要避免直接将塑管敷贴在皮肤表面,可用组织等效材料隔开。另外,很少用于深层(≥1 cm)的肿瘤的放疗。我科进行的表面敷贴近距离治疗,采用192Ir源,商用Flap管状施源器,治疗时将施源器紧密附着在皮肤表面,胶带固定。这种操作模式,有利于将治疗间隔拉开,避免导管脱落及伤口感染、裂开等并发症风险,并且可以在伤口轮廓和长度上灵活调整。此外,由于使用了远程后装操作系统,医护人员的暴露降至最小化。
从我们的测量数据来看,192Ir表面敷贴近距离治疗,在剂量学上优势明显:① 更集中照射需要照射的区域;② 减少对周围健康皮肤的辐射;③ 较长切口,外照射需要分野照射的病例中,采用近距离治疗避免分野处剂量衔接不佳等问题;④ 凹凸不平的表面,随着表面曲度变化,电子线外照射时,上下各层面高剂量区照射深度变化明显(随着源皮距增加,照射深度变浅),但表现仍能保持参考点平面的剂量分布一致。
另外,表面敷贴近距离治疗的放射源选择上,除了192Ir源外,文献报道应用最多的同位素是锶90。192Ir半衰期73.8 d,释放γ射线,能谱在0.29~0.48 Mev之间,防护半值厚度3 mmPb;锶90半衰期28.1 d,释放β射线,最大能量 1 Mev,防护半值厚度 0.14 mmPb。Wagner等 [9]报道同位素锶90~钇90表面敷贴近距离治疗瘢痕疙瘩的有效率达80%,但β射线穿透力弱,入射深度小,80%的等剂量曲线仅达到皮下2 mm,2 mm后剂量仅剩余20%,5 mm后仅剩余1%~3%。因为照射深度有限,在既往文献报道中,其复发率(20%~36%)大部分高于192Ir源(9.7%~12.5%),且皮肤副反应明显升高[9-12]。
综上所述,从剂量分布角度,建议如下:① 针对平坦皮肤表面,采用兆伏级电子线及192Ir HDR-SB剂量分布均较好,但兆伏级电子线照射深度更深,周围正常组织受量更多;② 针对表面不平及较长、外照射需要分野照射的部位,192Ir HDR-SB剂量学优势明显。Kuribayashi等[12]关于192Ir HDR-SB治疗术后瘢痕的回顾性分析的文献结果显示局部控制率较高(90.3%),且副反应可接受(没有发生2级及以上毒性反应)。但是,与兆伏级电子线比较的临床文献相对较少,仅有国内1篇,从控制率看,兆伏级电子线及192Ir HDR-SB在瘢痕术后控制率相当,但192Ir HDR-SB治疗的头颈部瘢痕切除术后组,复发率明显低于兆伏级电子线组,优势明显;且治疗相关皮肤等副反应无差异[13]。除放疗技术外,瘢痕治疗的疗效还与BED、手术与放疗时间间隔等因素相关[4]。
在本研究中,我们采用的剂量分割模式来自我们外照射经验。多年来,不同的放射方式和剂量被用于瘢痕疙瘩治疗。对所有模式的综合评估表明,至少需要30 Gy的生物等效剂量(BED,α/β=10)才能达到<10%的复发率[14]。针对张力较高的部位,如胸背部,照射剂量可以略高(BED30-35Gy);张力较低的部位,如耳部,照射剂量可以略低(BED15-22.5Gy)[15-17]。手术到放疗时间间隔间隔建议缩短至 24~48 h 以内 [16,18-19]。
由于近距离放射治疗和EBRT技术不同,治疗方案不能直接外推,BED也可能不同。多中心回顾性分析结果显示:HDR近距离治疗BED20 Gy左右可以达到较好的局部控制率[6],但这些剂量分割模式主要来自组织间插植近距离治疗,表面敷贴近距离治疗尚无相关文献报道。
4 结论
192Ir HDR-SB与兆伏级电子线比较,剂量学优势明显,尤其是针对较长及表面不平的难治性瘢痕,剂量优势尤为明显。需要注意的是治疗时需将施源器紧密敷贴在切口表面。剂量学上的比较,可以让我们了解不同技术间的细微差别,给患者提供更多的治疗选择和更优的治疗方案。其进一步的美容效果、剂量分割模式等问题需在后期临床实践中得出。
[1] Sequeira JH.Case illustrating the effects of X-rays on scarkeloid[J].Proc R Soc Med,1909,(2):96-98.
[2] Mustoe TA,Cooter RD,Gold MH,et al.International advisory panel on scar management. International clinical recommendations on scar management[J].Plast Reconstr Surg,2002,(297):433-438.
[3] Ogawa R,Yoshitatsu S,Yoshida K,et al.Is radiation therapy for keloids acceptable? The risk of radiation-induced carcinogenesis[J].Plast Reconstr Surg,2009,(124):1196-1201.
[4] Shen J,Lian X,Sun Y,et al.Hypofractionated electron-beam radiation therapy for keloids:retrospective study of 568 cases with 834 lesions[J].J Radiat Res,2015,56(5):811-817.
[5] Nicolettis C,Cassagne D.L’irridiation interstitielle par l’iridium 192 dans la prevention des recidives après excision chirurgicalle des cicatrices cheloidiennes[J].Ann Chir Plast,1967,(12): 237-242.
[6] Bijlard E,Verduijn GM,Harmeling JX,et al.Optimal high-doserate brachytherapy fractionation scheme after keloid excision:A retrospective multicenter comparison of recurrence rates and complications[J].Int J Radiat Oncol Biol Phys,2018,100(3):679-686.
[7] Goutos I,Ogawa R.Brachytherapy in the adjuvant management of keloid scars: literature review[J].Scars Burn Heal,2017,(3):2059513117735483.
[8] Guix B,Henríquez I,Andrés A,et al.Treatment of keloids by high-dose-rate brachytherapy: a seven-year study[J].Int J Radiat Oncol Biol Phys,2001,50(1):167-72.
[9] Wagner W,Alfrink M,Micke O,et al.Results of prophylactic irradiation in patients with resected keloids[J].Acta Oncol,2000,(39):217-220.
[10] Fraunholz IB,Gerstenhauer A,Boettcher HD.Results of postoperative 90Sr radiotherapy of keloids in view of patients subjective assessment[J].Strahlenther Onkol,2005,(181):724-729.
[11] Narkwong L,Thirakhupt P.Postoperative radiation with high dose rate Iridium 192 mould for prevention of earlobe keloids[J].J Med Assoc Thai,2006,(89):428-433.
[12] Kuribayashi S,Miyashita T,Ozawa Y,et al.Post-keloidectomy irradiation using high-dose-rate superficial brachytherapy[J].J Radiat Res,2011,(52):365-368.
[13] 钟亚华,周云峰,谢丛华,等.千伏X线、电子线和192铱放射治疗疤痕疙瘩疗效比较[J].武汉大学学报(医学版),2007,(6):820-822.
[14] Kal HB,Veen RE,Jurgenliemk-Schulz IM.Dose-effect relationships for recurrence of keloid and pterygium after surgery and radiotherapy[J].Int J Radiat Oncol Biol Phys,2009,74(1):245-251
[15] Ogawa R,Huang C,Akaishi S,et al.Analysis of surgical treatments for earlobe keloids: analysis of 174 lesions in 145 patients[J].Plast Reconstr Surg,2013,132(5):818e-825e.
[16] Flickinger JC.A radiobiological analysis of multicenter data for postoperative keloid radiotherapy[J].Int J Radiat Oncol Biol Phys,2011,79(4):1164-1170.
[17] 王庆国,李晓梅,张敏,等.107例瘢痕疙瘩术后两种分割剂量放疗疗效分析[J].北京大学学报(医学版),2014,46(1):169-172.
[18] Van Leeuwen MC,Stokmans SC,Bulstra AE,et al.Surgical excision with adjuvant irradiation for treatment of keloid scars: a systematic review[J].Plast Reconstr Surg Glob Open,2015,3(7):e440.
[19] Duan Q,Liu J,Luo Z,et al.Postoperative brachytherapy and electron beam irradiation for keloids: a single institution retrospective analysis[J].Mol Clin Oncol,2015,3(3):550-554.
Dosimetric Comparison of Two Kinds of Radiotherapy Techniques for Intractable Keloids