新型腹壁疝修补用复合补片的制备及其性能研究
引言
疝气是一种外科常见病和多发病[1-2],包括腹壁疝、股疝、盆壁疝、膈疝、会阴和盆底疝等,其中在临床上以腹壁疝最为常见。目前,临床上常用的治疗手段是无张力修补术,通过植入补片达到补强缺损组织的效果[3]。近年来,聚丙烯等人工合成补片得到广泛应用,存在的缺点是容易产生过量的瘢痕组织,与腹腔脏器直接接触时可能引起腹腔粘连、纤维化等,引起患者不适和慢性炎症[4-6]。
近年来,寻求一种生物相容性好的复合补片成为研究的热点[7]。目前,国内产品多为单一的生物补片或聚丙烯补片,复合补片较为少见。国外的复合补片主要有Sepramesh®、Proceed®、Parietex® 等 [8],这些产品是以聚丙烯网为基体,用可吸收材料进行编织复合,减少了聚丙烯的比例,材料更轻,部分可吸收,以确保相对小的永久性植入物,提高了腹壁顺应性。但因缺乏仿生结构,与机体存在不适配等难题,仍存在过量瘢痕增生、粘连的发生和术后慢性疼痛等[9-10]。
针对目前补片存在的缺陷,结合人体腹壁局部解剖结构,本研究设计了一种新型复合补片。该补片以轻质聚丙烯网为支撑层,模拟腹横筋膜提供力学强度;在支撑层内面构筑由纳米纤维丝制成的三维多孔膜结构,模拟腹膜壁层作为补片的防粘连层;以透明质酸等亲水性天然材料修饰支撑层外面,模拟细胞外基质成分作为补片的诱导层,诱导机体细胞长入及增殖。本文讨论了厚度设计、纺丝液质量分数、透明质酸分子量对复合补片的影响。
1 材料及方法
1.1 实验材料及设备
(1)实验材料。聚乳酸,重均分子量为15万,实验室自制;透明质酸,医用级,华熙福瑞达生物医药有限公司;聚丙烯网补片,日照天一生物医疗科技有限公司;六氟异丙醇,分析纯,济南朗化化工有限公司;无水乙醇;纯化水。
(2)实验设备。北京富友马科技有限公司的静电纺丝机(型号1206),美国CIF公司的CPC-B等离子体处理仪,上海轩准仪器有限公司的XG-CAMC31型接触角仪,德国Zeiss公司的SUPRA55扫描电子显微镜,日本岛津AGS-H电子万能试验机。
1.2 复合补片的制备
用无水乙醇超声清洗聚丙烯网,37℃恒温烘箱中干燥24 h备用。将一定质量的聚乳酸溶于六氟异丙醇中,搅拌溶解得到聚乳酸溶液。以适当电压将聚乳酸溶液纺成纳米纤维丝,收集于静电纺丝机接收板上的聚丙烯网内表面。将得到的聚丙烯网与聚乳酸复合纤维膜固定于等离子体处理仪基板上,设定一定射频功率对纤维膜进行表面处理。处理一定时间后,将透明质酸水溶液均匀涂覆于聚丙烯网外表面,常温下干燥24 h后,40℃真空烘箱干燥过夜,得到复合补片。
1.3 复合补片的表征
1.3.1 形貌观察
复合补片真空镀金后,采用扫描电子显微镜观察复合补片的内表面及横截面形貌[11];利用其自带软件,随机选取视野内20根纤维丝进行测量,纤维直径取平均值。
1.3.2 拉伸强度
将复合补片裁剪为4 cm长样条,采用电子万能试验机测试其拉伸强度[12];将样品两端夹紧,以5 mm/min的速度加载试验机直至样条断裂;记录拉伸强度及伸长率。
1.3.3 亲水性能
采用水滴静态接触角来表征亲水性能[13],使用接触角测量仪测试复合补片外表面的静态接触角,加液量为3.5 μL,每个样品测试5个点,取5次的平均值。
2 结果与讨论
2.1 复合补片诱导层、防粘连层的厚度设计
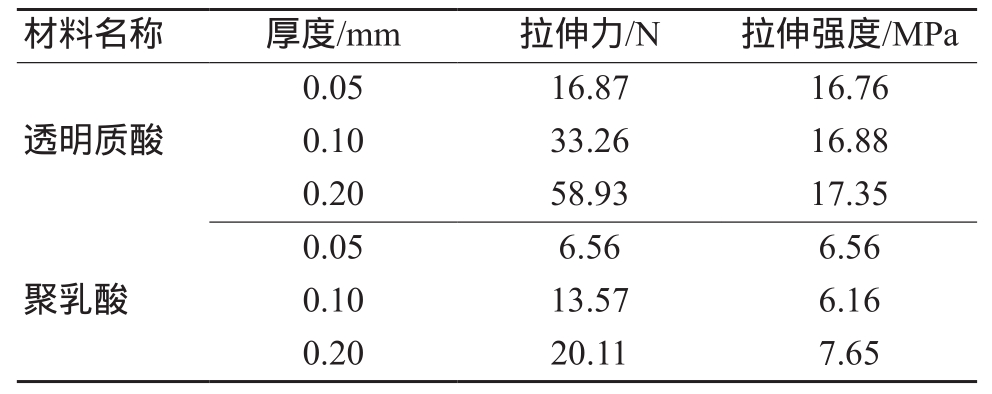
针对目前补片存在的缺陷,结合人体腹壁局部解剖结构,通过计算机软件设计了一种新型复合补片。该新型复合补片的结构设计图,见图1。多层复合存在层间力学匹配问题,当层间力学性能差异较大时,在受力条件下,各层之间容易滑移、脱落。但因每一层所选材料性质的差异,只能寻求最大匹配度来满足多层复合的力学要求。随着材料厚度的增加,试验样条所能承受的拉伸力越大(表1)。市售聚丙烯补片的厚度普遍在0.5 mm左右,且随着补片厚度的增加,植入人体后的异物感越强烈。因此,复合补片在保证补强效果的前提下,厚度应尽量减小。综上所述,诱导层和防粘连层的厚度均设计为0.05~0.10 mm之间。
2.2 纺丝液质量分数对防粘连层的影响
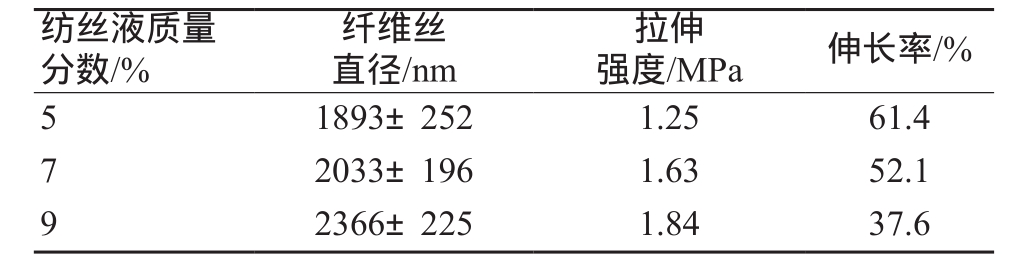
纺丝液质量分数对静电纺丝过程和最终所得纤维丝的形态有较大影响。由表2可知,当纺丝液质量分数由5%提高到7%时,纤维丝直径逐渐增大至2366 nm,防粘连层纤维膜的拉伸强度也呈增大趋势。由图2可见,当纺丝液质量分数为5%时,可以得到聚合物纤维,实现连续纺丝,但纤维丝中出现较多珠状物。随纺丝液质量分数提高,获得平滑纤维。由此可得,纺丝液质量分数影响防粘连层纤维丝的形貌、直径,进而影响到纤维膜的力学性能。

图1 新型复合补片的结构设计图(a)及截面SEM图(b)
表1 不同厚度样条的拉伸性能比较
材料名称 厚度/mm 拉伸力/N 拉伸强度/MPa透明质酸0.05 16.87 16.76 0.10 33.26 16.88 0.20 58.93 17.35 0.05 6.56 6.56 0.10 13.57 6.16 0.20 20.11 7.65聚乳酸
表2 当纺丝电压一定时,纺丝液质量分数对纤维膜性能的影响
纺丝液质量分数/%纤维丝直径/nm拉伸强度/MPa 伸长率/%5 1893±252 1.25 61.4 7 2033±196 1.63 52.1 9 2366±225 1.84 37.6

图2 不同纺丝液质量分数所得纤维膜的SEM照片
注:a. 5%;b. 7%;c. 9%。
出现这种现象的原因可能是,聚乳酸分子链间要有足够的缠绕才能实现静电纺丝过程,当聚乳酸分子链间的缠绕度较低时,获得珠状纤维而非平滑纤维。当纺丝液质量分数增加至7%时,纺丝液获得足够的分子间缠绕,所得纤维具有较好的形貌。随着质量分数的提高,所得纤维的直径逐渐增加,这是因为随质量分数增大,在电荷量不变的条件下较大质量的电荷载体通过喷头到达接收装置,而令电荷载体分散的库仑力不足以抵消在电场起拉伸作用的静电力的增加[14],使得纤维直径变大,进而导致纤维膜的拉伸强度得到提升。
2.3 透明质酸分子量对诱导层亲水性能的影响
透明质酸是由D-葡糖醛酸和N-乙酰葡糖胺以β-1,3糖苷键连接组成的双糖重复单元的多糖链,含有大量羧基和羟基,在水中可以形成大量的分子内和分子间氢键[15]。由于单糖残基间的β连接键和大量的链内氢键,以及外伸的负电荷羧基之间的相互斥力,不同分子量的透明质酸溶解速度不同。由图3和表3可见,随着分子量的增大,透明质酸的分子链越长,测得的水滴静态接触角越大,用其制备的诱导层亲水性越差。

图3 涂覆不同分子量透明质酸的复合补片表面接触角水滴图型
注:a. 2000 kDa;b. 800 kDa;c. 200 kDa;d. 50 kDa;e. 10 kDa;f. 1 kDa。
表3 透明质酸分子量对复合补片接触角的影响( ±s,n=5)
±s,n=5)
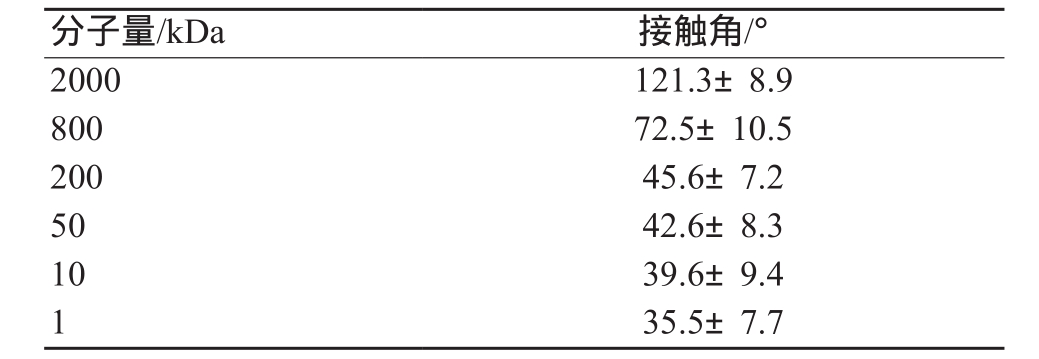
分子量/kDa 接触角/°2000 121.3±8.9 800 72.5±10.5 200 45.6±7.2 50 42.6±8.3 10 39.6±9.4 1 35.5±7.7
不同分子量的透明质酸在生物体内的生理作用不同[16],当分子量大于2000 kDa时,透明质酸具有良好的保湿性和润滑性,并抑制细胞的移动、增生、分化;当分子量小于500 kDa时,透明质酸具有清除自由基、促进细胞修复和创伤愈合、促进骨和血管生成的效果。因此,综合诱导层亲水性,选定分子量200 kDa的透明质酸为诱导层所选材料。
3 结论
本研究采用静电纺丝与等离子体处理技术制备了一种新型腹壁疝修补用复合补片,考察了诱导层与防粘连层的厚度设计对复合补片的影响,研究了纺丝液质量分数、透明质酸分子量对防粘连层纤维丝和诱导层亲水性能的影响。结果表明,诱导层和防粘连层的厚度最优设计为0.05~0.10 mm;纤维丝直径和纤维膜的拉伸强度随着纺丝液质量分数增加而增大,当纺丝液质量分数为7%时,得到的纤维膜形貌均匀;结合生理功能和亲水效果,选定分子量200 kDa的透明质酸为诱导层所选材料。
相较于单一结构的传统补片材料,本实验设计的复合补片引入了防粘连层和诱导层的概念。静电纺丝工艺制备的防粘连层具有独特的三维孔隙结构,可以阻挡成纤维细胞的长入,进而有效降低术后腹腔脏器和修补区域粘连的发生;由透明质酸构成的诱导层有望促进腹膜间皮细胞的生长,激发腹膜内源性修复,减轻患者不适和慢性炎症发生。下一步将通过动物实验验证其有效性。
[1] Deeken CR,Lake SP.Mechanical properties of the abdominal wall and biomaterials utilized for hernia repair[J].J Mech Behav Biomed Mater,2017,74:411-427.
[2] 陈柳莹,张杰,贾忠,等.腹壁疝补片的应用现状及展望[J].医学研究杂志,2018,47(5):18-22.
[3] Qiao J,Jiang Z,Yang Y,et al.Study of a new biodegradable hernia patch to repair abdominal wall defect in rats[J].Carbohyd Polym,2017,172:255-264.
[4] Shokry MM,Khalil IA,El-Kasapy A,et al.Multifunctional prosthetic polyester-based hybrid mesh for repairing of abdominal wall hernias and defects[J].Carbohyd Polym,2019,223:115027.
[5] Dreger NZ,Fan ZB,Zander ZK,et al.Amino acid-based Poly(ester urea) copolymer films for hernia-repair applications[J].Biomaterials,2018,182:44-57.
[6] 朱小倩,蒋金华,陈南梁,等.不同结构聚丙烯疝修补片定型工艺及结构参数[J].东华大学学报(自然科学版),2018,44(6):896-902.
[7] 夏克尔·赛塔尔,李彦,乔燕莎,等.疝气补片及其高生物相容性发展现状和趋势展望[J].纺织导报,2018,(5):42-46.
[8] 刘文博,高茗.可重塑生物补片在疝及腹壁外科的应用和展望[J].海军医学杂志,2016,37(4):378-381.
[9] 杨晓峰,叶小龙,黄江龙,等.纳米仿生防粘连复合补片修复大鼠腹壁缺损中胶原合成功能的研究[J].中华疝和腹壁外科杂志(电子版),2018,12(1):14-21.
[10] Sanbhal N,Mao Y,Sun G,et al.Surface modification of polypropylene mesh devices with cyclodextrin via cold plasma for hernia repair: characterization and antibacterial properties[J].Appl Surf Sci,2018,439:749-759.
[11] 王宪朋,刘阳,王传栋,等.静电纺丝法制备小口径胶原-聚乳酸人工血管[J].复合材料学报,2017,34(11):2550-2555.
[12] 秋晓峰,罗炜,屈雪,等.溶液喷纺法制备聚乳酸/锂藻土复合纳米纤维膜及其性能[J].功能高分子学报,2019,32(4):454-462.
[13] 赵月,陈灶妹,何婷,等.PEG/PLGA纳米纤维膜的制备及其参数优化[J].生物医学工程研究,2017,36(3):262-267.
[14] 李俊起,王宪朋,刘阳,等.聚乳酸-透明质酸复合膜的制备及其性能研究[J].生物医学工程研究,2018,38(1):95-98.
[15] 狄嘉伟,李想,谢瑞敏,等.透明质酸及其衍生物影响成骨细胞功能:分子机制与应用价值[J].中国组织工程研究,2018,22(18):2927-2932.
[16] 黄岳山,潘艺茗,薛静.不同相对分子量透明质酸功能及应用的研究[J].透析与人工器官,2011,22(2):10-13.
Study on Preparation and Properties of a New Composite Patch for Abdominal Hernia Repair