多通道并行采集技术在3.0 T术中磁共振成像的应用价值
引言
术中磁共振成像(Intraoperative Magnetic Resonance Imaging,iMRI)是一种能够在神经外科手术过程中对脑组织进行实时成像的新技术[1]。随着iMRI在临床应用的推广,越来越多的研究表明,这项技术能够显著提升颅脑肿瘤的全切率和手术的精准性[2-3]。但iMRI的应用也将增加手术麻醉时长。已有研究表明,长时间的麻醉会对机体产生影响,增加术后并发症[4-6]。Sano等[4]通过大鼠实验发现麻醉时间过长会影响机体的呼吸、循环和内分泌系统。刘欢等[5]探究麻醉后小鼠身体机能的研究也发现,长时间麻醉会对小鼠的认知功能产生影响。因此,在iMRI引导下的手术中控制术中成像时长十分重要。
并行采集技术是一种通过相位编码方向的图像欠采样和空间信息的特殊重构来提高磁共振成像速度的方法[7]。这种成像方法已经被广泛应用于常规临床MR扫描之中[8]。但目前,国内外尚没有关于并行采集技术在iMRI系统中的应用研究。为了探究并行采集技术在iMRI引导下神经外科手术的临床应用价值,本研究基于我院3.0 T高场强iMRI设备,对常规采集技术和并行采集技术下的图像采集时间和图像质量进行对比研究。
1 材料与方法
1.1 一般资料
本研究招募了20位正常人作为被试,年龄42~61岁,女性12例,男性8例。被试入组标准:① 体内无金属置入物;② 无磁共振扫描禁忌症。排除标准:① 颅内有明显病变;② 头外伤史、手术史。本研究已由本院伦理委员会审核批准,上述被试在扫描前均已签署知情同意书。
1.2 仪器设备
我院iMRI系统采用Siemens Verio dot 3.0 T设备。术中扫描时,磁体需从磁体间通过天花板滑轨技术移至手术间。术间配备的线圈为8通道头部柔线圈,分为上下两部分,可固定于手术头架上。
1.3 扫描方法
被试呈仰卧位,平躺于术间的手术床,头部上下用8通道头部软线圈覆盖。为减少术间复杂环境的干扰,接通头部柔线圈后对手术间进行断电。然后分别进行常规图像采集和并行采集。本研究采用的并行采集技术是基于西门子MRI设备的一般性自动校准部分并行采集(Generalized Autocalibrating Partially Parallel Acquisitions,GRAPPA),加速因子为2,其余参数与常规采集保持一致。扫描序列包括:T1轴位,T2轴位,T2 液体衰减反转恢复(Fluid Attenuated Inversion Recovery,FLAIR)轴位和T2矢状位。每个被试扫描前均进行手动匀场校正。具体的扫描参数和扫描时长如表1所示。
表1 扫描序列参数表
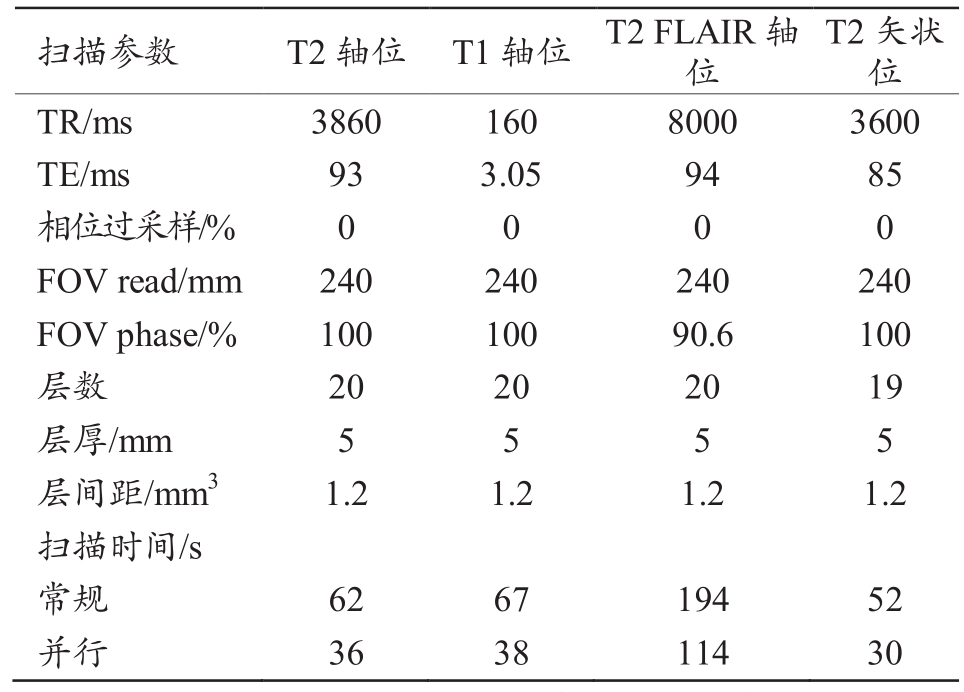
注:FLAIR:液体衰减反转恢复;TR:重复时间;TE:回波时间;FOV read:导航条读出方向的大小;FOV phase:导航条相位方向的大小。
扫描参数 T2轴位 T1轴位 T2 FLAIR轴位T2矢状位TR/ms 3860 160 8000 3600 TE/ms 93 3.05 94 85相位过采样/% 0 0 0 0 FOV read/mm 240 240 240 240 FOV phase/% 100 100 90.6 100层数 20 20 20 19层厚/mm 5 5 5 5层间距/mm3 1.2 1.2 1.2 1.2扫描时间/s常规 62 67 194 52并行 36 38 114 30
1.4 被试影像分析
由于人脑组织的复杂性,术中MR图像的客观评价不再按照传统的SNR进行[9-10]。目前,国际上组织影像评价指标通常用图像不均匀性指标(Non-Uniformity Index,NUI)来表征[11-12]。因此,本研究选取常规和并行采集下各序列的中间层图像进行NUI的计算。我们在每个序列的中间层图像中选择8个面积均为200 mm2的感兴趣区域(Region of Interest,ROI)(图 1),提取信号强度(Signal Intensity,SI),得到 SI最大值(SImax)和最小值(SImin)进行NUI的计算[7],见式(1)。
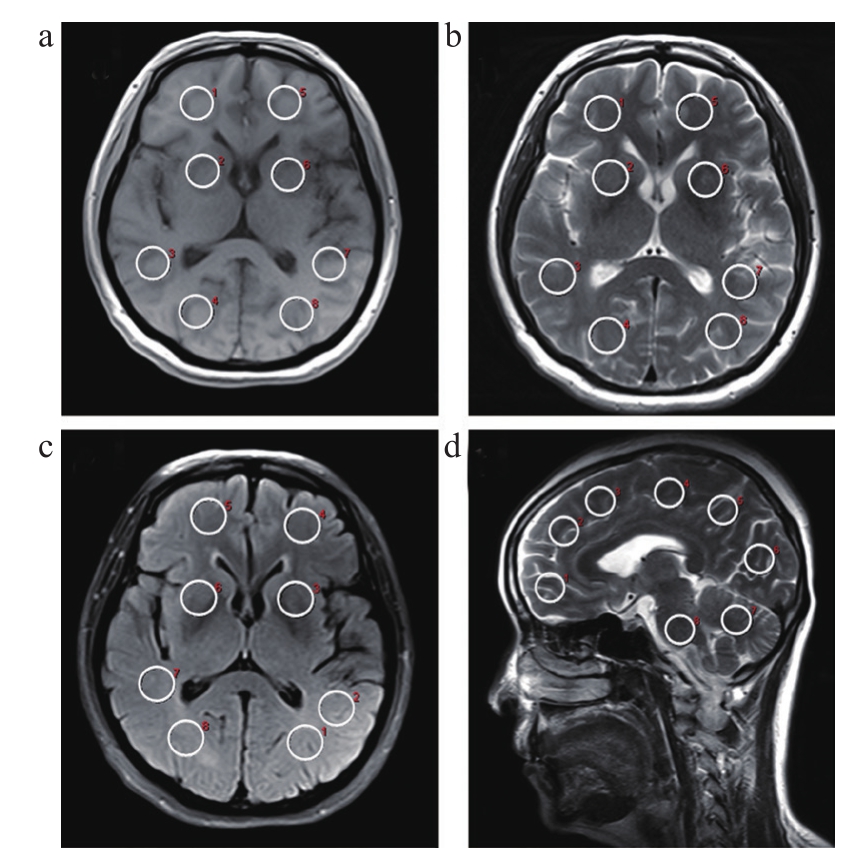
图1 四个扫描序列中间层图像的ROI分布
注:a. T1轴位图;b. T2轴位图;c. T2FLAIR轴位图;d. T2加权矢状位图。
1.5 主观评价分析
扫描完成后,对图像进行匿名化,由我院两名高年资诊断医师采用盲法对图像进行主观评价,如果出现分歧,两位诊断医师协商后给出一致意见。主观评价采用四分法:4=脑组织、颅骨等结构显示清楚,无伪影;3=脑组织、颅骨等结构显示较为清楚,无伪影;2=脑组织、颅骨等结构显示一般,有伪影但不影响诊断;1=脑组织、颅骨等结构显示不清楚,伪影较严重,影响诊断。
1.6 统计学分析
获取四个序列扫描在并行采集技术下的扫描时间总和(∑并行)和常规采集扫描时间总和(∑常规),并计算∑并行相较于∑常规缩短的扫描时长占比,即(1-∑并行/∑常规)×100%。基于SPSS 21.0统计学软件,对两种技术下得到图像的NUI进行配对t检验,对主观评价得分进行非参数检验,对将P<0.05认为差异具有统计学意义。
2 结果
2.1 扫描时长
通过计算常规采集和并行采集下的总扫描时长可以发现,四个扫描序列在常规采集的总扫描时长为375 s,而并行采集所用的总扫描时长为218 s。对比常规和并行采集下的总扫描时长可以发现,采用并行采集技术(加速因子为2)的总扫描时长相较于常规采集缩短了41.9%。
2.2 NUI结果
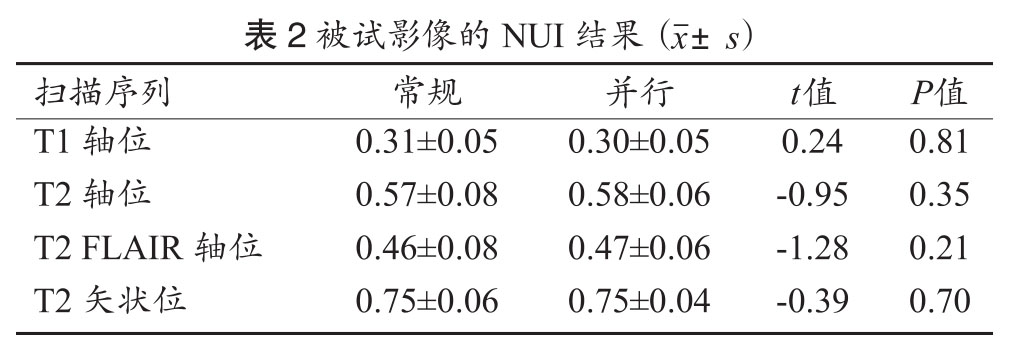
四个扫描序列的NUI值如表2所示,统计结果显示常规和并行采集技术下的NUI均无显著差异(P>0.05),见图2。
images/BZ_102_897_2739_917_2772.png±s值 值
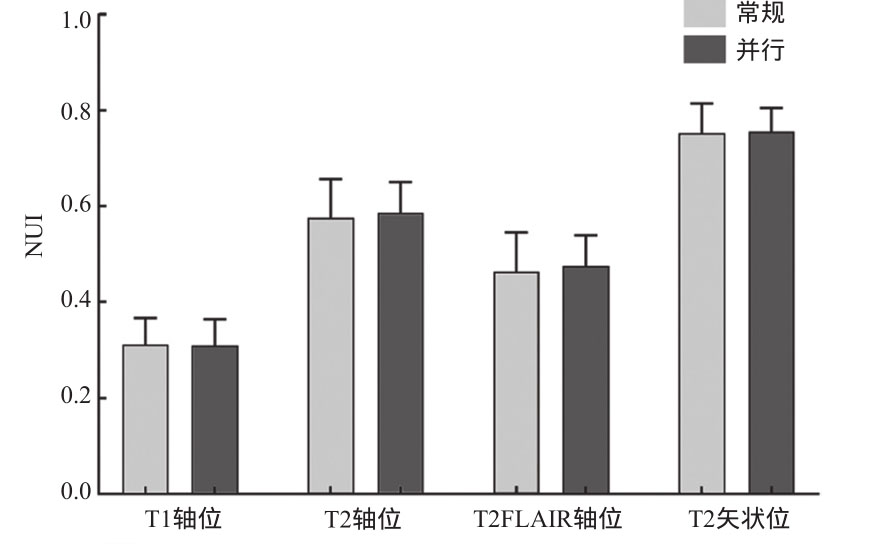
图2 四个扫描序列在常规采集和并行采集下的NUI比较
2.3 主观评价分析结果
主观评价得分的统计检验结果可以得出,并行采集下四个扫描序列的主观评价得分与常规扫描无显著的统计学差异(P>0.05),见表 3。
表3 四个序列常规和并行采集下的主观评价得分

扫描序列 常规[中位数(四分位距)]并行[中位数(四分位距)] Z P T1 轴位 3(3~3)3(3~3)-0.49 0.62 T2 轴位 2(2~2)2.5(2~3)-1.86 0.06 T2 FLAIR 轴位 2(2~3)2(2~3)-1.85 0.06 T2 矢状位 2(2~3)2.5(2~3)-0.45 0.65
3 讨论
有研究表明,手术时长的过度延长会影响身体机能,增加术后并发症的发生率[4-6]。作为一项先进的影像辅助手术的技术,iMRI虽然能够帮助临床医生在手术过程中实时掌握肿瘤的位移和范围,但也会增加一定的手术麻醉时长。为了更好地发挥iMRI的优势,降低成像时长是控制应用iMRI进行颅脑手术时长的必要手段。并行采集技术是目前能够有效降低成像时长的一种技术手段,所以本研究基于西门子的GRAPPA技术,探究了其对术中颅脑成像的成像时长、NUI和主观评价得分的影响。
并行采集技术是近年来用于临床的MR快速采集新技术,它是基于并行采集算法、多通道接收线圈和高性能计算机技术发展的结合体,可以帮助缩短成像时间。西门子的GRAPPA并行采集技术基于K空间信号整合,在复杂频域内对信号数据进行处理,在傅里叶变换之前结合已接收的线圈信息进行频域重建[13]。GRAPPA技术不需要精准、复杂的线圈校准,只要提前采集部分的K空间填充线就能实现自动校正,获得MR图像。已有的研究证实了并行采集技术在常规临床MRI中能够有效降低成像时长[10,14]。但尚没有研究将这一技术用于iMRI系统之中,探究其临床价值。本研究基于加速因子为2的GRAPPA并行采集技术,通过对比其与常规采集下总扫描时长,同样发现了并行采集技术能够有效降低扫描时长,即加速因子为2的GRAPPA并行采集技术为术中成像的四个扫描序列节省了41.9%的成像时长,可以有效地控制iMRI引导下手术的术中成像时长,以期帮助降低手术麻醉时长。
基于K空间过疏采集的并行采集技术虽然能够帮助降低成像时长,但也会因为加速因子的增加造成图像信噪比的丢失[15]。因此,我们进一步评估了并行采集技术下iMRI的图像质量。由于术中成像环境和扫描部位的复杂性,会导致边界信号采集不足,结合先前的相关研究结果,本研究采用NUI来评估图像质量更加合理[11-12]。NUI是指射频激励场、接收线圈灵敏度的不均匀性,以及磁场梯度涡流等因素引起的磁流变学中常见的平滑强度的变化。磁体本身的磁场均匀度、梯度脉冲、射频、涡流等因素都会影响到NUI[16-17]。目前,在MR扫描过程中,NUI不能被实时监测到,很难通过肉眼辨别,但却能够影响到图像的后处理和诊断[18-19]。本文采用的NUI计算方法是基于峰值差的非均匀性度量,被美国电气协会认为是最适合对磁场不均匀性进行评估的标准[12]。研究结果显示,并行采集技术下iMRI四个扫描序列的NUI与常规采集无显著的统计学差异。先前有关并行采集的研究中,Aja-Fernández等[20]提出,在各场强的头颅MRI中,如果加速因子小于2.5,将不会对图像质量造成影响,该结论与本研究的结果一致。因此可以表明,虽然iMRI的成像环境复杂,但加速因子为2的并行采集技术在iMRI的应用仍然不会对图像的均匀度产生影响。
为了更进一步评估并行采集技术下的iMRI是否会对影像诊断产生影响,本研究由两名高年资诊断医师采用盲法对图像进行了主观评价。盲法的应用能够有效减少主观因素的影响[21]。通过统计学比较,结果发现并行采集和常规采集技术下,四个扫描序列的主观评价得分无显著的统计学差异,表明并行采集技术下的iMRI不会影响影像诊断。将主观评价结果结合图像扫描时长和NUI的统计学结果,可以进一步表明并行采集技术在iMRI系统中的应用可以有效降低成像时长,且不会对图像质量和医师诊断产生影响,具有较大的临床应用价值。
本研究还有一定的局限性。首先,纳入的样本数量不够多,后续的研究需要进一步增大样本数量来验证本文结果的可靠性。其次,由于伦理限制,本文的研究对象基于正常被试,缺乏手术过程中患者术中图像的对比。最后,本研究针对临床常用的四个扫描序列进行了对比研究,未来的研究还可以纳入更多的扫描序列。
4 结论
本研究首次将并行采集技术应用于iMRI系统进行对比探究,结果表明并行采集技术不仅可以大幅降低术中成像时间,而且不会对图像质量和影像诊断产生影响,有助于提高手术效率、保证患者的安全,对iMRI在神经外科手术的应用具有一定的指导意义。
[1]Senft C,Bink A,Franz K,et al.Intraoperative MRI guidance and extent of resection in glioma surgery: a randomised, controlled trial[J].Lancet Oncol,2011,12(11):997-1003.
[2]丁大领,赵爱玲,王朝艳,等.术中磁共振联合神经导航在丘脑胶质瘤手术中的应用[J].中国实用神经疾病杂志,2019,22(3):253-259.
[3]Shahar T,Rozovski U,Marko NF,et al.Preoperative imaging to predict intraoperative changes in tumor-to-corticospinal tract distance: an analysis of 45 cases using high-field intraoperative magnetic resonance imaging[J].Neurosurgery,2014,75(1):23-30.
[4]Sano Y,Ito S,Yoneda M,et al.Effects of various types of anesthesia on hemodynamics, cardiac function, and glucose and lipid metabolism in rats[J].Am J Physiol Heart Circ Physiol,2016,311(6):H1360-H1366.
[5]刘欢,许芳霞,崔银,等.GLYX-13对小鼠长时间异氟醚麻醉后认知功能的影响[J].中华麻醉学杂志,2017,37(10):1196-1200.
[6]康丹.颅脑损伤患者开颅手术的围手术期护理效果观察[J].中国医药指南,2019,17(20):183-184.
[7]Griswold MA,Blaimer M,Breuer F,et al.Parallel magnetic resonance imaging using the GRAPPA operator formalism[J].Magn Reson Med,2005,(54):1553-1556.
[8]Harisinghani MG,O’Shea A,Weissleder R.Advances in clinical MRI technology[J].Sci Transl Med,2019,(11):523.
[9]韩林梅,俞琴.并行采集技术在1.5T 8通道相控阵线圈头颅3D TOF MRA中的优化:体模研究[J].中国医学影像技术,2019,35(3):423-427.
[10]顾海峰,郑玲,郝绍伟,等.磁共振并行采集技术与常规采集技术对图像质量影响的综合评价[J].医学研究生学报,2012,25(1):35-38.
[11]Belaroussi B,Milles J,Carme S,et al.Intensity non-uniformity correction in MRI: existing methods and their validation[J].Med Image Anal,2006,10(2):234-246.
[12]Felemban D,Verdonschot RG,Iwamoto Y,et al.A quantitative experimental phantom study on MRI image uniformity[J].Dentomaxillofac Rad,2018,47(6):20180077.
[13]Blaimer M,Breuer F,Mueller M,et al.SMASH, SENSE, PILS,GRAPPA. How to choose the optimal method[J].Top Magn Reson Imaging,2004,(15):223-236.
[14]公伟,迟洁茹,杨新强.基于GRAPPA图像重建的采样轨迹[J].计算机应用,2010,30(7):1847-1848.
[15]泮智勇,丁雪委,王世威,等.32通道头部线圈与并行采集技术iPAT在头颅MRA检查中的应用[J].医学影像学杂志,2013,23(11):1673-1675.
[16]高宇,黎良山,王栋.柔性线圈与硬质线圈在肩关节MRI图像质量的比较[J].浙江临床医学,2019,21(3):388-390.
[17]Damen FC,Cai K.B1-non-uniformity correction of phasedarray coils without measuring coil sensitivity[J].Magn Reson Imaging,2018,(51):20-28.
[18]Sled JG,Pike GB.Understanding intensity non-uniformity in MRI[J].Lecture Notes in Computer Science,1998:614-622.
[19]Dadar M,Fonov VS,Collins DL.A comparison of publicly available linear MRI stereotaxic registration techniques[J].Neuroimage,2018,(174):191-200.
[20]Aja-Fernández S,Vegas-Sánchez-Ferrero G,Tristán-Vega A.Noise estimation in parallel MRI: GRAPPA and SENSE[J].Magn Reson Imaging,2014,32(3):281-290.
[21]朱妍昕,王霞,徐维.循证医学数据库信息模型中证据强度模块的构建及验证[J].中华医学图书情报杂志,2019,28(6):35-41.
Application Value of Multi-channel Parallel Acquisition Technique in 3.0 T Intraoperative Magnetic Resonance Imaging