重建层厚(1/2/3 mm)对人工智能检测肺结节效能的影响
引言
肺结节是肺癌的早期表现,其检出率随着薄层计算机断层扫描(Computed Tomography,CT)技术的发展而提高,国内大型三级医院现已大部采集薄层图像,但明显增多的CT数据不仅增加了影像科医师的阅片负担[1],同时对医院PACS的传输、硬盘的存储等方面也带来了大量的负担,医院每年对此付出的经济成本相当巨大[2-3]。目前,很多基层医院由于财政投入不足,使用的CT设备及网络建设还相对落后,受限于机器的球管热容量、辐射剂量以及网络存储空间、传输速度等条件,并不适合对全部胸部CT采用薄层后处理重建。近年来,人工智能(Artificial Intellience,AI)技术在各个行业中都有了广泛的应用,基于深度学习[4]的AI辅助诊断系统在影像学诊断肺结节方面的应用有了突飞猛进的进展[5-6],提高了早期肺癌的检出率。应用AI技术对海量CT图像进行初步筛查并标记可疑结节病变,可以帮助三级医院影像医师减少工作量并提高诊断准确率[7-8],也能帮助基层影像医师降低结节的漏诊率。目前国内各级医院利用AI辅助筛查的胸部CT层厚不尽相同,主要应用在1/2/3 mm层厚的CT图像,现在还没有不同层厚间效能对比方面的研究文章,本研究通过分析评价AI所检出的总结节、>4 mm结节、<4 mm结节、实性结节以及亚实性结节的综合效能,从而得出相对适合AI检出肺结节的最佳胸部CT层厚。
1 资料与方法
1.1 研究对象
前瞻性收集2018年11月1日至12月31日在我院影像科门诊接受常规胸部CT检查的280例患者,经排除,符合研究条件的共190例,其中男性101例,女性89例;年龄范围19~84岁,平均年龄(55.7±7.65)岁。纳入标准:① 患者年龄在18岁以上有肺结节患者;② 经AI推测结节数不超过50个;③ 排除带有伪影的影像资料;④ 排除肺部弥漫性病变、肺炎的影像资料。
1.2 采用设备及扫描技术
采用西门子二代炫速双源CT,吸气屏气状态下肺尖扫描至两侧肾上腺。扫描参数:管电压120 kV,自动管电流设置,探测器准直器128×0.6 mm,机架旋转时间为0.5 s/周,矩阵:512×512。观察CT图像的肺窗窗宽1200 HU,窗位600 HU;必要时手动调整合适的窗条件。扫描后数据分别以1/2/3 mm层厚行骨算法重建图像。
1.3 研究方法及图像评价
将190例胸部CT行1/2/3 mm层厚重建,卷积核B70f,肺窗。所有重建后数据传输至工作站,由推想公司基于深度学习模型的AI软件将3种层厚的CT图像分别利用AI进行结节检测,分别记录三组层厚的所有肺结节、>4 mm结节、<4 mm结节、实性结节以及亚实性结节的检测个数。所有胸部CT分析由两名十年以上诊断经验主治医师和一名十五年以上诊断经验的副主任医师借助AI软件对190例病例图像的肺结节制定金标准。统计分析三组肺结节的检出情况及差异。
1.4 统计学分析
采用SPSS 20.0统计软件进行数据录入、整理及统计学分析。分别计算AI对三组数据(各组总结节、>4 mm结节、<4 mm结节、实性结节以及亚实性结节)检出的敏感度及假阳性率,并对三组肺结节数据进行单因素方差分析或非参数秩和检验。P<0.05为差异有统计学意义。
2 结果
2.1 1/2/3 mm层厚检出结节的数目
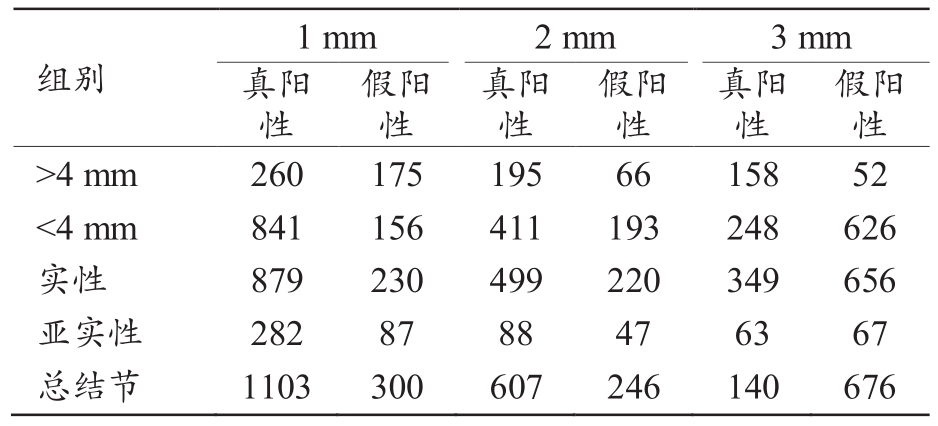
190例胸部CT,金标准共检出1333个肺结节。AI软件在1 mm层厚共检出1403个结节,其中正确结节1103个,错误结节300个;2 mm层厚共检出853个结节,其中正确结节607个,错误结节246个;3 mm层厚共检出1077个结节,其中正确结节401个,错误结节676个。1 mm层厚检测的结节最多,明显优于2和3 mm(图1),但是检测>4 mm的结节假阳性较多;2 mm层厚检测出的结节数要低于1 mm图像,而假阳性结节数也随之减少,尤其是检测>4 mm的结节,假阳性数明显低于1 mm图像;3 mm层厚检测的结节最少,假阳性也是最多,见表1。
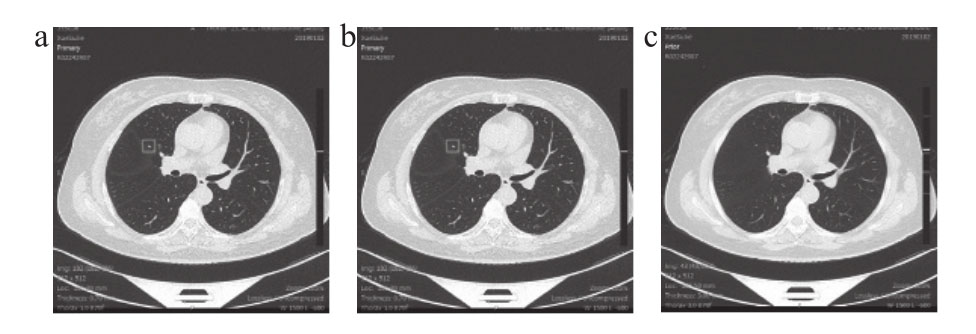
图1 AI辅助肺结节检测系统检测结果
注:在1 mm层厚胸部CT图像检测到了一个结节,但在2、3 mm层厚胸部CT图像中并未检出。a. 1 mm层厚胸部CT图像; b. 2 mm层厚胸部CT图像;c. 3 mm层厚胸部CT图像。
表1 1/2/3 mm层厚利用AI检出结节的数目(个)
组别1 mm 2 mm 3 mm真阳性假阳性真阳性假阳性真阳性假阳性>4 mm 260 175 195 66 158 52<4 mm 841 156 411 193 248 626实性 879 230 499 220 349 656images/BZ_112_1296_1515_1500_1556.png282 87 88 47 63 67images/BZ_112_1296_1568_1500_1610.png1103 300 607 246 140 676
2.2 1/2/3 mm层厚检出结节的敏感度比较
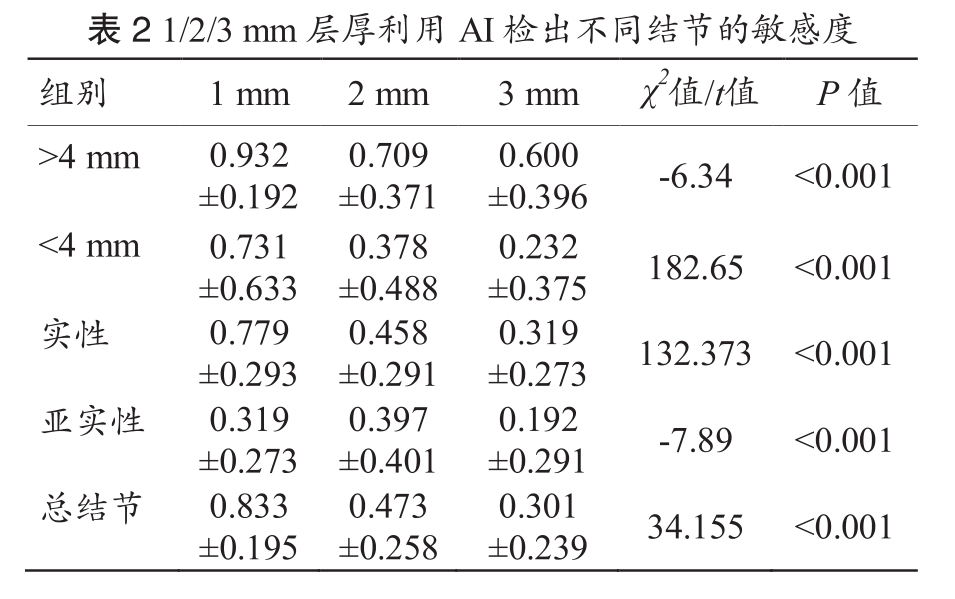
AI软件在1 mm层厚检测所有结节的敏感度为(0.833±0.195),2 mm层厚检测所有结节的敏感度为(0.473±0.258),3 mm层厚检测所有结节的敏感度为(0.301±0.239),P<0.001,三组间差异具有统计学意义,见表 2。
?
2.3 1/2/3 mm层厚检出结节的假阳性率比较
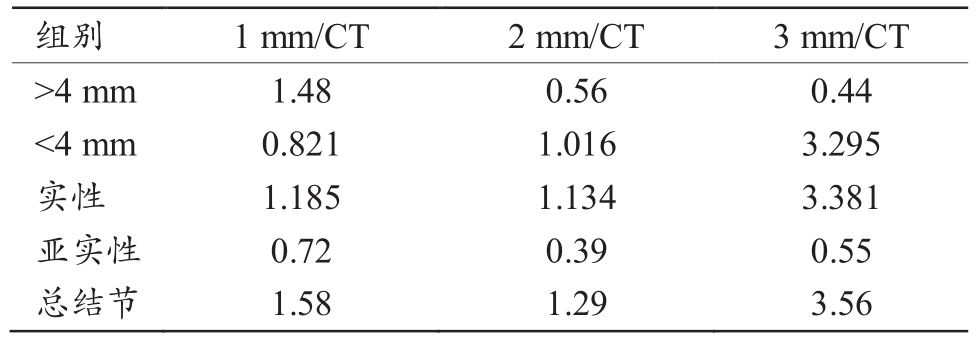
AI软件在1 mm层厚检测所有结节的假阳性率为1.58/CT,2 mm层厚检测所有结节的假阳性率为1.29/CT,3 mm层厚检测所有结节的假阳性率为3.56/CT;在1 mm层厚图像检测>4 mm结节假阳性率最高,其余相对较低;2 mm层厚图像检测亚实性结节假阳性率最低,其余介于1、3 mm层厚之间;3 mm层厚图像检测>4 mm结节假阳性率最低,其余都很高(图1)。
表3 1/2/3 mm层厚利用AI检出不同结节的假阳性率
组别 1 mm/CT 2 mm/CT 3 mm/CT>4 mm 1.48 0.56 0.44<4 mm 0.821 1.016 3.295实性 1.185 1.134 3.381亚实性 0.72 0.39 0.55总结节 1.58 1.29 3.56
3 讨论
本研究结果显示AI软件在三种层厚胸部CT图像的肺结节检测中,1 mm层厚检出的敏感度最高,远高于2、3mm,分析其原因是因为我们使用的基于深度学习的薄层检测模型,此模型大部分是通过1 mm层厚图像的人工标注数据集进行深度学习;三组层厚AI的结节检测假阳性率均相对较高,尤以3 mm层厚为著,这是由于肺内气管、血管复杂,肺结节位置又具有多样性,极易混淆[9-11]。同时,某些肺结节易与肺正常组织粘连,不利于检测,增加了AI辅助检查系统的假阳性率[12-13]。
4 mm以上的肺结节更具有临床意义,也是需要随访的对象[14-15],AI在>4 mm结节检测中,随着层厚的增厚,敏感度逐渐降低[16],但都在较高的水平,3 mm层厚图像结节检出敏感度相对较低,也达到了(0.600±0.396)的。有研究表明,AI辅助诊断系统对结节的检出率随结节的减小而降低[17-18],对直径>4 mm的肺结节,AI辅助检测系统对肺结节的检出率为100%,但对直径≤4 mm的肺结节,其检出率降至70%[19-20]。而AI在>4 mm结节检测中,2 mm层厚的假阳性率却很低,只有1 mm层厚的三分之一左右。
本研究的局限性在于数据样本量不足,4 mm以上的结节数量较少,因此结果可能存在一定的选择性偏倚。
综上所述,AI在1 mm层厚胸部CT的肺结节检测中,虽然存在一定的假阳性率,但相当高的敏感度可以确保结节检出率的提升,能极大降低漏诊的发生概率,并能提高影像医师的工作效率;其层厚最薄,数据量最多,所占用的存储空间最大,建议具有较好经济基础,高端CT设备,患者更多的大型三级医院使用1 mm作为AI检测肺结节的首选层厚。AI在>4 mm结节的检测中,2 mm层厚检测的假阳性率很低,敏感较高,考虑其占用存储较小,对设备要求不高,更适合经济基础比较薄弱,诊断水平相对较低的基层医院使用。
[1]Sui Y,Wei Y,Zhao D.Computer-aided lung nodule recognition by SVM classifier based on combination of random undersampling and SMOTE[J].Comput Math Methods Med,2015,12(8):368-373.
[2]吴平.DICOM医学图像格式转换与肺结节检测方法研究[D].昆明:昆明理工大学,2013.
[3]Hinton GE,Salakhutdinov RR.Reducing the dimensionality of data with neural networks[J].Sci,2016,31(3):504-507.
[4]Kligermans C,White CS.The effect of computer aided detectionon radiologist performance in the detection of lung cancers previously missed on a chest radiograph[J].J THORAC IMAG,2013,28(4):244-252.
[5]Sahiner B,Chan HP,Hadjiiski LM,et al.Effect of CAD on radiologists’ detection of lung nodules on thoracic CT scans:analysis of an observer performance study by nodule size[J].Acad Radiol,2009,16(12):1518-1530.
[6]Xia Y,Lu S,Wen L,et al.Automated identification of dementia using FDG-PET imaging[J].Biomed Res Int,2014,10(5):421-425.
[7]金文忠,陆耀,汪阳.基于人工智能的胸部CT智能辅助诊断系统在LDCT数据集上的应用研究[J].中国计算机医学影像,2018,24(5):373-377.
[8]万祥慧,巩武贤,邵江,等.MSCT重建、重组层厚对肾上腺MPR图像质量的影响[J].医学影像学杂志,2018,12(3):1006-1011.
[9]谷宇,吕晓琪,杨立东,等.基于CT影像的肺结节计算机辅助检测技术进展[J].重庆医药,2017,18(6):839-842.
[10]李甜,李晓东,刘敬禹.人工智能辅助诊断肺结节的临床价值研究[J].中国全科医学,2020,23(7):828-831.
[11]Brown S,Goldin JG,Suh RD,et al.Lung micronodules:automated method for detection atthin-section CT-initial experience[J].Radiology,2003,226(1):256-262.
[12]吴光耀,伍建林.基于CT的计算机辅助检测与诊断肺结节技术研究进展[J].中华医学影像技术杂志,2018,34(7):1114-1117.
[13]萧毅,夏晨,张荣国,等.人工智能技术在医学影像中的应用讨论[N].第二军医大学报,2018,8(13):813-818.
[14]李欣菱,郭芳芳,周振,等.基于深度学习的人工智能胸部CT肺结节检测效能评估[J].中国肺癌杂志,2019,22(6):336-340.
[15]张雪菊.《中国专家对肺结节诊断与治疗共识的解释》(2018年版)[J].中国实用诊断与治疗杂志,2019,33(1):1-3.
[16]萧毅,刘士远.肺结节影像人工智能技术现状与思考[J].肿瘤影像学,2018,27(4):249-252.
[17]王伟伟.64排螺旋CT不同重建层厚对肺小结节检出能力的比较[J].影像研究与医学应用,2020,4(3):189-191.
[18]杨兴云,宋立江,王涛,等.多层螺旋CT图像后处理技术在肺部结节鉴别诊断中的应用研究[J].中国医学装备,2019,8(4):33-36.
[19] Schwyzer M,Ferraro DA,Muehlematter UJ,et al.Automateddetection of lung cancer at ultralow dose PET/CT by deep neural networksinitial results[J].Lung Cancer,2018,1(26):170-173.
[20]史燕杰,张晓锦,李剑颖,等.多排低剂量螺旋CT鉴别肺结节:两种重建层厚比较[J].中华医学影像技术杂志2010,26(8):1477-1480.
Effect of Reconstruction Thickness (1/2/3 mm) on Effectiveness of Artificial Intelligence in Detecting Pulmonary Nodules