常规超声及声辐射力脉冲成像技术在乳腺癌免疫组化分型中的应用研究
引言
乳腺癌是目前女性最常见的恶性肿瘤之一,也是癌症死亡的主要原因。据统计,全球每年有167万新确诊的乳腺癌患者,其中有52万人因乳腺癌而死亡[1]。乳腺癌的各种分子亚型具有不同的生物学特征、临床治疗方式和预后,且其生物学行为、浸润程度、组织学分级、高度异质性等会导致形态学表现的多变性,因此,乳腺癌的形态学表现与分子生物学之间存在一定的相关性[2-4]。硬度改变也属于乳腺肿瘤的形态学改变之一,声辐射力脉冲成像(Acoustic Radiation Force Impulse,ARFI)是一种检测组织弹性的新兴的超声检查技术,根据其剪切波速度值的高低来反映组织的软硬程度。本文旨在研究乳腺癌常规超声征象及应用ARFI技术测定的乳腺癌病灶内部的剪切波速度值(Shear Wave Velocity,SWV)在免疫组化分型中的应用价值,为乳腺癌的诊疗和预后评估提供有价值的信息。
1 材料与方法
1.1 研究对象
选取2015年1月至2016年12月于我院行乳腺穿刺活检或乳腺手术后经病理检查确诊的乳腺癌患者148例,年龄24~84岁,平均(53.6±12.1)岁,病灶最大径线0.5~6 cm,平均(4.4±1.1)cm,每一例均行免疫组化检查,排除术前行放化疗及内分泌治疗的患者。
1.2 仪器与方法
1.2.1 仪器
使用西门子Acuson S2000彩色多普勒超声仪器,线阵探头9L4,探头频率4~9 MHz。配备ARFI成像技术软件,用于正常组织和病变的剪切波速检测。
1.2.2 超声检查方法
患者取仰卧位,双臂抬起以完全暴露乳房。首先行常规超声检查,观察乳腺病变的大小、生长方位、形态、边界、边缘、内部回声、后方回声、有无钙化以及血流分级(按Adler 血流分级法,分为0-I级和II-III级),腋窝淋巴结有无肿大;然后切换到ARFI模式以获得病变的硬度特征,将取样框置于病变部位,嘱患者呼气后屏住呼吸,按确定键后系统会自动检测病灶的SWV。每一个病灶大小不同,至少重复测量6次,记录平均值并存储图像。仪器设定的剪切波速度值范围为0至9 m/s,为排除方法学错误,如病灶的测值为X.XX m/s,表明病变太硬,超过检测范围,为方便统计将此类数据记录为9 m/s。
1.2.3 免疫组化检测及分型标准
根据2017年的St.Gallen乳腺癌国际专家共识[5],ER、PR及Ki一67表达情况依据细胞核着色阳性的肿瘤细胞百分比,ER、PR、Ki一67阳性定义为视野中肿瘤细胞核着色细胞百分比≥1%,阴性定义为视野中肿瘤细胞核着色细胞百分比<1%。HER2过表达定义为免疫组化检测为+++,阴性定义为-~+,++者进一步行荧光原位杂交检测HerbB-2基因有无扩增,有扩增者定为阳性,无扩增者定为阴性。根据ER、PR、HerbB-2、Ki-67的表达,将乳腺癌患者免疫组化分为4型,即管腔上皮型(Luminal)A型:ER+/PR+,HerbB-2-,Ki-67低表达(<14%);B型:ER+/PR+,HerbB-2+或 ER+/PR+,HerbB-2-,Ki-67高 表达(>14%);HerbB-2过表达型 :ER-,PR-,HerbB-2 +;基底样型(三阴型乳腺癌TNBC):ER-,PR-,HerbB-2-。
1.2.4 统计学分析
应用SPSS 21.0统计软件进行分析,采用例数(n)、构成比(%)描述不同免疫组化分型的乳腺癌超声表现,采用χ2检验比较不同免疫组化分型的乳腺癌超声表现的差异,不同免疫组化分型的乳腺癌的剪切波值的正态性检验采用Shapiro-Wilk检验,剪切波值不服从正态分布,采用中位数(四分位间距)描述,统计学检验采用Kruskal-Wallis H检验。检验水准α=0.05,以P≤0.05为差异具有统计学意义。
2 结果
2.1 乳腺癌病理及免疫组化分型表达情况
本组148例乳腺癌中管腔上皮A型47例(占31.8%),管腔上皮B型53例 (占35.8%),HerbB-2过表达型28例(占18.9%),三阴型20例 (占13.5%)。其中浸润性导管癌104例,导管内癌20例,浸润性小叶癌13例,粘液癌3例,浸润性筛状癌2例,基底细胞样癌2例,浸润性假腺管型微乳头状癌2例,髓样癌1例,Paget's病(湿疹样癌)1例。
2.2 不同免疫组化分型乳腺癌常规超声征象差异
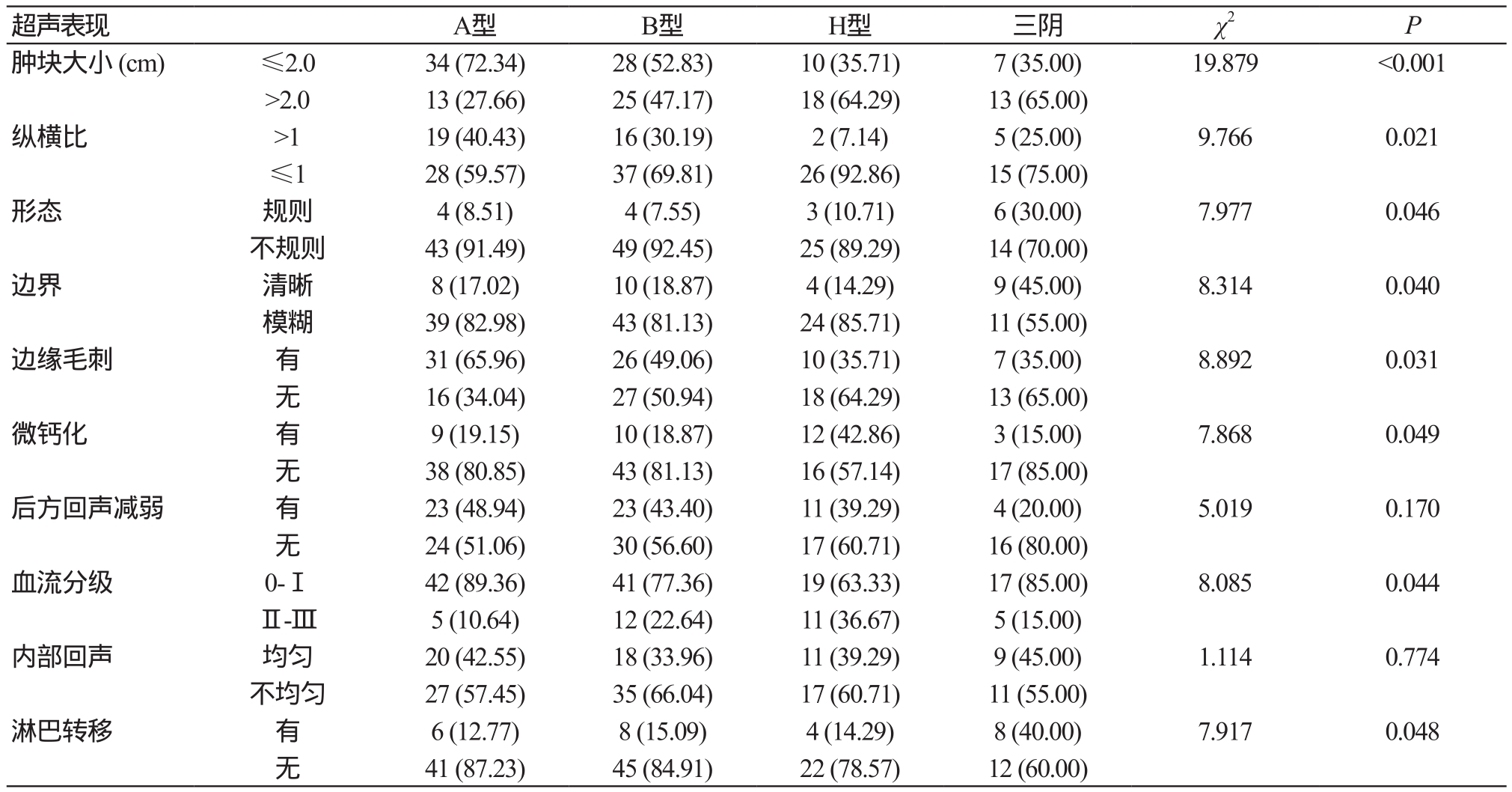
不同免疫组化分型乳腺癌的肿块大小、纵横比、形态、边界、边缘毛刺、微钙化、血流分级及淋巴结转移等常规超声表现均具有统计学差异(P<0.05)。三阴型乳腺癌肿块>2.0 cm的构成比最高(65%),HerbB-2过表达型(64.29%)及管腔上皮B型(47.17%)次之;管腔上皮A型乳腺癌纵横比大于1的比例最高(40.43%),管腔上皮B型(30.19%)及三阴型(25%)次之;三阴型乳腺癌形态规则的构成比最高(30%),HerbB-2过表达型次之(10.71%);三阴型乳腺癌边界清晰的构成比最高(45%),管腔上皮B型 (18.87%)次之;管腔上皮A型边缘毛刺的构成比最高(65.96%),管腔上皮B型(49.06%)次之;HerbB-2过表达型乳腺癌微钙化的比例最高(42.86%),管腔上皮B型(18.87%)次之;HerbB-2过表达型乳腺癌血流分级II-III级的比例最高(36.67%),管腔上皮B型(22.64%)及三阴型(15%)次之;三阴型乳腺癌淋巴转移的构成比最高(40%),管腔上皮B型(15.09%)及HerbB-2过表达型(14.29%)次之。故三阴型乳腺癌多表现为肿块>2.0 cm、形态规则、边界清晰,分别占65.00%、30.00%及45.00%(图1),并且三阴型乳腺癌淋巴结转移率较高,达40.00%;边缘毛刺、纵横比>1在管腔上皮A型中表现显著高于其他各型,分别占40.43%、65.96%(图2);HerbB-2过表达型乳腺癌常伴微钙化及血流分级Ⅱ-Ⅲ级,分别占42.86%、36.67%(图3)。管腔上皮A型乳腺癌后方回声减弱的比例最高(48.94%),但各型间差异无统计学意义(P>0.05)。三阴型乳腺癌内部回声均匀的比例最高(45%),管腔上皮B型内部回声不均匀的比例最高(66.04%),各型间差异无统计学意义(P>0.05)。见表1。
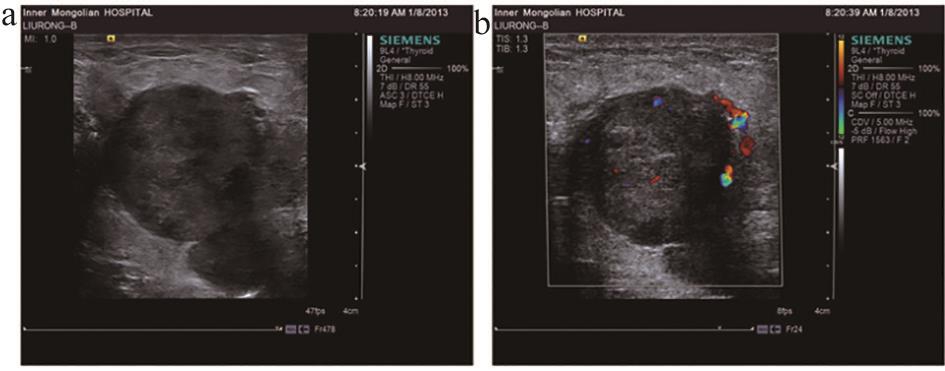
图1 三阴型乳腺癌常规声像图
注:a.二维声像图;b.彩色多普勒声像图。
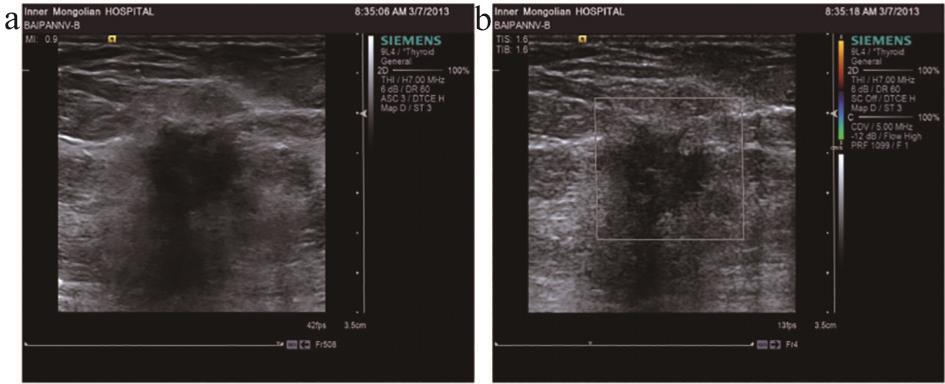
图2 管腔上皮A型常规声像图
注:a.二维声像图;b.彩色多普勒声像图。
表1 不同免疫组化分型的乳腺癌常规超声征象分析 [n (%)]
超声表现 A型 B型 H型 三阴 χ2 P肿块大小 (cm) ≤2.0 34 (72.34) 28 (52.83) 10 (35.71) 7 (35.00) 19.879 <0.001>2.0 13 (27.66) 25 (47.17) 18 (64.29) 13 (65.00)纵横比 >1 19 (40.43) 16 (30.19) 2 (7.14) 5 (25.00) 9.766 0.021≤1 28 (59.57) 37 (69.81) 26 (92.86) 15 (75.00)形态 规则 4 (8.51) 4 (7.55) 3 (10.71) 6 (30.00) 7.977 0.046不规则 43 (91.49) 49 (92.45) 25 (89.29) 14 (70.00)边界 清晰 8 (17.02) 10 (18.87) 4 (14.29) 9 (45.00) 8.314 0.040模糊 39 (82.98) 43 (81.13) 24 (85.71) 11 (55.00)边缘毛刺 有 31 (65.96) 26 (49.06) 10 (35.71) 7 (35.00) 8.892 0.031无16 (34.04) 27 (50.94) 18 (64.29) 13 (65.00)微钙化 有 9 (19.15) 10 (18.87) 12 (42.86) 3 (15.00) 7.868 0.049无38 (80.85) 43 (81.13) 16 (57.14) 17 (85.00)后方回声减弱 有 23 (48.94) 23 (43.40) 11 (39.29) 4 (20.00) 5.019 0.170无24 (51.06) 30 (56.60) 17 (60.71) 16 (80.00)血流分级 0-Ⅰ 42 (89.36) 41 (77.36) 19 (63.33) 17 (85.00) 8.085 0.044Ⅱ-Ⅲ 5 (10.64) 12 (22.64) 11 (36.67) 5 (15.00)内部回声 均匀 20 (42.55) 18 (33.96) 11 (39.29) 9 (45.00) 1.114 0.774不均匀 27 (57.45) 35 (66.04) 17 (60.71) 11 (55.00)淋巴转移 有 6 (12.77) 8 (15.09) 4 (14.29) 8 (40.00) 7.917 0.048无41 (87.23) 45 (84.91) 22 (78.57) 12 (60.00)
2.3 不同免疫组化分型乳腺癌剪切波速度值比较
比较不同免疫组化分型乳腺癌的剪切波速度值结果显示,管腔上皮A型组的剪切波速度值最低 (5.43~7.10 m/s),而HerbB-2过表达型组剪切波速度值(8.24~8.59 m/s)高于管腔上皮A型(5.43~7.10 m/s)、管腔上皮B型(7.00~8.32 m/s)及三阴型(7.01~8.39 m/s),而三阴型与管腔上皮B型剪切波速度值相比差异无统计学意义。见表2及图4~5。
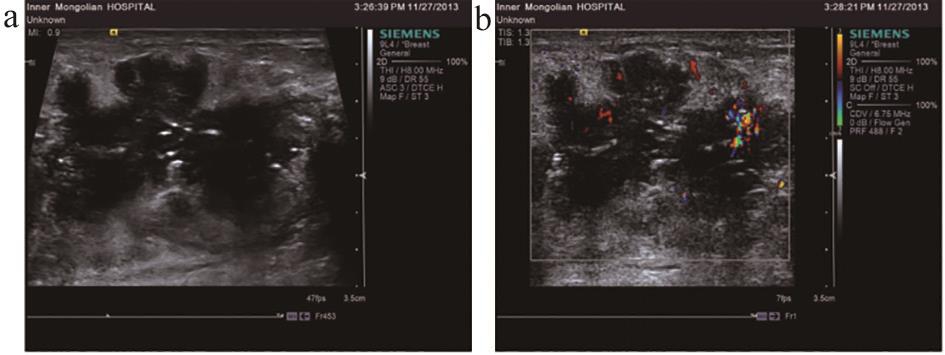
图3 HerbB-2过表达型常规声像图
注:a.二维声像图;b.彩色多普勒声像图。
表2 不同免疫组化分型的剪切波值(m/s)
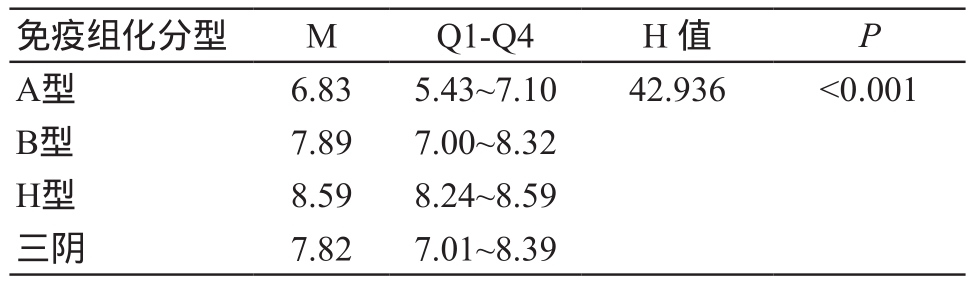
免疫组化分型 M Q1-Q4 H 值 P A型 6.83 5.43~7.10 42.936 <0.001 B型 7.89 7.00~8.32 H型 8.59 8.24~8.59三阴 7.82 7.01~8.39
3 讨论
乳腺癌免疫组化分型的差异决定治疗方案的选择及术后5年生存率高低的判断。管腔上皮型分化程度高、恶性程度低、内分泌治疗效果好,预后好(A型较B型好),化疗反应差(B型比A型好);HerbB-2过表达型肿瘤分化差、预后差,对生物靶向治疗即应用曲妥珠单抗体治疗(赫赛汀)较为敏感,对新辅助化疗反应好;基底样型分化程度低、恶性程度高、淋巴结转移率高,预后差,内分泌及靶向治疗效果较差,新辅助化疗反应好[6]。每一型乳腺癌对新辅助化疗的敏感程度不同,疗效也不同。故一种简便、无创、可重复检查方法的应用对于预估乳腺癌新辅助化疗的疗效及指导穿刺活检、制订下一步治疗方案及判断预后起关键作用。
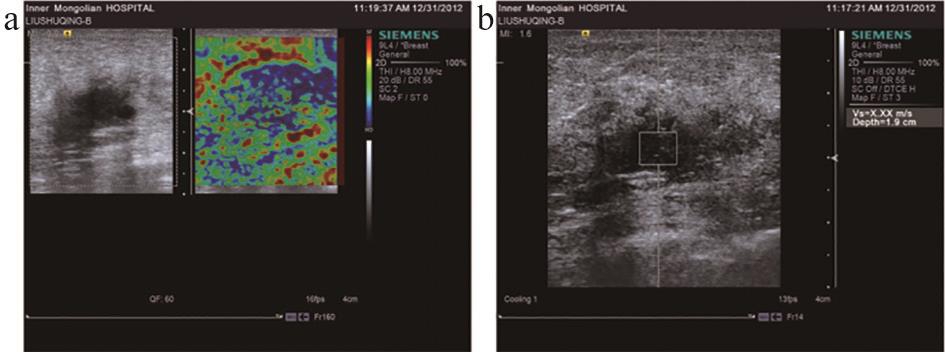
图4 HerbB-2过表达型乳腺癌声辐射力脉冲剪切波弹性成像图
注:a.弹性成像图;b.ARFI值。
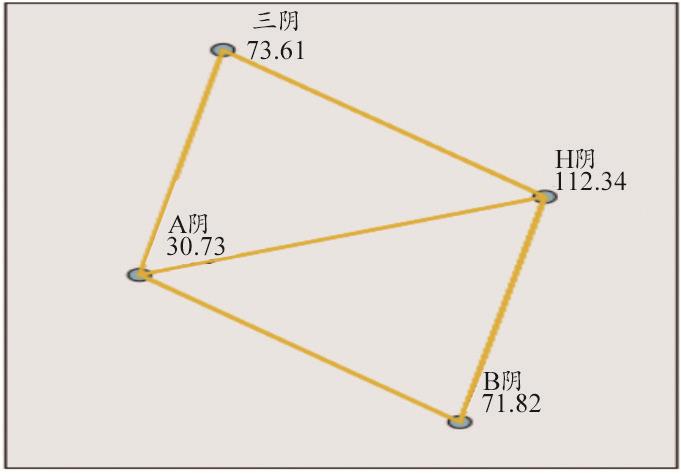
图5 四组不同免疫组化分型乳腺癌ARFI剪切波速度值之间的两两比较示意图
超声检查是乳腺疾病检查的首选方法。乳腺癌的高度异质性决定超声声像图表现的差异。以往的研究大多将超声特征与某些生物学标志物,如ER、PR、HER2等相关[7-11],缺乏全面的分析。本研究是为了全面分析乳腺癌声像图和免疫组化分型之间的关系。研究结果显示三阴型乳腺癌多表现为肿块>2.0 cm、形态规则、边界清晰,这是由于三阴型乳腺癌异型性较高,细胞分裂活跃,病灶在短时间内生长较快造成超声图像呈现膨胀性表现,故具有肿块较大、形态规则、边界清晰、内部乏血供等更倾向于良性肿块的超声表现,与临床预后差的特点相反。但其淋巴结转移率较高,还是与其分化程度差、恶性程度高有关[12]。管腔上皮A型多表现为边缘有毛刺、纵横比大于1,其病理基础可能是由于乳腺肿瘤细胞的生长速度不一致,向周围组织浸润,肿瘤周围单纯的导管和纤维结缔组织增生,伴有不同程度的间质反应,由于肿瘤组织周边间质组织反应性增生,限制或减缓癌细胞向周围正常组织扩散,形成一种保护机制,提示肿瘤的侵袭性更低。管腔上皮A型乳腺癌大多数分化较高,对内分泌治疗敏感,效果较好,此型边缘毛刺征、纵横比大于1的阳性率更高,说明肿瘤细胞的生长仍受激素调控,故边缘毛刺征阳性、纵横比大于1的病例更适合内分泌治疗,预后较好。微钙化及血流分级II-III级在HerbB-2过表达型中多见,此型患者HerbB-2基因扩增,与肿瘤发展进程呈正相关。根据Yang等[13]的研究结果,HerbB-2过表达型乳腺癌多伴有导管原位癌,细胞溶解、碱性磷酸酶增多和钙盐沉着,这与钙化的形成有关。HerbB-2过表达状态与血管生成密切相关,这可能与血管内皮生长因子表达增加有关[14],血管内皮生长因子刺激形成新生血管,这些新生血管往往走行迂曲,粗细不一,形态不规则,缺乏平滑肌,部分形成动静脉瘘,故HerbB-2过表达型乳腺癌在彩色多普勒超声上多表现为血供丰富,Adler血流分级II-III级。HerbB-2过表达是预后不良的因素[15],此型患者对靶向药物敏感,因此,乳腺癌超声图像出现微钙化及血流分级II-III级可能与不良预后有关,更适合靶向药物治疗。
ARFI技术是一种新兴的弹性成像技术,具有非依赖性、可重复性好的优点,正广泛应用于临床研究,它通过获取感兴趣区域中的剪切波速度值的大小来反应组织的软硬程度,即剪切波传播速度值越大,表明组织越硬,反之亦然。管腔上皮A型ER/PR呈强阳性,HER-2呈阴性、增殖指数低,肿瘤的增殖、浸润和转移能力减弱,病灶硬度相比其阴性时软,故SWV值小于其他三型。管腔上皮B型中Ki-67高表达,Ki-67蛋白是一种与增殖相关的非组蛋白核蛋白,它可以直接反映增殖细胞的数量[16],Ki-67的高表达表明肿瘤细胞具有较强的增殖浸润能力,乳腺癌病变的硬度增加,因此,管腔上皮B型SWV值高于A型。HER2蛋白可以促进DNA合成的增加,增加蛋白水解酶的分泌,加速癌细胞的生长和运动能力,肿瘤内结构和肿瘤间质的胶原纤维组成增加、无序排列,使肿瘤的侵袭与转移能力增强,恶性度增大,此外,肿瘤中的胶原蛋白含量和成纤维细胞间质与肿瘤细胞的比例更高[17],故HerbB-2过表达型硬度更高。三阴性型乳腺癌组织学分级增加,癌细胞有丝分裂期活跃、组织分化程度较低[18],然而,三阴性型乳腺癌的SWV值低于HerbB-2过表达型,可能是由于血液供应不足、肿瘤的快速生长导致小区域液化和坏死以致病灶局部硬度降低, 并且由于病变中癌细胞的增殖速率不一致,肿物内部硬度非完全均匀一致而降低了肿块总体的SWV。本研究结果显示,将常规超声及ARFI技术相结合,若乳腺肿块表现为微钙化、血流分级II-III级且SWV越高,提示HerbB-2过表达型的可能性越大,更适合靶向药物治疗;若乳腺肿块表现为边缘毛刺、纵横比大于1且SWV越低,则提示管腔上皮A型的可能性越大,更适合内分泌治疗。另外,SWV可对肿瘤内部成分的软硬度直接量化并客观显示,可为术前穿刺活检提供恰当的穿刺位置,避开有可能存在液化、坏死的位置,从而取得更多的癌组织,达到更精准的穿刺效果,帮助医生更好地了解组织病理学特征。
本研究存在一定的局限性:第一,对于不同免疫组化分型乳腺癌的研究,样本量相对较小;第二,目前剪切波弹性成像检查方法尚未有统一的标准,ARFI剪切波速度值设定范围 0~9 m/s,高于 9 m/s只能按 9 m/s定量 ;第三,乳腺癌剪切波速度值与病理切片难以完全对应;第四,本研究没有发现管腔上皮B型乳腺癌与其他型的显著差异。
综上所述,将常规超声、ARFI技术与免疫组织化学相结合,可初步预估乳腺癌的生物学行为,可为临床提供一种无创、重复性好的新辅助化疗的疗效评估办法及指导乳腺病灶穿刺活检,从而提高了超声检查在乳腺癌诊治中的应用价值。但是,乳腺癌的发生、发展是多因素作用的结果,形态学表现和分子生物学特性之间的关系存在很多影响因素,本研究仅做了初步的分析,还有待于深入的研究。
4 结论
不同免疫组化分型乳腺癌常规超声征象及ARFI技术剪切波速度值有差异,常规超声结合ARFI技术可初步预估乳腺癌的生物学行为,为新辅助化疗疗效的评估及指导穿刺活检提供帮助。
[1]Siegel RL,Miller KD,Jemal A.Cancer statistics,2018[J].CACancer J Clin,2018,60(5):277-300.
[2]Turkoz FP,Solak M,Petekkaya I,et al.Association between common risk factors and molecular subtypes in breast cancer patients[J].Breast,2013,22(3):344-350.
[3]吴绍勇,谭月,官泳松.不同分子亚型乳腺癌首发肝转移患者的临床特征和预后[J].中华肝脏病杂志,2016,24(6):422-428.
[4]赵鹤楠,李紫瑶,俞卫东,等.剪切波弹性成像及超微血管显像在乳腺浸润性导管癌病理分级中的应用研究[J].中华超声影像学杂志,2017,26(2):146.
[5]Curigliano G,Burstein HJ,Winer EP,et al.De-escalating and escalating treatments for early-stage breast cancer: the St.Gallen International Expert Consensus Conference on the Primary Therapy of Early Breast Cancer 2017[J].Ann Oncol,2017,28(8):1700.
[6]Zhang L,Li J,Xiao Y,et al.Identifying ultrasound and clinical features of breast cancer molecular subtypes by ensemble decision[J].Sci Rep,2015,5:11085.
[7]樊智颖,王学梅,康姝,等.乳腺浸润癌剪切波弹性成像与临床病理、免疫组化特征相关性分析[J].中国医科大学学报,2014,43(4):344-350.
[8]刘军杰,陈圆圆,李智贤,等.乳腺浸润性导管癌超声BI-RADS分类与雌、孕激素受体及CerbB-2表达的相关性[J].中国医学影像学杂志,2014,22(4):244-248.
[9]李宏,李德华,胡波.乳腺癌超声征象与Ki67、p53表达的相关性及临床意义[J].中国临床医学影像杂志,2015,26(5):321-324.
[10]刘海芳,高杨,姜楠,等.乳腺癌超声表现与生物学指标的相关性及对临床治疗的指导意义[J].中国医药,2015,10(1):1-4.
[11]Elebi F,Pilanc KN,Ordu E,et al.The role of ultrasonographic findings to predict molecular subtype,histologic grade,and hormone receptor status of breast cancer[J].Diagn Interv Radiol,2015,21(6):448-453.
[12]时兆婷,乐坚,陈雅玲,等.浸润性乳腺癌超声征象与腋下淋巴结转移的相关性研究[J].中华超声影像学杂志,2017,26(5):424.
[13]Yang WT,Dryden M,Broglio K,et al.Mammographic features of triple receptor-negative primary breast cancers in young premenopausal women[J].Breast Cancer Res Treat,2008,111(3):405-410.
[14]Zhu X,Ying J,Wang F,et al.Estrogen receptor,progesterone receptor, and human epidermal growth factor receptor 2 status in invasive breast cancer: a 3,198 cases study at National Cancer Center, China[J].Breast Cancer Res Treat,2014,147(3):551-555.
[15]Zeng L,Yang K.Exploring the pharmacological mechanism of yanghe decoction on HER2-positive breast cancer by a network pharmacology approach[J].J Ethnopharmacol,2017,199(5):68.
[16]Xu J,Guo X,Jing M,et al.Prediction of tumor mutation burden in breast cancer based on the expression of ER,PR,HER-2,and Ki-67[J].Onco Ther,2018,11:2269-2275.
[17]杨雅洁,孙艳花.乳腺癌组织中HER2的表达及其与临床病理特征的关系[J].南昌大学学报:医学版,2018,58(1):55-59.
[18]Dent R,Trudeau M,Pritchard KI,et al.Triple-negative breast cancer: clinical features and patterns of recurrence[J].Clin Cancer Res,2018,13(15 Pt 1):4429-4434.
Application of Conventional Ultrasound and Acoustic Radiation Force Pulse Imaging in Immunohistochemical Classification of Breast Cancer