一种小型化低成本免疫荧光分析仪的设计
引言
免疫荧光技术又称荧光抗体(抗原)技术,它是利用抗原、抗体特异性结合的特点,可以准确快速地检测待测物(抗原)的含量[1]。免疫荧光技术的原理是在硝酸纤维素膜的测试区(T)包被BSA与抗原的偶联物,标记垫上含有预先包被的荧光标记抗体。检测时,首先用处理试剂将样本中的抗原与标记垫上的荧光标记抗体发生结合,形成免疫复合物,复合物在层析作用下沿着硝酸纤维素膜向前扩散至包被有另一种单克隆抗体的检测区,从而形成双抗体夹心复合物,而游离的荧光抗体则附着在质控区[2]。当检测卡插入干式荧光免疫分析仪后,分析仪自动扫描检测区和质控区的荧光强度,通过两种荧光强度的比值计算待测样本中的抗原含量。免疫荧光分析技术具有灵敏度高、特异性强等特点,在床旁即时检测(Point-of-Care Testing,POCT)领域上应用广泛,比如定量检测血清、血浆、全血样本中C-反应蛋白、糖化血红蛋白、甲胎蛋白、降钙素原等物质的含量。免疫荧光耗材保存要求低、操作简便,适合中小医疗单位推广使用[3-4]。
光学模块是免疫荧光分析仪的核心模块。当前免疫荧光光学模块,大多包括激光光源、二向分色片、透镜、滤光片、光电转换器件等[5]。光学器件较多,成本高,安装与维护复杂,对使用环境有一定的要求。另外,大多光学模块采用“电机-皮带”或者“电机-齿轮”的动力与传动机构[6]。多个运动机构的组合,不仅增加了设备的体积与重量,机构间的间隙还容易带来误差。复杂的光路、运动机构设计使设备在野战、救灾、移动医疗等领域作用受限[7]。因此,需要提出一种新的设计方式,简化光路与运动部件,同时具有测试卡插入检测功能、废片自动抛弃功能,且性能参数达到行业标准。
1 硬件部分
硬件部分采用上下位机的结构。上位机负责GUI显示、IC模块通讯以及连接打印机;下位机主要完成测试功能,可连接多个通道,包括控制各个通道的光源恒流电路、电机控制以及光强检测。整机结构框架如图1所示。
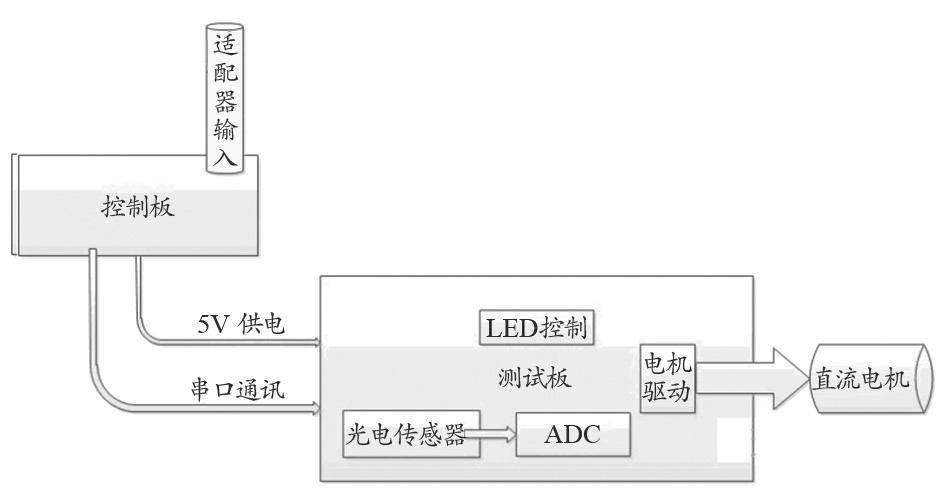
图1 整机结构框图
(1)上位机,即控制板,采用工控板为平台。操作系统、应用软件以及数据库运行在该平台上。应用软件用于与客户交互,接收操作指令,分解测试步骤,并将测试步骤通过串口下发到下位机;获取下位机返回的测试数据后,应用软件计算出检测结果;可以通过打印机打印,也可以存储在本地数据库,或者通过网口上传到LIST系统。
(2)下位机,即测试板,使用80C51作为MCU,通过RS232与上位机通讯。下位机检测到微动开关信号后,发送命令通知上位机启动检测程序;获得上位机的检测参数后,下位机通过调整数字变阻器来调整光源亮度,通过电机控制与AD采样时序的配合,实现整个测试卡的扫描,并将扫描结果返回上位机处理;下位机还具有开机复位、废片抛样以及光路异常报警功能。
2 光学部分
光学设计上使用非共聚焦光路方式[8],如图2所示。LED光源与试纸条成45°夹角放置,相互对称,使照射到试纸条上的激发光尽量均匀。光电二极管位于试纸条正上方,检测试纸条上被激发的荧光[9]。LED光源的出射方向上装有激发波长滤光片以滤除干扰杂散光,光电二极管前方装有发射波长滤光片,让需要的荧光信号完全通过,同时最大程度地阻止激发光和各种杂散光进入检测系统[10]。这种光路结构的优点是结构简单、成本低,光学器件都固定在硬件上,间隙小,抗震抗摔能力强[11]。
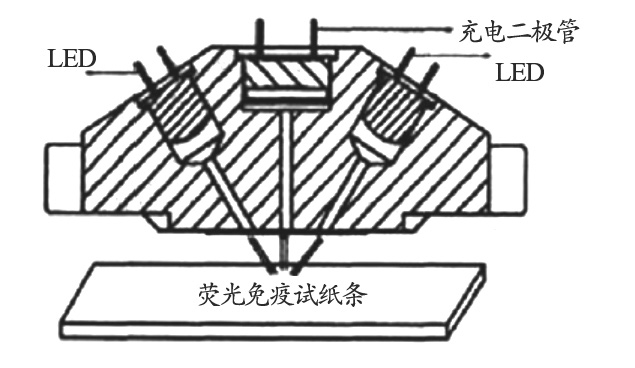
图2 非共聚焦光路
在光源选择上,采用直径为5.5 mm的圆子弹头LED冷光源。滤光片方面,根据荧光波长,选用中心波长在620 nm、带宽在10 nm的带通滤光片。采用硅光二级光作为光电传感器,传感器在620 nm上有一定的感光灵敏度[12]。光学模块3D效果图如图3所示。
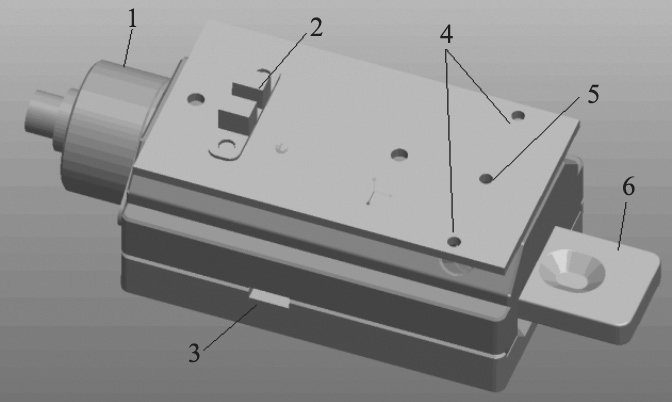
图3 光学模块3D效果图
注:1.推杆电机;2.复位光耦;3.微动开关;4.光源;5.光电二极管;6.测试卡。
传统的光学检测法常用激光作为激发光源[13]。激光光源优点是波长精度高、杂波少、信号强,在第值区间分辨率高;同时缺点也明显,例如热漂移明显,发光效率随着使用时间变长而变弱,需要反馈-补偿电路来确保光强一致,并且聚焦距离大,体积大[14]。目前,越来越多荧光分析仪采用LED作为光源。本设计采用高亮度LED灯,配合前端的带通滤光片得到单色激发光,在运动方面采用直接推杆电机,克服传统的“电机+皮带”的运动结果,有效降低机械运动带来的测试误差,因此能有效保证测试的精密度与准确性[15]。
3 算法部分
以C反应蛋白项目为例,先对8组定标品测试,获得对应的测试值,然后采用拟合方程[16]。具体的方法步骤如下。
(1)使用可溯源定标品,浓度为200 mg/L,标定为#1号定标液。使用芬兰QuikRead产品测试定标液五次,取平均值202.3 mg/L作为参考值。
(2)取#1号定标液100 μL,加入100 μL稀释液稀释,定义为#2号定标液。使用芬兰QuikRead产品测试定标液五次,取平均值98.4 mg/L作为参考值。
(3)取#2号定标液100 μL,加入100μL稀释液稀释,定义为#3号定标液。使用芬兰QuikRead产品测试定标液五次,取平均值49.5 mg/L作为参考值。
(4)取#3号定标液100 μL,加入100μL稀释液稀释,定义为#4号定标液。使用芬兰QuikRead产品测试定标液五次,取平均值23.8 mg/L作为参考值。
(5)取#4号定标液100 μL,加入100 μL稀释液稀释,定义为#5号定标液。使用芬兰QuikRead产品测试定标液五次,取平均值12.2 mg/L作为参考值。
(6)取#5号定标液100 μL,加入100 μL稀释液稀释,定义为#6号定标液。使用芬兰QuikRead产品测试定标液五次,取平均值5.9 mg/L作为参考值。
(7)取#6号定标液100 μL,加入100μL稀释液稀释,定义为#7号定标液。使用芬兰QuikRead产品测试定标液五次,取平均值2.5 mg/L作为参考值。
(8)取#7号定标液100 μL,加入100 μL稀释液稀释,定义为#8号定标液。使用芬兰QuikRead产品测试定标液五次,取平均值1.1 mg/L作为参考值。
各定标品浓度与散射值列表,见表1。通过测试,获取标准液的测试结果,并在二维坐标上描点(图4)。
表1 定标品浓度与散射值列表
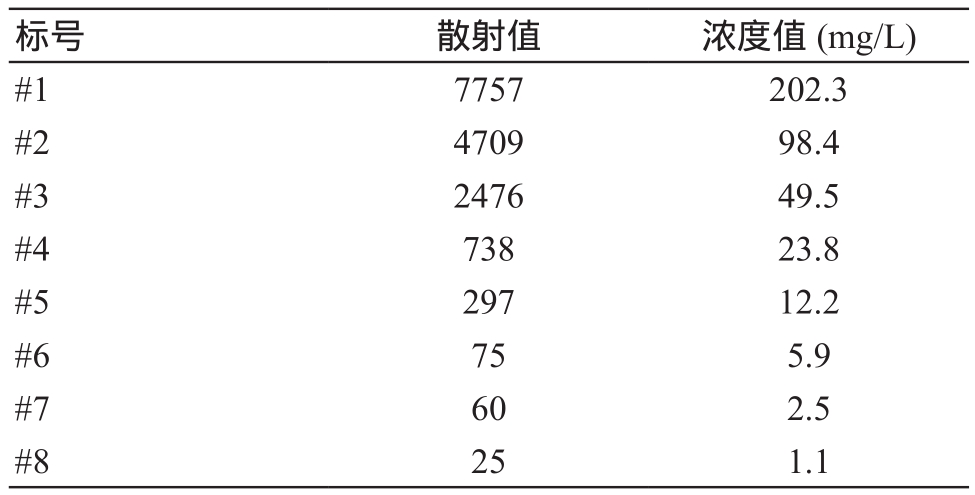
标号 散射值 浓度值 (mg/L)#1 77 57 202.3#2 4709 98.4#3 2476 49.5#4 738 23.8#5 297 12.2#6 75 5.9#7 60 2.5#8 25 1.1
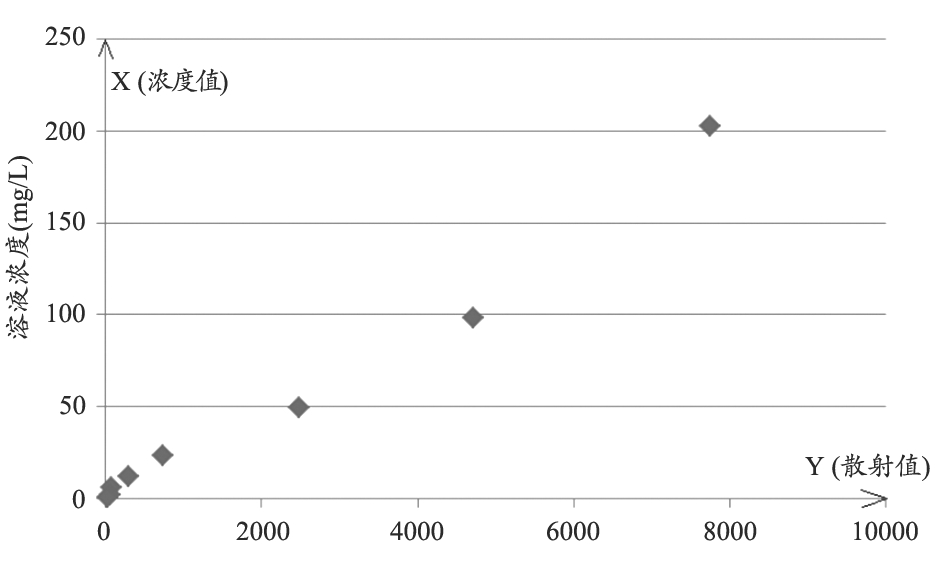
图4 标准品溶液浓度与散射值关系
如果试剂测试标准物所得的浓度与散射值之间呈现某种线性关系,可以使用一元线性回归模型来估算样本的定量结果。对于所测得的原始数据,建立一元一次线性回归模型。
其中,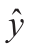 为浓度,x为散射值,a,b为系数。
为浓度,x为散射值,a,b为系数。
设在一次试验中,取得n对数据(xi,yi)(i=1,2,…n),这n对数据(xi,yi)就是一组样本值,根据这一组样本值可以寻求一对系数a和b。但由于y是一个随机变量,所以如果通过另一组试验又可得到一对a和b的值[6],也就是说,可以通过一组数据所得到的是系数a和b的估计值,记作![]() 通过一组试验数据所求出的回归方程如式 (2)。
通过一组试验数据所求出的回归方程如式 (2)。
对于每次试验取得n对数据(xi,yi),记yi是随机变量y对应于xi的试验值,记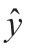 是试验值yi的回归值。每一个试验值yi与回归值
是试验值yi的回归值。每一个试验值yi与回归值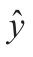 之间的差
之间的差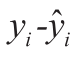 ,可表示为两个纵坐标之差,这个差有正有负,其绝对值为
,可表示为两个纵坐标之差,这个差有正有负,其绝对值为![]() 我们目的是找到一条使所有这些距离之和为最小的一条直线,即
我们目的是找到一条使所有这些距离之和为最小的一条直线,即![]() 最小。但由于绝对值在处理上比较麻烦,所以代之以平方和。
最小。但由于绝对值在处理上比较麻烦,所以代之以平方和。
这个平方和Q是随着回归系数![]() 而变的,因此它是
而变的,因此它是![]() 的一个二元函数,其中xi和yi为常数。根据二元函数求极值的方法,求分别对 a 和 b 求偏导数得到式 (4)。
的一个二元函数,其中xi和yi为常数。根据二元函数求极值的方法,求分别对 a 和 b 求偏导数得到式 (4)。

解出回归系数![]() 为
为

上式或写成
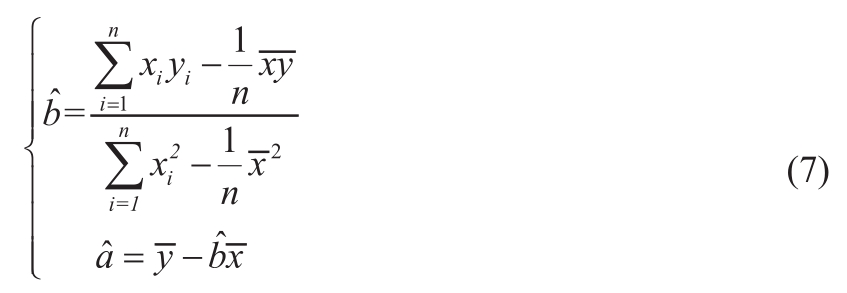
式中的![]() 即为Q的最小值点,使得
即为Q的最小值点,使得![]() 达到最小。以
达到最小。以![]() 为回归系数的直线方程,就是所要求的回归方程。
为回归系数的直线方程,就是所要求的回归方程。
如果散点图上看,接近是二次曲线,则使用一元二次回归,具体算法是将一元二次回归转化为二元一次回归。
设一元二次多项式回归方程为
令![]() 则得二元线性回归方程
则得二元线性回归方程
然后进行二元线性函数的回归分析,得到最后结果。
计算获得标准曲线后,存入到IC卡中,随试剂发送到用户。用户在使用前,先刷IC卡,仪器获得标准曲线,然后将待测样本的测试值,代入标准曲线计算,得到浓度值。
4 性能测试
使用精密度、准确性、线性相关性来对仪器的性能进行评估[17]。
4.1 精密度
精密度以变异系数CV表示。选取C反应蛋白项目作为测试项目,随机抽取免疫荧光分析仪一台,使用浓度为10 mg/L的可溯源质控品按正常测试条件共测试10次[18]。按式(10)计算10次结果的变异系数CV。
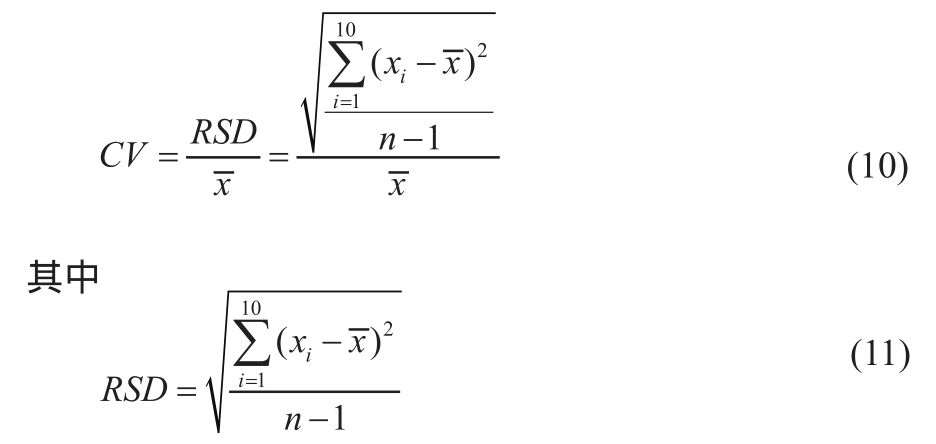
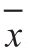 为10次测量结果的算术平均值;xi为每次实测结果;n为实测的次数,本文中n=10。
为10次测量结果的算术平均值;xi为每次实测结果;n为实测的次数,本文中n=10。
精密度测试结果,见表2。计算得到仪器精密度为CV=3.9837%,满足CV不大于5%的要求。
表2 精密度测试结果

结果 测试次数T1 T2 T3 T4 T5 T6 T7 T8 T9 T10散射值 609 552 561 571 569 522 586 596 523 562浓度值(mg/L) 11.9211.0211.1611.3211.2910.5511.5611.7210.5611.18
4.2 准确性
选取C反应蛋白项目作为测试项目,随机抽取免疫荧光分析仪一台,分别使用浓度为20、70 mg/L的可溯源质控品按正常测试条件共测试5次。按式(12)计算低值样本、中值样本的准确性。
式中,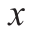 为5次连续测定值的均值;T为参考物质的标称参考值。
为5次连续测定值的均值;T为参考物质的标称参考值。
准确性测试结果数据,见表3。
表3 准确性测试结果
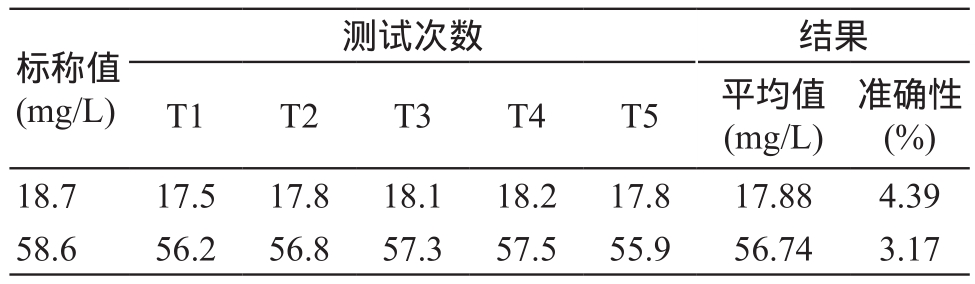
准确性(%)18.7 17.5 17.8 18.1 18.2 17.8 17.88 4.39 58.6 56.2 56.8 57.3 57.5 55.9 56.74 3.17标称值(mg/L)测试次数 结果T1 T2 T3 T4 T5 平均值(mg/L)
4.3 线性相关性测试
选取C反应蛋白项目作为测试项目,随机抽取免疫荧光分析仪一台,分别使用浓度为200、103、49.6、25.6、14.4、6.7、3.1 mg/L几种浓度梯度血清样本检测,其中样本浓度经过迈瑞BS-380测试确认靶值。按照式(13)计算各梯度浓度值与标称浓度值的线性系数。
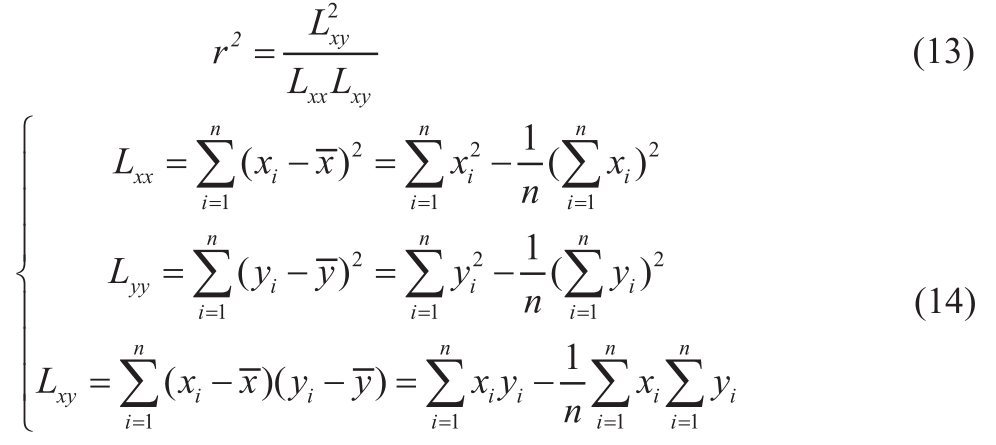
其中![]() 为测量结果的算术平均值;x1为每次实测结果;n为实测的次数。
为测量结果的算术平均值;x1为每次实测结果;n为实测的次数。
线性相关性测试数据,见表4。标称值与实测值在测试范围内两者的相关系数大于0.99(图5)。
表4 线性系数测试结果
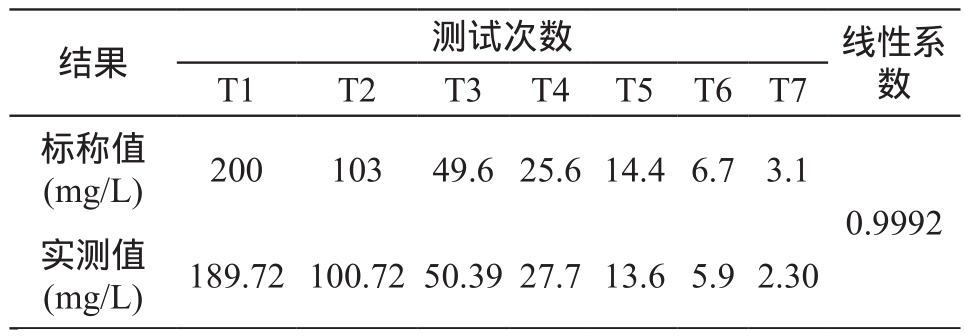
结果 测试次数 线性系数T1 T2 T3 T4 T5 T6 T7标称值(mg/L) 200 103 49.625.614.46.7 3.1 0.9992实测值(mg/L) 189.72100.7250.3927.713.65.92.30
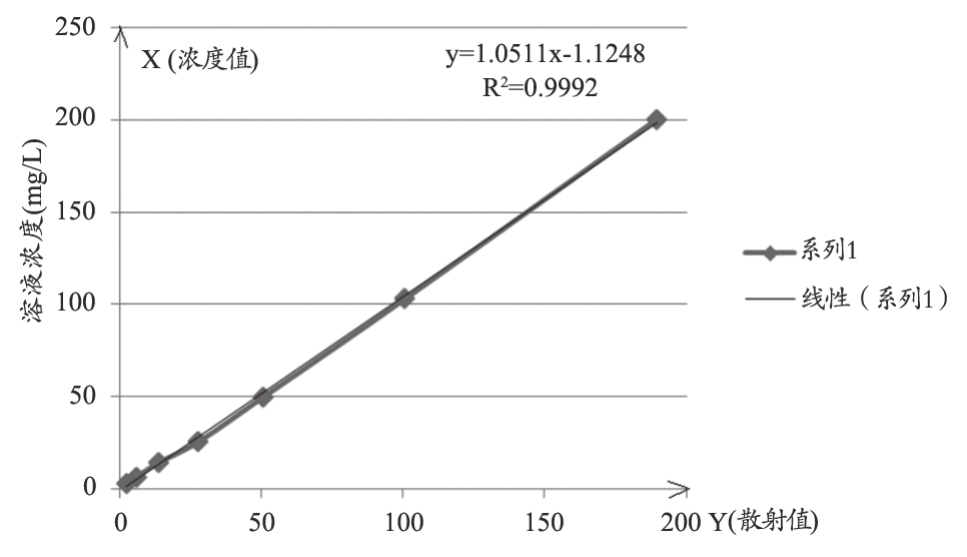
图5 线性相关性结果
5 总结
一台专业的免疫荧光分析仪具有检测线性范围宽、重复性好、灵敏度高、检测速度快的优点,本文所描述的一种低成本免疫荧光分析仪的设计方案,具有良好的抗震性能,成本低,体积小,结构简单。经过测试,仪器的精密度、准确性、线性范围等主要指标均达到行业平均水平。随着免疫荧光技术的不断成熟,除了在医疗领域广泛应用外,还在动植物检疫、食品安全、农药残留检测方面得到了扩展,市场也越来越大,其前景越来越好。
[1]潘星,郑忠亮,吴琼水.免疫荧光定量分析仪设计[J].电子技术应用,2014,11(40):19-22.
[2]黄晓群.酶联免疫法、金标法、时间分辨免疫荧光分析法测定HBsAg对比分析[J].中国保健营养:临床医学学刊,2009,18(5):7-9.
[3]汪宏良,陈丽峰,胡芳.生物化学分析仪检测结果的临床评价[J].检验医学与临床,2007,4(6):558-559.
[4]龙宪和.对IMMULITEⅠ型化学发光酶免疫技术中检测原理及相关内容的初评[J].标记免疫分析与临床,2005,12(1):50-52.
[5]张超,刘艳珍.免疫荧光层析定量检测系统的改进研究[J].中国医药科学,2014,(23):157-161.
[6]钱英超,陈丽华.免疫荧光干式定量法检测全血CRP的临床应用评估[J].中国实用医药,2014,(32):76-77.
[7]刘云峰,邓清华,杜利容,等.时间分辨免疫荧光分析法影响因素初探[J].泸州医学院学报,2007,30(2):124-126.
[8]杭建峰,吴英松,徐伟文,等.总PSA时间分辨免疫荧光分析法的建立[J].现代免疫学,2005,25(5):402-405.
[9]黄华伟,杜美菊.免疫荧光分析的研究进展[J].应用化工,2007,36(4):394-397.
[10]刘威龙,孙明磊,王頔,等.基于STM32的分布式步进电机控制系统设计[J].数字技术与应用,2012,(3):12-14.
[11]吴刚,姜瞻梅,霍贵成,等.胶体金免疫层析技术在食品检测中的应用[J].食品工业科技,2007,(12):216-218.
[12]梁晓威,程威,孙云,等.全自动免疫荧光分析仪检测苯丙氨酸的性能验证[J].南京医科大学学报(自然科学版),2018,38(5):134-137.
[13]段秀群,田欢,龚国富.两种仪器测定血清C反应蛋白的性能比对分析[J].中国医疗设备,2017,32(2):87-90.
[14]杨泽权.降钙素原乳胶增强免疫比浊法与免疫荧光法的相关性[J].国际检验医学杂志,2016,(3):416-417.
[15]蒋玲丽,唐大海,张健,等.5种C反应蛋白快速检测系统检测性能比较[J].检验医学,2016,31(4):293-298.
[16]汪怀周,陈燕,岳展伊,等.C反应蛋白测定两种检测系统间结果的比较[J].现代检验医学杂志,2016,31(3):127-130.
[17]卢锦沛.不同检测系统C反应蛋白测定结果可比性研究[J].国际检验医学杂志,2016,37(8):1110-1111.
[18]胡静,李立新,罗俐梅,等.全自动间接免疫荧光法分析仪检测抗核抗体与人工判读的对比研究[J].华西医学,2016,31(6):1084-1087.
Design of a Miniaturized and Low-Cost Immunofluorescence Analyzer