手术室医疗器械不良事件的分析思考
引言
医疗器械不良事件是指获准上市的、合格的医疗器械在正常使用情况下,发生的或可能发生的任何与医疗器械预期使用效果无关的有害事件[1-2]。我国现行的医疗器械不良事件报告原则是“可疑即报”原则。自2018年8月1日起开始实施的新修订的《医疗器械分类目录》[3]按照技术专业和临床使用特点将医疗器械分为了22个子目录,子目录由一级产品类别、产品描述、预期用途、品名举例和管理类别组成。本文按照新《医疗器械分类目录》将本院手术室年度医疗器械不良事件数据进行统计,并结合医院提取的几例不良事件实例,对手术室动力系统和医用内窥镜系统的风险控制进行对策的讨论和思考。
1 医院手术室2018年度设备不良事件报表统计
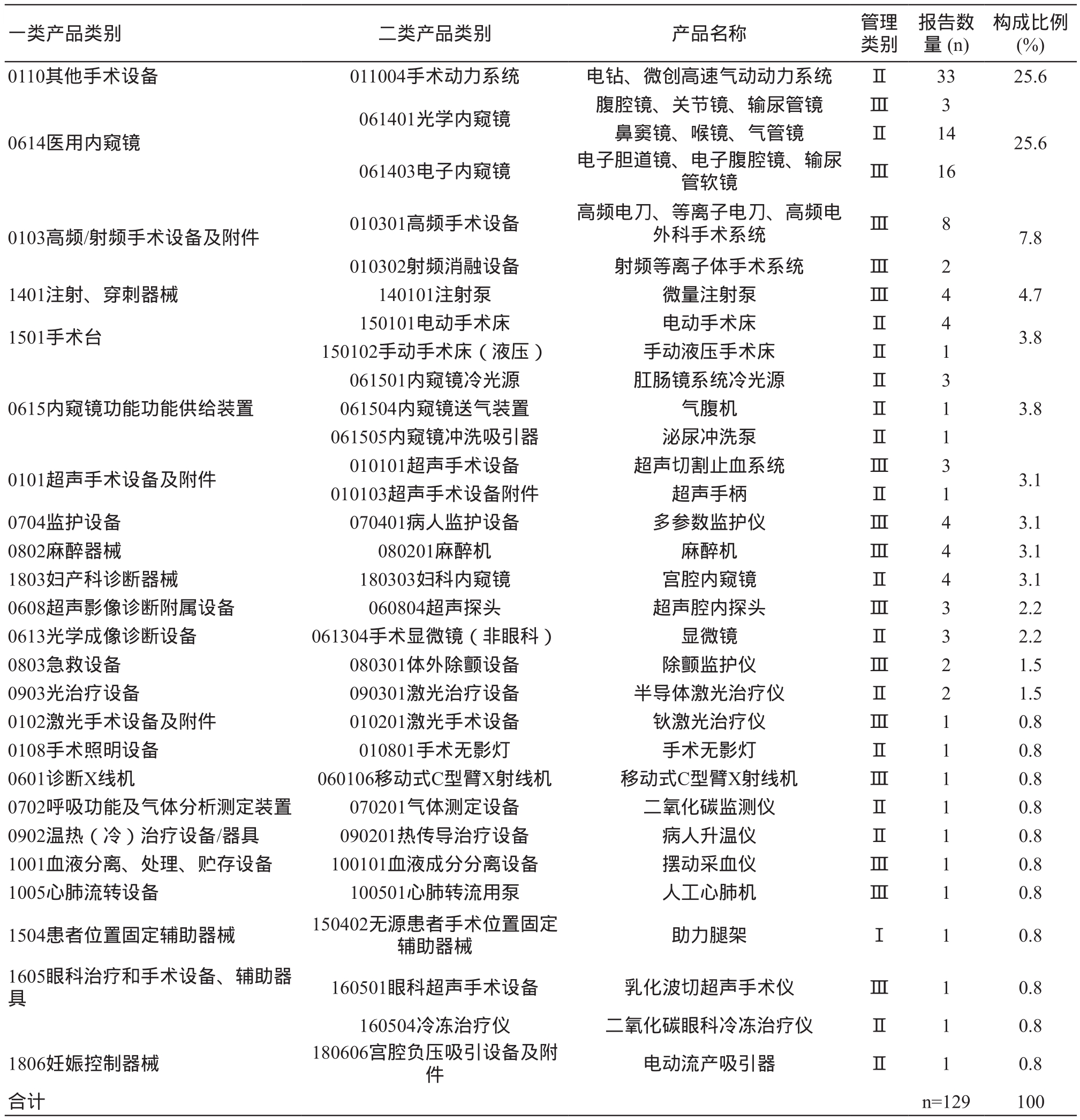
2018年本院驻手术室工程师共上报不良事件129例:① 从医疗器械一类产品类别分类来看共涉及24个种类中的41种产品;② 上报数量前三的医疗器械分别是手术动力系统,医用内窥镜,高频/射频手术设备;③ 根据使用安全性来看,Ⅲ类医疗器械56例,占上报总数的43.4%,Ⅱ类医疗器械72例,占上报总数的55.8%,I类医疗器械1例,占上报总数的0.8%。其中Ⅲ类医疗器械不良事件的主体是医用内窥镜、高频电刀分别占Ⅲ类医疗器械不良事件总数的33.9%、17.9%。而Ⅱ类医疗器械中不良事件的主体是手术动力系统及医用内窥镜分别占据Ⅱ类医疗器械不良事件总数的45.8%、19.4%。具体数据分析,见表1。
根据上述数据分析,能够突出地反映出手术室医疗器械不良事件的现状;动力系统、医用内窥镜这些精密性高、部件连接复杂、单位价值较大、使用频率高,需要反复消毒灭菌的医疗器械发生不良事件的概率较高[4]。
2 动力系统和医用内窥镜不良事件实例分析和现状讨论
2.1 实例一
事件过程:2018年2月患者在全麻下行脑外伤手术,术前检查动力系统功能正常,术中铣刀手柄发烫,并发现铣刀手柄轴承异位。
事件分析:为了方便临床使用,该型号铣刀手柄设计的轻巧、易于把握;从而其内部轴承、驱动马达等配件精密小巧;而颅骨过硬过厚,高速转动下小轴承受力过大,因此该型号产品极易发生手柄发热、轴承损坏和异位,怀疑手柄设计和轴承材质存在一定缺陷。同时,精小的设计对术中、术后的清洁和保养提出了更高的要求。
表1 发生医疗器械不良事件的产品类别和比例(n=129)
一类产品类别 二类产品类别 产品名称 管理类别报告数量 (n)构成比例(%)0110其他手术设备 011004手术动力系统 电钻、微创高速气动动力系统 Ⅱ 33 25.6 061401光学内窥镜 腹腔镜、关节镜、输尿管镜 Ⅲ 3 0614医用内窥镜 鼻窦镜、喉镜、气管镜 Ⅱ 14 061403电子内窥镜 电子胆道镜、电子腹腔镜、输尿管软镜 Ⅲ 16 25.6 0103高频/射频手术设备及附件010301高频手术设备高频电刀、等离子电刀、高频电外科手术系统Ⅲ87.8 010302射频消融设备 射频等离子体手术系统 Ⅲ 2 1401注射、穿刺器械 140101注射泵 微量注射泵 Ⅲ 4 4.7 1501手术台 150101电动手术床 电动手术床 Ⅱ 4 3.8 150102手动手术床(液压) 手动液压手术床 Ⅱ 1 061501内窥镜冷光源 肛肠镜系统冷光源 Ⅱ 3 0615内窥镜功能功能供给装置061504内窥镜送气装置 气腹机 Ⅱ 1 061505内窥镜冲洗吸引器 泌尿冲洗泵 Ⅱ 1 0101超声手术设备及附件 010101超声手术设备 超声切割止血系统 Ⅲ 3 3.1 010103超声手术设备附件 超声手柄 Ⅱ 1 0704监护设备 070401病人监护设备 多参数监护仪 Ⅲ 4 3.1 0802麻醉器械 080201麻醉机 麻醉机 Ⅲ 4 3.1 1803妇产科诊断器械 180303妇科内窥镜 宫腔内窥镜 Ⅱ 4 3.1 0608超声影像诊断附属设备 060804超声探头 超声腔内探头 Ⅲ 3 2.2 0613光学成像诊断设备 061304手术显微镜(非眼科) 显微镜 Ⅱ 3 2.2 0803急救设备 080301体外除颤设备 除颤监护仪 Ⅲ 2 1.5 0903光治疗设备 090301激光治疗设备 半导体激光治疗仪 Ⅱ 2 1.5 0102激光手术设备及附件 010201激光手术设备 钬激光治疗仪 Ⅲ 1 0.8 0108手术照明设备 010801手术无影灯 手术无影灯 Ⅱ 1 0.8 0601诊断X线机 060106移动式C型臂X射线机 移动式C型臂X射线机 Ⅲ 1 0.8 0702呼吸功能及气体分析测定装置 070201气体测定设备 二氧化碳监测仪 Ⅱ 1 0.8 0902温热(冷)治疗设备/器具 090201热传导治疗设备 病人升温仪 Ⅱ 1 0.8 1001血液分离、处理、贮存设备 100101血液成分分离设备 摆动采血仪 Ⅲ 1 0.8 1005心肺流转设备 100501心肺转流用泵 人工心肺机 Ⅲ 1 0.8 1504患者位置固定辅助器械 150402无源患者手术位置固定辅助器械 助力腿架 Ⅰ 1 0.8 1605眼科治疗和手术设备、辅助器具3.8 160501眼科超声手术设备 乳化波切超声手术仪 Ⅲ 1 0.8 160504冷冻治疗仪 二氧化碳眼科冷冻治疗仪 Ⅱ 1 0.8 1806妊娠控制器械 180606宫腔负压吸引设备及附件电动流产吸引器 Ⅱ 1 0.8合计 n=129 100
事件处理:立即停用该动力系统,联系厂家进行维修。同时向厂家反馈临床使用中存在安全风险,寻求解决方案,经沟通为了不影响临床使用,厂家暂提供备品以备应急。
2.2 实例二
事件过程:2018年2月患者在全麻下行脑瘤切除术,术前动力系统功能检查正常,术中铣刀刀头断裂,并且刀头取不下来。
事件分析:由于铣刀刀头成本较高,大部分医院无法做到一次性使用,厂家建议在外观无明显的变形磨损下,刀头会消毒灭菌继续使用,使用次数可达3~5次。实际应用中刀头使用次数越多磨损越大,术中轴承需要承受的力越大,极易产生刀头断裂、轴承异位、刀头取不下来的现象,造成不良事件的发生。
事件处理:暂停该铣刀手柄的使用,联系厂家维修,同时向厂家和医院反馈该现象。经院内讨论,2018年下半年开始在脑科手术中,使用一次性铣刀刀头产品,以期降低术中风险。实施半年来,铣刀的故障率有所降低。
2.3 实例三
事件过程:2018年3月患者在全麻下行腹腔镜下卵巢癌恶性肿瘤减灭术,术中CO2气腹机温度过高报警,气腹机加热模块发烫。
事件分析:加温二氧化碳气腹可使术野清晰,减少术后低体温及寒战的发生,不加重术后血气及血液流变学的改变[5]。但CO2加热模块在手术时间较长的使用过程中,容易发生温度过高报警。是否是38℃恒温加热,实际过程中未能有明显的温度监测显示,存在温度不可控性和不灵活性,有一定的安全风险。
事件处理:立即暂停该气腹机和加热模块,联系厂家检测,同时向厂家反馈CO2加热手术应用中存在的不灵活和不可控的问题。经检测该气腹机和加热模块未有故障,厂家建议暂停用该加热模块。
2.4 实例四
事件过程:2018年3月工程师上报1例光学腹腔镜不良事件,术中光学硬镜不断起雾,视野模糊,需要不断地用碘伏擦拭清洁镜头,影响大夫操作和手术进程。
事件分析:光学硬镜应用于腹腔手术,不同于电子腹腔镜,镜头前端内部没有加热或发热组件,硬镜本身的温度与患者体温产生差异,造成频繁起雾的情况。但该品牌产品相比较其他品牌的产品起雾情况严重。
事件处理:联系厂家工程师,反馈该型号设备临床使用中存在的问题,寻求解决方案,再未有更好的解决方法之前,厂家建议术前和术中用热水加热一下内窥镜物镜端,术中增加流通,以期降低起雾的频率。
结合不良事件的统计和实例,利用鱼骨图对容易造成医疗器械不良事件的原因进行分类[6-8],见图1。

图1 鱼骨图
由鱼骨图可以看出,动力系统、医用内窥镜引起医疗器械不良事件发生原因多数在于医疗器械本身的固有因素和人的使用维护上[9]。这既是两个独立的因素,又有着连带性。
3 对动力系统、医用内窥镜系统的风险管理进行对策的思考和讨论
将不良事件的监测数据纳入医疗器械临床准入和评价管理的一部分,从而为医院医疗器械采购提供一项重要参考依据[10-11]。
医疗器械不良事件上报监管的意义在于从源头(设计和构造、生产)上保障医疗器械产品的安全性,降低使用风险性,同时提醒医疗机构与用户在使用中引以为戒。对于短期内无法从设计和构造上消除或降低风险的医疗器械,需要在使用和维护保养等环节上实现风险控制管理。
在设备的使用上,手术室护士一定要做好术前的器械清点和功能检查工作,术中实时关注设备的使用情况,发现问题及时解决[12-13]。基于动力系统的特性,术中及时的血液、组织和骨屑的预清理是台上洗手护士规范操作的必要的环节;而对于内窥镜而言,术中临床医生的操作手法起到决定性作用;例如腹腔镜手术时扶镜手握持的位置,有无弯折电缆根部,关节镜手术时刨刀与关节镜的操作距离,钬激光手术时操作不当引起的软镜的漏水、模糊等使用风险。设备科应协同培训部,实行相关人员的精准培训、再培训和考核工作,这是促进使用人高效、全面掌握设备的操作规范,提高使用人责任意识、规范化意识的有效方法。
在医疗器械维护保养方面上,术后规范的清洁、保养,是降低设备故障率、保障设备性能正常的重要因素,尤其对于动力系统和医用内窥镜来说,而这两种医疗器械的清洁和保养主要依赖消毒供应中心完成。如何做好清洗、保养的监管管理工作,是降低该类设备不良事件发生风险的重要措施。设备管理小组联合科室质量控制小组(设备维修人员及科室指定的器械管理人员)切实落实医院《手术部消毒供应室监测制度》[14]定期对各环节进行现场检查和抽查,记录清洁、除锈保养情况,形成设备质量持续改进档案。对于操作不规范的人员进行针对性再培训和考核。结合医院《手术动力系统清洗保养安全管理措施》《内镜器械清洗消毒的安全管理措施》,建议对于清洗、维护保养过程中发现存有安全隐患的设备及时通知设备工程师进行处理。定期联系厂家工程师来院对这两类设备做全面的零配件性能检查工作,并做好设备的预防性维护保养记录。
持续完善手术室各项规章制度、应急预案及工作流程[15]。指定医疗器械不良事件监报员(最好是质量控制小组或设备管理小组成员)进行不良事件的上报整理和分析,建立科室医疗器械不良事件处置流程(图2),定期将上报的手术室医疗器械不良事件总结反馈到科室质量控制小组,并与厂家及时沟通,会同设备管理小组对医疗器械风险进行预警,对存在的问题及时采取有效干预措施,并形成科室不良事件处置整改档案。
医院作为医疗器械的大规模使用单位,厂家应变被动为主动,定期来院收集、记录医疗器械的质量问题与医疗器械不良事件信息,及时维修和整改,提高产品的设计、性能和功效,提高企业竞争力[9,16]。
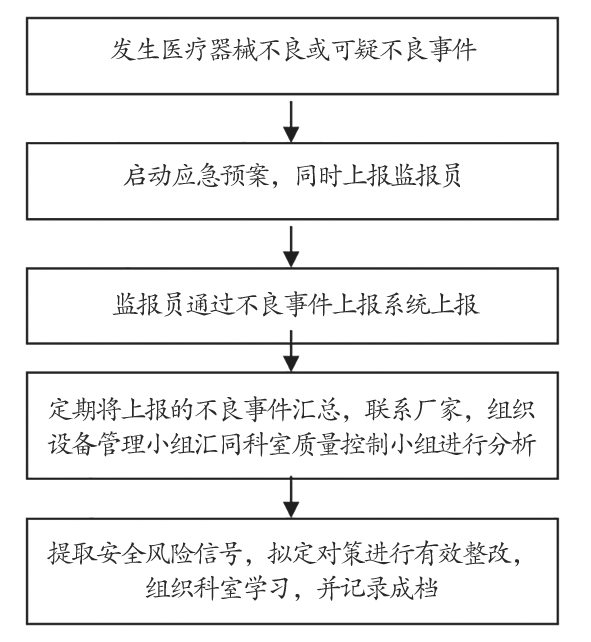
图2 医疗器械不良事件处置流程
4 小结
动力系统、医用内窥镜系统只是手术室设备的一部分,众所周知,手术室设备具有设备种类多,贵重、精细、直接作用于患者等特点,而绝大部分的手术设备都属于Ⅲ类医疗器械,设备本身安全风险系数较高加之设备使用人员牵扯多部门多岗位,这些因素造成手术室设备工程师设备的预防性维护保养和设备的质量管理,任务重、难度高[17-18]。本文对动力系统和医用内窥镜质量控制的对策思考和讨论,同样应用于手术室其他设备。不良事件的上报监测,提高医疗安全质量的同时,促进了医疗质量的精细化管理[19],也促进了医疗器械厂家售后服务质量的发展和提高。
[1]卫医管发[2010]4号,卫生部关于印发《医疗器械临床使用安全管理规范(试行)》的通知[Z].
[2]汤黎明,吴敏,沈苏静,等.浅谈医院医疗器械不良事件监测与管理体制建立[J].中国医疗设备,2006,21(2):41-42.
[3]国家食品药品监管局.总局关于发布医疗器械分类目录的公告(2017年第104号)[EB/OL].(2017-08-31)[2017-09-04].2017年第104号公告附件.docx.http://samr.cfda.gov.cn/WS01/CL0087/177089.html.
[4]孙丽霞,毕惠萍.浅谈颅脑外科手术动力系统术后清洗和保养的注意事项[A].2014年河南省现代手术室护理安全暨管理学术交流会议论文集[C].河南省护理学会,2014:3.
[5]史红梅,朱社宁,都红蕾,等.加温二氧化碳气腹对妇科腹腔镜手术患者的影响[J].中国妇幼保健,2012,27(18):2836-2838.
[6]杨俊,钱正瑛.“鱼骨图”在医疗设备风险控制中的应用[J].江苏医药,2014,40(5):608-609.
[7]葛秋菊.鱼骨柏拉图分析法在消毒供应中心质量管理中的应用[J].齐鲁护理杂志,2018,24(9):69-72.
[8]陈锐.应用持续性质量改进降低神经外科动力系统坏损率[J].中国医疗设备,2017,32(1):154-156.
[9]努尔江·沙布开,余永强,蒋冬贵,等.可疑医疗器械不良事件报告表完整性分析[J].中国药物警戒,2010,7(9):542-546.
[10]尚金华.医疗设备质量管理与风险控制体系分析[J].当代医学,2016,22(35):19-20.
[11]刘慧萍.医疗器械不良事件风险管理思考[J].中国医疗器械信息,2017,23(66):133-135.
[12]刘玉涛,郭凯,等.手术动力系统实施标准化管理的效果分析[J].护士进修杂志,2016,31(8):700-701.
[13]唐丽琴,黄静,王国蓉.手术室腔镜器械不良事件原因分析及防范[J].川北医学院学报,2018,33(6):954-956.
[14]曲华,宋振兰,朱永建,等.手术室护士手册[M].北京:人民卫生出版社,2011.
[15]罗志辉.医院可疑医疗器械不良事件监测与上报管理[J].医疗装备,2019,32(1):70-72.
[16]宋来全,王鑫.我院可疑医疗器械不良事件上报情况分析及思考[J].中国医疗设备,2019,(3):149-151.
[17]金国春,杨巧玲.医院手术室设备的使用与管理[J].中国医药管理杂志,2018,2(22):44-45.
[18]胡亚冰.手术室医疗设备的维修[J].医疗装备,2018,31(17):144-145.
[19]尹爱群.烟台市药品不良反应报告和监测工作指南[M].天津:天津科学技术出版社,2018.
Analysis and Thought on Adverse Events of Medical Devices in Operating Room