超声射频信号定量分析发现关节软骨退行性变的可行性研究
引言
膝关节软骨退行性变在各种膝关节疾病中(如骨关节炎、类风湿性关节炎等)相当常见,随着病变发展,可引起膝关节疼痛,造成膝关节功能障碍。早期诊断、早期治疗是改善预后的关键[1]。但目前的诊断手段均存在一定局限性,常规的X线和CT并不能直观地显示软骨病变;核磁对于软骨的显示虽佳,但其价格昂贵、耗时久,并不是临床膝关节炎患者的常规检查方式;高频超声经济、便捷,可以清晰地显示关节软骨,但对软骨退行性改变的评估仍然存在主观、敏感性差等问题。基于超声射频信号定量分析的研究表明,原始射频信号较灰阶超声图像能够提供更多的组织信息,早期发现病理改变。本研究将提取膝关节滑车软骨的超声原始射频信号,评估其早期发现软骨退行性改变的可行性。
1 材料与方法
1.1 临床资料
选择2018年4~10月入院行膝关节镜检查的患者58人60例膝关节作为研究对象。其中韧带损伤30例,髌骨脱位4例,半月板损伤8例,骨性关节炎18例。以关节镜结果为金标准将病人分为病例组及对照组。
病例组:关节镜结果显示股骨滑车软骨退行性变患者39人40例膝关节,其中男17人,女22人,年龄30~69岁,平均(54±12)岁。
对照组:关节镜结果显示股骨滑车软骨正常患者19人20例膝关节,其中男12人,女7人,年龄18~37岁,平均年龄(24±5)岁。
1.2 仪器与方法
使用 GE LOGIQ E9(美国),9L 高频线阵探头,配备原始射频信号开放端口。所有受试者均平卧于检查床,膝关节屈曲90°,由同一医师于髌骨上缘采集股骨滑车软骨横切面的常规灰阶及射频信号,采集过程中探头垂直于股骨长轴。
所有数据均于仪器内置肌骨条件B-Mode模式下采集,图像深度深度3.5 cm,增益及其他参数保持原始设置不变,聚焦置于软骨平面。
1.3 数据分析
1.3.1 常规灰阶超声图像分析
由一位具有10年肌骨超声经验的非操作医师对软骨的常规灰阶图像进行盲法判读并分类:软骨形态正常、前表面光滑清晰且内部回声均匀记录为正常;软骨表面欠清晰,内部回声增强和(或)软骨出现缺损记录为异常。
1.3.2 超声射频信号的参数分析
采用Matlab 2016对原始射频信号进行图像重建,选取滑车软骨区域作为感兴趣区域并进行10个参数的计算,分析软骨上边界和下边界的声学特征,并与软骨内部声学特征进行比较。具体分析参数如下:上边界粗糙度(URI_ant)、上边界反射强度(R_ant)、上边界反射均匀度(SVR_ant)、上边界和内部回波对比度(Contrast_ant)、下边界粗糙度(URI_post)、下边界反射强度(R_post)、下边界超声反射均匀度(SVR_post)、下边界和内部回波对比度(Contrast_post)、内部反射强度平均值(R_mean)、内部回声均匀度(std)(图1)。主要参数公式如下:

(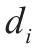 :软骨上/下边界某一点到探头的距离;d:软骨上/下边界各点到探头的平均距离;Ai软骨上/下边界反射强度
:软骨上/下边界某一点到探头的距离;d:软骨上/下边界各点到探头的平均距离;Ai软骨上/下边界反射强度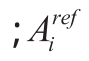 :对照实验中,相同深度下钢板全反射强度;
:对照实验中,相同深度下钢板全反射强度; :软骨上/下边界反射强度;
:软骨上/下边界反射强度;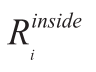 :距离上/下边界20个采样点的软骨内部反射系数;Ri软骨上/下边界某一点的反射强度;R:软骨上/下边界各点的平均反射强)
:距离上/下边界20个采样点的软骨内部反射系数;Ri软骨上/下边界某一点的反射强度;R:软骨上/下边界各点的平均反射强)

图1 射频信号重建图
1.4 统计学分析
数据分析采用SPSS 23.0统计软件,两组间均数比较采用独立样本t检验,同时绘制ROC曲线。计算射频信号参数及常规高频灰阶超声检测软骨退变的敏感性、特异性及准确率。均以P<0.05为差异有统计学意义,P<0.01有显著性差异。
2 结果
2.1 高频超声灰阶图像分析
病变组40例中,27例滑车软骨被诊断为退变,13例被诊断为正常;对照组20例4例被诊断退变,16例被诊断为正常(图2)。其诊断敏感度、特异度、准确率、阳性预测值及阴性预测值,见表1。
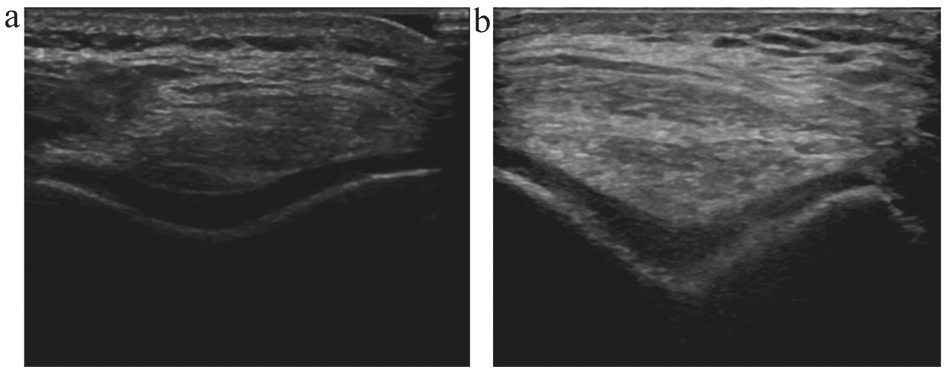
图2 股骨滑车软骨高频超声灰阶图像
注:a.正常;b.异常:软骨表面欠光滑,内部回声增强,局部可见软骨缺损。
表1 灰阶超声图像及部分参数检测软骨退变的敏感性、特异性及准确性
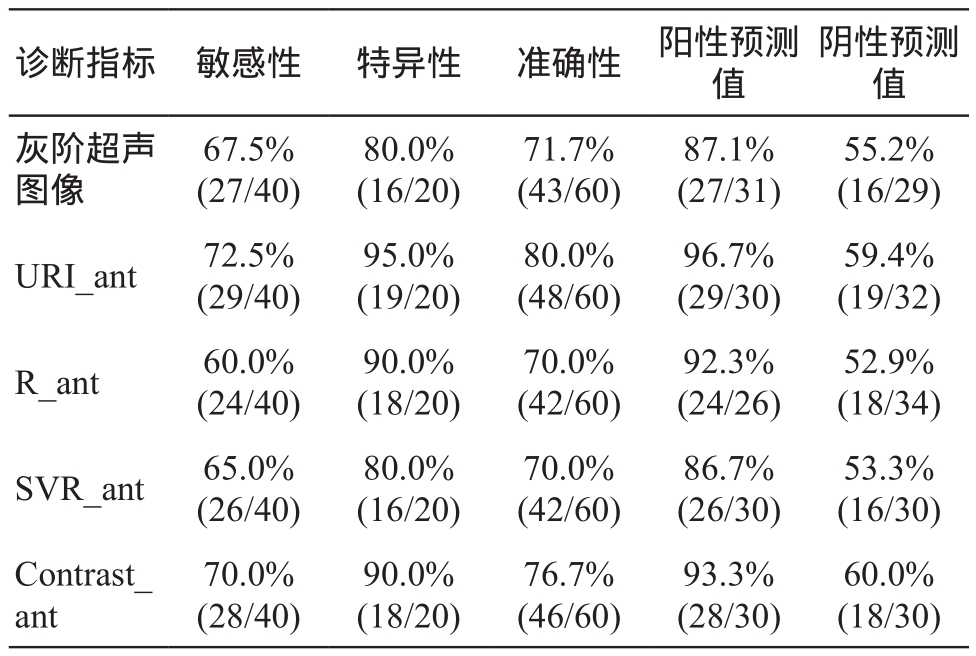
诊断指标 敏感性 特异性 准确性 阳性预测值阴性预测值灰阶超声图像55.2%(16/29)URI_ant 72.5%(29/40)67.5%(27/40)80.0%(16/20)71.7%(43/60)87.1%(27/31)59.4%(19/32)R_ant 60.0%(24/40)95.0%(19/20)80.0%(48/60)96.7%(29/30)52.9%(18/34)SVR_ant 65.0%(26/40)90.0%(18/20)70.0%(42/60)92.3%(24/26)60.0%(18/30)53.3%(16/30)Contrast_ant 80.0%(16/20)70.0%(42/60)86.7%(26/30)70.0%(28/40)90.0%(18/20)76.7%(46/60)93.3%(28/30)
2.2 基于射频信号的多参数分析
病例组的URI_ant(8.84±0.65)显著高于对照组(7.38±1.08)(P<0.01),病例组的 R_ant(0.11±0.06)显著低于对照组(0.17±0.07)(P<0.01),病例组的 SVR_ant(0.07±0.04)显著低于对照组(0.12±0.06)(P<0.01),病例组的Contrast_ant(6.13±1.36)显著低于对照组(9.25±3.26)(P<0.01),其他参数在两组间没有统计学差异(表2)。
运用ROC曲线分析各参数对软骨退变的诊断价值,结果表明 URI_ant、R_ant、SVR_ant和 URI_post分别以 8.454、0.096、0.070、6.436为截点时,曲线下面积最大,分别为0.904、0.774、0.753、0.846。各参数检测软骨退变的敏感性、特异性、准确率、阳性预测值及阴性预测值,见表1。
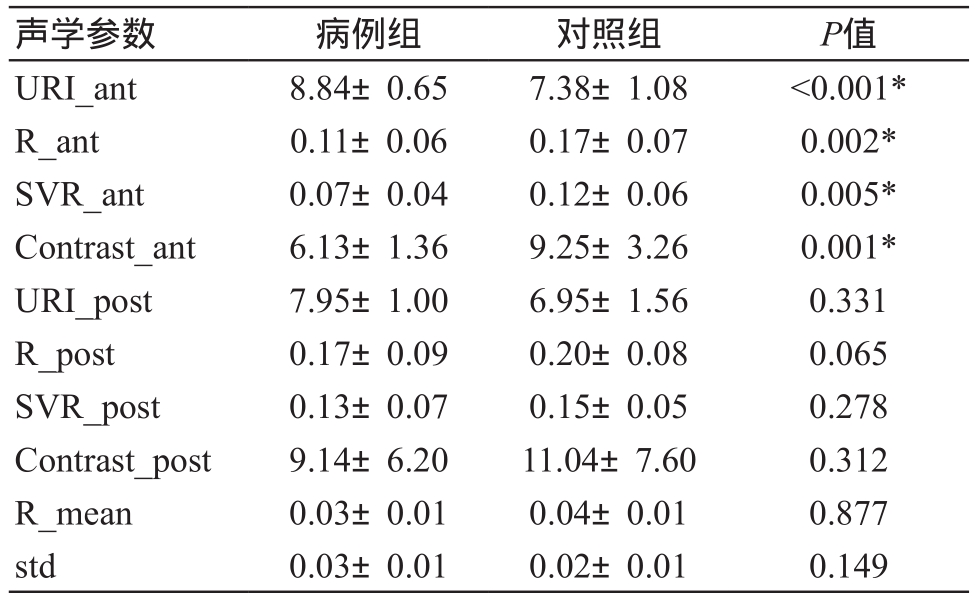
表2 病例组与对照组的参数比较(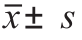 )
)
注:*P<0.01。
声学参数 病例组 对照组 P值URI_ant 8.84±0.65 7.38±1.08 <0.001*R_ant 0.11±0.06 0.17±0.07 0.002*SVR_ant 0.07±0.04 0.12±0.06 0.005*Contrast_ant 6.13±1.36 9.25±3.26 0.001*URI_post 7.95±1.00 6.95±1.56 0.331 R_post 0.17±0.09 0.20±0.08 0.065 SVR_post 0.13±0.07 0.15±0.05 0.278 Contrast_post 9.14±6.20 11.04±7.60 0.312 R_mean 0.03±0.01 0.04±0.01 0.877 std 0.03±0.01 0.02±0.01 0.149
3 讨论
膝关节软骨为透明软骨,附着于运动关节的骨性关节面,是组成活动关节面的弹性负重组织。作为人体最大的负重关节,膝关节软骨也是最易发生退行性变的部位。多项研究表明,在软骨病变早期可通过细胞保护剂、生长因子治疗,同时可通过物理治疗、减重等手段来逆转软骨的病理改变,从而有效阻止疾病进展[2]。关节镜检查是诊断、评估软骨退行性变的金标准,但作为一种有创检查手段,其重复性受限,一些患者难以耐受,故在阻止或延缓膝关节软骨退行性变的进一步发展中,仍需要一种无创、可重复的检查手段。
已有研究[3-4]证明常规高频超声可通过对软骨的厚度、边缘及内部回声进行软骨情况的评估,但目前临床应用较少,主要问题是缺乏统一的诊断标准,且受成像设备以及成像条件、操作者的个体认知及经验等影响严重。本研究中常规高频超声的诊断效果差强人意,除了以上影响因素以外,其主要原因是病例组部分病例软骨退变处于早期阶段,利于常规超声辨别的较明显的病变特征(如软骨缺损、变薄)尚未出现。
超声射频信号是指超声探头发射声学脉冲波在生物组织内传播、相互作用后组织反射回来的通过超声探头接收到的回波信号。相较于常规超声的灰度信息,该信号没有经过任何图像处理,保留着不同组织细微结构的振幅和相位等全部信息[5]。通过对射频信号进行多参数提取,可对软骨进行定量分析。已有国外学者利用射频信号参数对离体软骨进行定量分析,证实其有效性,但在体软骨的相关研究鲜有报道[6-8]。本研究初步验证了其在体应用的可行性。
早期的软骨退变表现为透明软骨浅表层的糖胺聚糖的丢失和胶原纤维的排列紊乱[9]。退变进展一定程度则会发生结构性改变,软骨表面的不规则越来越明显,成为小的裂缝并逐渐向下延伸直至软骨下骨。软骨由浅至深逐步崩解脱落,局部厚度变薄,最后软骨下骨暴露[10]。本研究表明一些早期表现在常规高频超声中并无明显差异,即使有经验的医师判读也难以鉴别。我们采用原始射频信号分析发现与软骨前表面相关的参数URI_ant、R_ant、SVR_ant及Contrast_ant在病变组与对照组软骨之间均有统计学差异,符合软骨退变的浅表层病理学改变,即其成分的变化和上表面粗糙度的增加。这也与国外学者[11-14]离体软骨相关声学参数的研究相一致。
膝关节软骨退变的病理变化除了表浅退化还存在基底退化[15],骨关节炎早期钙化层软骨细胞会激活表现出生长板细胞特性,继而表达肥大的软骨细胞表型,分泌Ⅹ型胶原,引起软骨基质矿化、潮线前移或复制;同时,来自骨髓腔的新生血管侵入钙化层,使钙化层被骨组织慢慢取代[16-18]。但本研究并未发现病变组与对照组间软骨后表面参数的差异,可能与样本量以及超声机器调节有关,还有待进一步验证。
本研究亦存在一些不足,首先样本量有限,且仅对膝关节滑车软骨进行了分析,并未全面采集内外侧髁及髁间软骨的信号;其次并未对软骨退变进行分级。未来可以扩大样本量,更换不同频率探头,获得关节镜或病理标本进行更深层次的研究。
4 结论
基于超声射频信号的参数URI_ant、R_ant、SVR_ant及Contrast_ant的定量分析,对评估股骨滑车软骨退变具有一定潜力,尤其是URI_ant和Contrast_ant,具有在体应用的可行性,并能够早于常规超声发现异常。未来需要进一步扩大样本量,进一步验证参数间与退行性变程度的相关性。
[1]Madry H,Kon E,Condello V,et al.Early osteoarthritis of the knee[J].Knee Sur Sports Traum Arth,2016,24(6):1753-1762.
[2]Hurtig M,Chubinskaya S,Dickey J,et al.BMP-7 protects against progression of cartilage degeneration after impact injury[J].J Orthop Res,2009,27(5):602-611.
[3]Saarakkala S,Waris P,Waris V,et al.Diagnostic performance of knee ultrasonography for detecting degenerative changes of articular cartilage[J].Ultrasound Q,2012,20(5):376-381.
[4]Nieminen HJ,Zheng Y,Saarakkala S,et al.Quantitative assessment of articular cartilage using high-frequency ultrasound: research findings and diagnostic prospects[J].Crit Rev Biomed Eng,2009,37(6):461.
[5]严郁,朱伟,竺明月,等.基于MATLAB的超声射频信号成像重建设计[J].中国医疗设备,2018,33(8):86-88.
[6]Wataru K,Yasuaki N,Akira I,et al.Ultrasound parameters for human osteoarthritic subchondral bone, ex vivo : comparison with micro-computed tomography parameters[J].Ultrasound Med Biol,2018:S0301562918302369.
[7]Wang Q,Liu Z,Wang Y,et al.Quantitative ultrasound assessment of cartilage degeneration in ovariectomized rats with low estrogen levels[J].Ultrasound Med Biol,2016,42(1):290.
[8]Zhang J,Xiao L,Tong L,et al.Quantitative evaluation of enzyme-induced porcine articular cartilage degeneration based on observation of entire cartilage layer using ultrasound[J].Ultrasound Med Biol,2018:S0301562917324602.
[9]Madry H,Luyten FP,Facchini A.Biological aspects of early osteoarthritis[J].Knee Surg Sport Tra,2012,20(3):407-422.
[10]Pritzker KPH, Gay S,Jimenez SA,et al.Osteoarthritis cartilage histopathology: grading and staging[J].Osteoar Cart,2006,14(1):13-29.
[11]Männicke N,Schöne M,Oelze M,et al.Articular cartilage degeneration classification by means of high-frequency ultrasound [J].Osteoarthr Cartil,2014,22(10):1577-1582.
[12]Niu HJ,Wang Q,Wang YX,et al.Ultrasonic reflection coefficient and surface roughness index of OA articular cartilage: Relation to pathological assessment[J].BMC Muscul Disord,2012,13(1):34.
[13]Kiyan W,Ito A,Nakagawa Y,et al.Relationships between quantitative pulse-echo ultrasound parameters from the superficial zone of the human articular cartilage and changes in surface roughness, collagen content or collagen orientation caused by early degeneration[J].Ultrasound Med Biol,2017,43(8):1703-1715.
[14]Saarakkala S,Töyräs J,Hirvonen J,et al.Ultrasonic quantitation of superficial degradation of articular cartilage [J].Ultrasound Med Biol,2004,30(6):783-792.
[15]沙雷亚尔.O'Connor关节镜外科学[M].上海:复旦大学出版社,2001.
[16]Goldring M,Goldring S.Osteoarthritis[J].J Cell Physiol,2007,213(3):626-634.
[17]Zhang J,Chen S,Chen W,et al.Ultrastructural change of the subchondral bone increases the severity of cartilage damage in osteoporotic osteoarthritis of the knee in rabbits[J].Pathol Res Pract,2018,214(1):38-43.
[18]Fell N,Lawless B,Cox S,et al.The role of subchondral bone, a nd its histomorphology, on the dynamic viscoelasticity of cartilage, bone and osteochondral cores[J].Osteoarthr Cartil,2019,27(3):535-543.
Feasibility Study on Detection of Articular Cartilage Degeneration by Quantitative Analysis Based on Ultrasound Radio Frequency Signal