专论——定量成像技术与人工智能
编者按:定量成像技术是通过某种成像方法和技术开发对组织的特性进行量化测量的技术,在目前的医学成像领域应用广泛,是各医学成像领域研究人员关注的焦点,也是人工智能辅助诊断不可或缺的中间过程。本栏目优选5篇定量成像技术及人工智能辅助诊断方面的探索性研究,涉及超声颈动脉血流多点频谱多普勒分析方法研究、超声颈动脉弹性成像方法研究、超声多参数定量分析诊断股骨滑车软骨退行性变研究、超声弹性成像的支持向量机实现对颈动脉易损斑块的自动检测研究、三维MR图像上的脑肿瘤分割深度神经网络算法研究等。体现了定量成像技术的临床应用价值。当然,这些研究还只是方法学研究的摸索,其实际临床应用价值还有待临床多中心研究的进一步验证。
栏目主编:邵金华
邵金华,清华大学医学院助理研究员,从事多年生物医学工程研究、医疗装备软硬件的研发和产业化工作。先后主持国家自然科学基金青年基金项目、国家“十二五”科技支撑计划子课题、江苏省成果转化项目、江苏省科技支撑计划等多项课题;发表SCI论文十余篇,申请专利200多项。获得北京市科学技术三等奖、河北省科学技术一等奖、江苏省双创之星、科技部科技推进计划人才和国家万人计划领军人才称号。作为联合创始人带领团队研发的FibroTouch肝脏纤维化无创诊断设备填补了国内空白,相关产品性能达到国际领先水平,产品成功进行了产业化,获得了包括清华启迪创投、联想君联资本等知名风险投资机构上亿元投资,目前已获得美国FDA、欧盟CE认证和中国CFDA认证,并在国内上千家医疗机构使用,产生经济效益数亿元,每年服务数百万肝病人群。

基于线阵超声探头多波束并行发射的颈动脉血流多点频谱多普勒分析
引言
在全球范围内,心血管疾病是人类的主要死亡原因之一[1]。近年来,我国心血管疾病的发病人数也在持续增加[2]。在诸多心血管疾病中,动脉粥样硬化所致的颈动脉狭窄多发于颈内动脉,导致脑部供血异常[3-5]。目前,判断颈内动脉狭窄的常规手段是颈部B模式超声检测或者频谱多普勒超声检测[3]。美国超声医师学会在2003年旧金山会议共识声明中推荐了颈内动脉狭窄的判断标准,给出了颈动脉相关生理参数的临床参考值,包括颈内动脉(Internal Carotid Artery,ICA)与颈总动脉(Common Carotid Artery,CCA)的血流峰值流速(Peak Systolic Velocity,PSV)的比值,简单表示为R值[4-5]。
传统的脉冲多普勒技术一次只能选择血管中的某一位置进行采样,进而分析得到频谱多普勒图像。如果需要测量颈内动脉与颈总动脉的血流峰值流速比值,通常需要二次测量,在观察到颈总动脉后,沿颈总动脉长轴向上追踪至颈动脉分叉处和颈内动脉[4];先后选取不同位置的采样体积,分别测量颈总动脉和颈内动脉的血流峰值流速。而脉冲多普勒的能量输出较一般二维B模式成像的能量输出高,进行快速的检查有利于减少患者接受超声辐射的时间[6]。先后分别测量颈总动脉和颈内动脉的血流峰值流速,因为测得的峰值流速并不属于同一个心动周期,成像截面也可能并不一致,所以可能引入一定的误差。在超声成像领域,借助超声多波束并行发射技术(Multi-Line Transmission,MLT)有可能实现血管中多个位置的同时采样分析,进而简化操作流程,缩短检查时间。
国际上,超声多波束并行发射技术的研究主要集中在基于相控阵超声探头的心脏成像[7-9],基于线阵超声探头的多波束并行发射技术的探究较少,而且也尚未用于颈动脉血流测量[10]。本文将基于线阵超声探头,实现多波束并行发射技术;进一步,同时获得血管中多个采样体积的频谱多普勒图像;为了验证方法的可靠性,将把多波束并行发射的实验结果同目前临床广泛使用的单波束发射以及近年来引起关注的平面波发射的实验结果进行对比分析。
1.方法
1.1 脉冲多普勒技术
使用超声探头,发射超声脉冲后,通过距离采样门获取某一深度采样体积对应的超声回波信号,采样体积的大小和深度都可以通过距离选通门调节。持续发射超声脉冲,并对采样体积对应的超声回波信号进行持续采样,得到该采样体积沿慢时方向的一组回波信号。对该组回波信号进行离散短时傅里叶变换,如式(1):
上式中x(n)为采样体积沿慢时方向的回波信号![]() 为一个M点的窗函数,m和k分别为输出的离散时间变量和离散频率变量[11],对其进行对数压缩等优化处理[12],即可得到频谱多普勒图像,显示出不同血流速度的分布以及随时间的变化。
为一个M点的窗函数,m和k分别为输出的离散时间变量和离散频率变量[11],对其进行对数压缩等优化处理[12],即可得到频谱多普勒图像,显示出不同血流速度的分布以及随时间的变化。
1.2 线阵探头多波束并行发射可行性验证
应用超声仿真软件Field II[13],对线阵探头的发射声场进行仿真。在传统的聚焦波发射即单波束发射(Single-Line Transmission,SLT)的基础上,对探头各个阵元对应的脉冲发射延时和变迹进行改动。利用特殊形式的延时和变迹,将线阵探头的孔径进行分块,得到若干子孔径,每一子孔径内均采用类似单波束发射的发射延时;同时,为了抑制多波束并行发射时交叉伪影(crosstalk)的影响,每个子孔径均施加一定的变迹[14],以实现多个子孔径同时发射波束,即多波束并行发射。为了方便理解,图1给出了三波束并行发射(3-MLT)时在128阵元的线阵探头上设置的发射延时以及变迹,波束向左偏转10°,每个子孔径采用汉宁窗变迹。通过仿真发射声场,可见看出这样的发射延时以及变迹可以产生三条波束同时发射的效果。

图1 线阵探头三波束并行发射的脉冲延时和变迹设置以及对应的声场分布
注:a.脉冲延时;b.变迹;c.声场分布。
1.3 实验
1.3.1 采集模式及参数
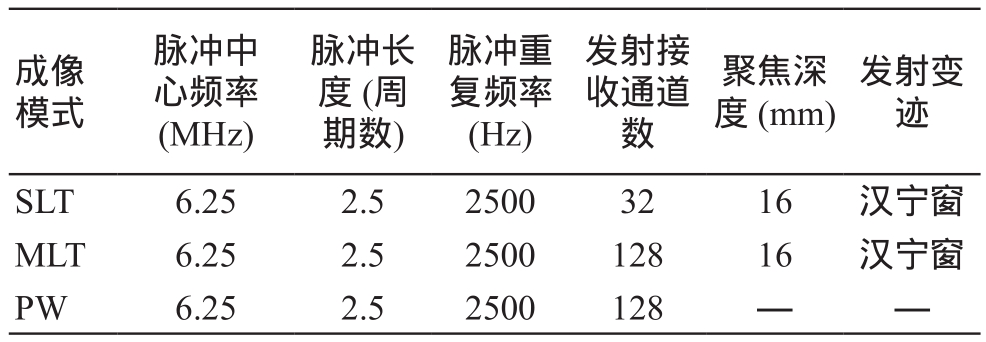
为了定量探究多波束并行发射测量结果的准确性,我们除了使用多波束并行发射模式外,还采用单波束发射模式以及平面波发射模式,三种发射模式均进行仿真、仿体和在体实验,实验采集参数如表1所示。
表1 实验采集参数设置
成像模式脉冲中心频率(MHz)脉冲长度 (周期数)脉冲重复频率(Hz)发射接收通道数聚焦深度 (mm)发射变迹SLT 6.25 2.5 2500 32 16 汉宁窗MLT 6.25 2.5 2500 128 16 汉宁窗PW 6.252.52500128— —
表1 中,多波束并行发射时采用汉宁窗变迹指的是在线阵探头的每一个子孔径内均采用该变迹。
1.3.2 仿真实验
应用超声仿真软件Field II,在二维空间(横向尺寸40 mm,轴向尺寸35 mm)设置随机分布的散射子,每单位面积约分布 个散射子,
个散射子, 为发射脉冲的波长。二维空间的中间位置处(深度15~20 mm)存在一水平直管,直管管半径为2.5 mm,周围组织与管内散射子的强度比为 40 dB。
为发射脉冲的波长。二维空间的中间位置处(深度15~20 mm)存在一水平直管,直管管半径为2.5 mm,周围组织与管内散射子的强度比为 40 dB。
管内散射子的运动速度遵循抛物线型血流分布,即:
其中,V(r)是随直管径向位置而改变的速度值,Vmax为最大速度值,R为直管半径。颈动脉血液峰值流速一般在1m/s左右[4-5],所以Vmax设置为1 m/s。仿真实验中,线阵探头阵元间距设置为0.3 mm;采用三波束并行发射,单波束发射、三波束并行发射和平面波发射的发射偏角均设置为10°;单波束发射焦点的横向坐标为0 mm,三波束并行发射的三个焦点的横坐标分别为-10、0和10 mm。
1.3.3 仿体实验
使用256发射接收通道的Vantage超声采集系统(Verasonics公司,美国)和L10-5线阵探头(嘉瑞公司,中国),对Gammax 1425A标准血流仿体(Gammax公司,美国)进行实验。该仿体内含一个电控流体泵和一个循环流体管腔,管腔内封装有特殊流体,该流体在声学特性上和人体血液相似 :声速大小为 (1550±10) m/s,密度为 1.03 g/cm3,流体内含微粒平均直径为4.7 μm,微粒浓度为20 mg/mL。通过电控流体泵控制流体在管腔内循环流动的速率,在水平直管部位产生稳定的抛物线型层流。图2为该仿体内部结构示意图,水平直管位于仿体浅表部位,在深度为20 mm处有一个直径5 mm的水平直管,设置其内流速最大值为1 m/s。同仿真实验类似,仿体实验中,单波束发射、三波束并行发射和平面波发射的发射偏角均设置为10°,单波束发射焦点的横向坐标为0 mm,三波束并行发射的三个焦点的横坐标分别为-10、0和10 mm。
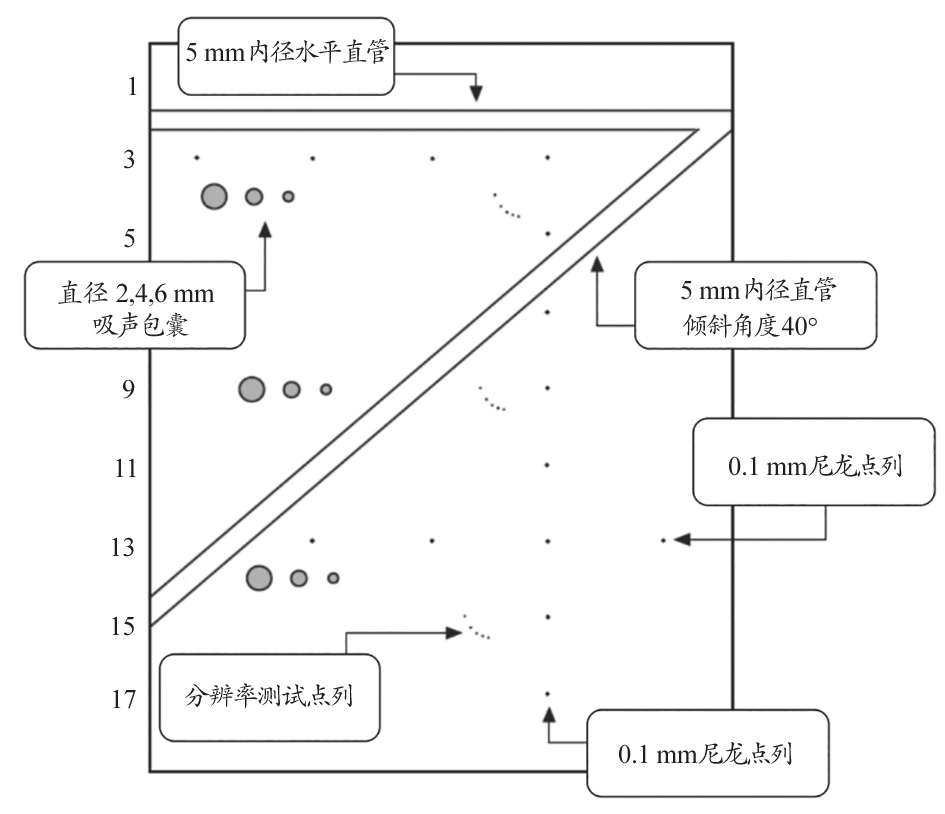
图2 Gammax 1425A标准血流仿体内部结构示意图
1.3.4 在体实验
使用Vantage超声采集系统扫描健康志愿者的左颈动脉分叉处,采集序列分为四个阶段:单波束发射扫描颈总动脉;单波束发射扫描颈内动脉;双波束并行发射扫描以及平面波发射扫描。每个阶段采集时长2.5 s,双波束并行发射的两个聚焦位置和单波束分别扫描颈总动脉和颈内动脉的两个聚焦位置一致。双波束并行发射和平面波发射扫描时,因为颈总动脉和颈内动脉血管不是沿水平方向,而且二者走向不一致,所以不设置发射偏角,后期根据B模式图像在数据处理时进行角度修正。颈总动脉和颈内动脉内采样体积的横坐标分别为-15 mm和15 mm。
1.3.5 数据采集及分析
在单波束发射模式中,每次发射一个固定位置的聚焦波束,使用脉冲多普勒技术,沿波束方向选取不同深度的采样体积,进行频谱多普勒分析,得到相应的频谱多普勒图像。在多波束发射模式中,同时发射若干条聚焦波束,在每一条波束方向上,都可以选取不同深度的采样体积,进行频谱多普勒分析,从而同时获取多个不同波束位置上的频谱多普勒图像。在平面波发射模式中,所有阵元同时发射超声脉冲,形成平面波;这可以简单理解为扫描区域内的所有波束同时发射,因此,可以选取扫描区域内的任何一个位置作为采样体积,进而分析得到其频谱多普勒图像。
仿真和仿体实验中,直管内的流体为稳定层流,通过频谱多普勒图像可以得到管内不同深度的流体速度大小,进而可以和抛物线型稳定层流的理论速度曲线进行定量比较,直管内径为5 mm,选取0.5 mm为采样间隔,在管内获取11个采样体积的流体速度大小,按下式计算其与理论值之间的均方根误差(RMSE)[15],比较得到不同发射模式间误差的相对大小。
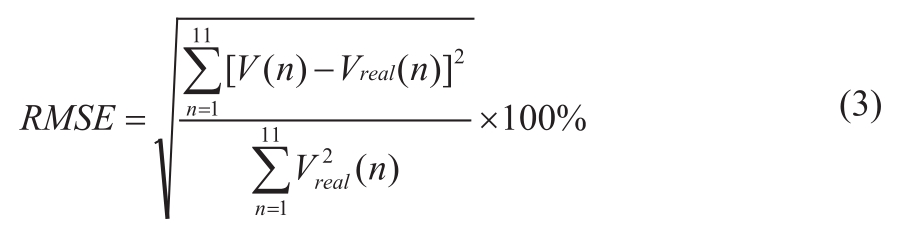
其中,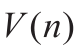 是计算出来的直管内随深度位置改变的流体速度值,
是计算出来的直管内随深度位置改变的流体速度值,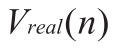 为抛物线型稳定层流的理论速度值。
为抛物线型稳定层流的理论速度值。
在体实验中,可以得到波束方向上某一深度采样体积的频谱多普勒图像,而频谱随心动周期呈现出规律性的周期变化。因为在体实验缺乏理论真值,所以我们选取临床上广泛接受的单波束发射的测量结果作为参照,在颈总动脉和颈内动脉处,均获得三种发射方式的频谱多普勒图像,使用形态学方法进一步得到频谱包络[12]。按下式分别计算多波束并行发射和平面波发射获得的频谱包络相对于单波束发射获得的频谱包络之间的相关系数[15],从而定量评估不同方法的结果。
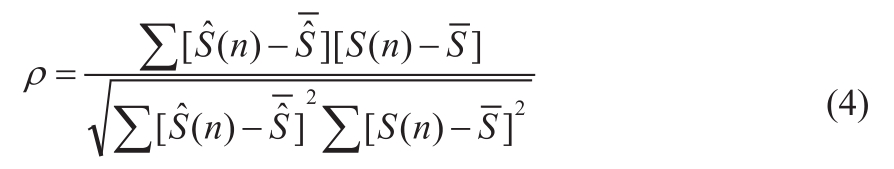
其中,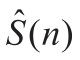 表示使用多波束并行发射或平面波发射获得的频谱包络,
表示使用多波束并行发射或平面波发射获得的频谱包络,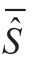 表示对应的频谱包络的均值;
表示对应的频谱包络的均值;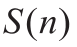 表示使用单波束发射获得的频谱包络,
表示使用单波束发射获得的频谱包络,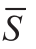 表示对应的频谱包络的均值。
表示对应的频谱包络的均值。
仿体和在体实验中,通过超声采集系统获得超声通道数据后,通过传统的延时叠加方式进行波束合成,得到波束合成后的超声射频数据。进一步,通过离散短时傅里叶变换获得频谱多普勒图像,其中,轴向数据采样窗的大小选为1 mm,慢时方向采用汉明窗,窗长为51.2 ms(128点),窗移动步长为3.2 ms (8点)。以上步骤均使用MATLAB软件进行离线处理。
2 结果
2.1 仿真实验
仿真实验得到的结果如图3所示,图3a为仿真模型的B模式图像。单波束发射模式始终扫描图中如白色实线所示的位置;多波束并行发射模式除了扫描白色实线对应的位置外,还可以同时扫描两条白色虚线对应的位置;平面波发射模式则可以对B模式图像中的任意位置进行扫描。我们选取白色实线位置处三种发射模式测量得到的流体速度分布曲线,如图3b所示。计算测量的流体速度分布和理论值之间的均方根误差,得到单波束发射、多波束并行发射和平面波发射三种模式的均方根误差分别为16%、16%和14%。
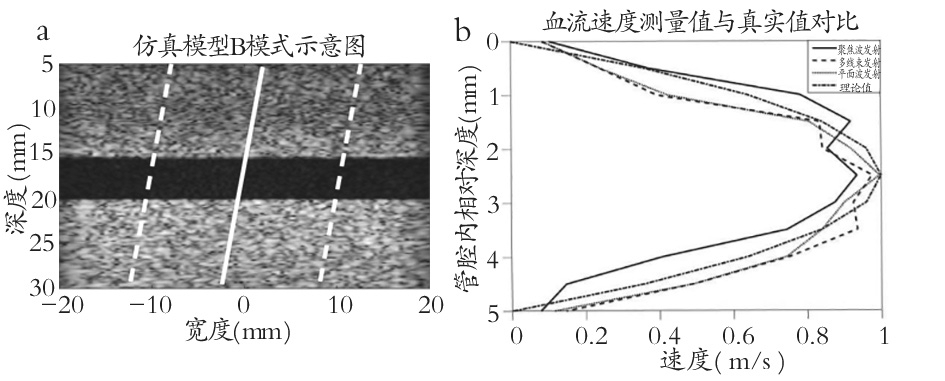
图3 三种扫描模式的仿真实验结果
注:a.仿真模型的B模式示意图,白色实线表示单波束发射扫描位置,白色实线及虚线表示多波束并行发射扫描位置;b.三种发射模式计算出的管内流体速度分布曲线及理论值。
2.2 仿体实验
仿体实验的结果如图4。图4a为血流仿体的B模式示意图。与仿真实验一样,白色实线表示单波束发射模式扫描的位置;多波束并行发射除了扫描白色实线对应的位置外,还可以同时扫描另外两条白色虚线对应的位置;平面波发射模式可以对B模式图像的任意位置进行扫描。同样地,选取白色实线位置处三种发射模式测量出来的流体速度分布曲线,如图4b所示。单波束发射、多波束并行发射和平面波发射三种模式测量的流体速度分布和理论值之间的均方根误差分别为20%、18%和18%。
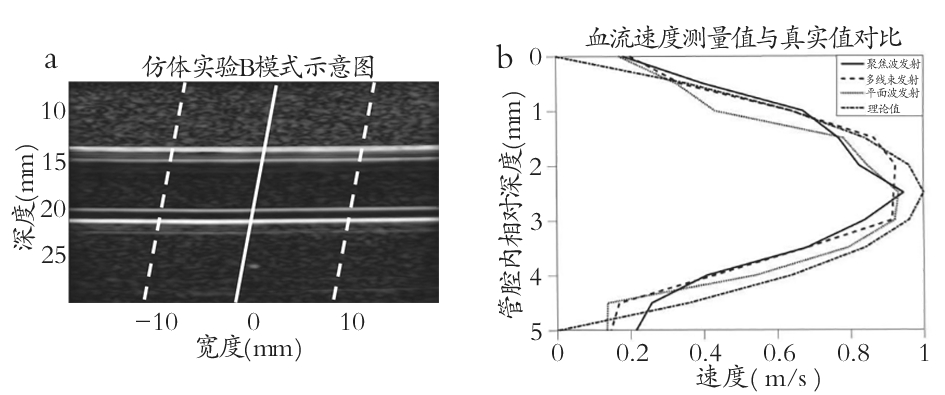
图4 三种扫描模式的仿体实验结果
注:a.血流仿体的B模式示意图,白色实线表示单波束发射扫描位置,白色实线及虚线表示多波束并行发射扫描位置;b.三种发射模式计算出的管内流体速度分布曲线及理论值。
2.3 在体实验
健康志愿者颈动脉分叉处的在体实验结果如图5所示。在图5a的B模式示意图中,圆点表示颈总动脉中选取的采样体积,方点表示颈内动脉中选取的采样体积。如前文所述,使用三种扫描方式,采集时长共10 s,分别得到圆点和方点处的频谱多普勒图像,如图5b和5c所示。图5b和5c中,白色虚线将图像分为Ⅰ、Ⅱ、Ⅲ和Ⅳ四段,分别对应前文所述的四个扫描阶段:单波束发射扫描颈总动脉;单波束发射扫描颈内动脉;双波束并行发射扫描以及平面波发射扫描。单波束发射模式来只能选择一个采样体积,所以在获得颈总动脉频谱图像的同时,无法得到颈内动脉的数据,图5b中Ⅱ部分表现为空白;同理,图c中Ⅰ部分表现为空白。图5b和5c中,白色实线显示了频谱包络。对于颈总动脉处的采样体积,选取单波束发射模式的频谱包络(图5b中Ⅰ部分内的白色曲线)作为参考,可以计算出多波束并行发射的频谱包络(图5b中Ⅲ部分内的白色曲线)和单波束发射的频谱包络的相关系数为0.92,平面波发射的频谱包络(图5b中Ⅳ部分内的白色曲线)和单波束发射的频谱包络的相关系数为0.81。对于颈内动脉处的采样体积,同样选取单波束发射模式的频谱包络(图5c中Ⅱ部分内的白色曲线)作为参考,可以计算出多波束并行发射的频谱包络(图5c中Ⅲ部分内的白色曲线)和单波束发射的频谱包络的相关系数为0.80,平面波发射的频谱包络(图5c中Ⅳ部分内的白色曲线)和单波束发射的频谱包络的相关系数为0.71。在单波束发射模式中,我们需要通过两次测量得到R值,为0.89;在多波束并行发射和平面波发射模式中,我们都可以通过一次测量得到R值的大小,分别为0.90与0.93。
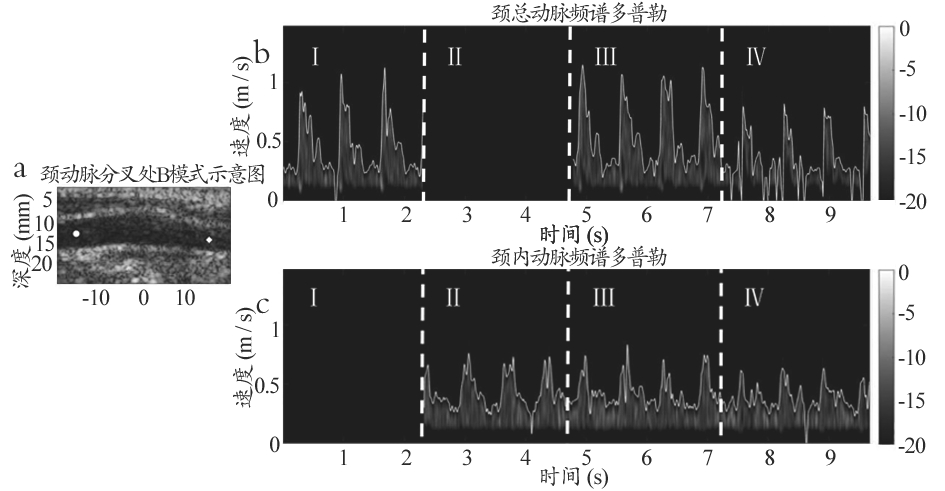
图5 三种扫描模式的在体实验结果
注:a.颈动脉分叉处B模式图像,圆点表示颈总动脉内采样体积,方点表示颈内动脉内采样体积;b.圆点位置处的频谱多普勒图像;c.方点位置处的频谱多普勒图像,b和c均由虚线分割成Ⅰ、Ⅱ、Ⅲ和Ⅳ四段,分别对应单波束采集颈总动脉、单波束采集颈内动脉、双波束并行发射采集和平面波发射采集。
3 讨论和结论
单波束发射是目前商用超声设备最常用的发射模式。通过仿真实验和仿体实验,我们可以发现,多波束并行发射和单波束发射的流体速度测量误差相近。而在体实验中,多波束并行发射可以同时获取多个位置采样体积的频谱多普勒图像。本研究同时选取了位于颈总动脉和颈内动脉的两个采样体积,相比于单波束发射测量,减少了多次测量,简化了操作流程,缩短了检查时间。在体实验中,多波束并行发射和单波束发射获得的频谱包络之间的相关系数较高,说明多波束并行发射的血流速度测量准确性与目前临床常用的单波束发射相近。
平面波发射是近年来超声成像研究领域的热点,在频谱多普勒分析上具有很大的潜力。在平面波发射模式中,每次发射都采集整个视野范围内的回波信号;所以,通过平面波发射的持续采集,可以获取任何一个位置的频谱多普勒图像[16-19]。但是,这种特殊的发射模式导致视野范围内的能量分布较为分散,进而导致图像的分辨率和对比度降低[20-21]。所以,在体实验中,我们可以看到平面波发射得到的频谱多普勒图像连续性较差。相关系数的计算也表明,相较于平面波发射,多波束并行发射的频谱包络测量结果更接近单波束发射的结果。
多波束并行发射也存在一定的局限。相较于传统的单波束发射,多波束并行发射需要系统具备任意波形发生器,以产生特定的声场分布[14]。平面波发射时,超声设备需要采集通道数据,设备硬件层面的系统架构需要重新搭建,系统的数据并行采集及处理能力都需要提升[22-23];多波束并行发射并不需要系统采集通道数据。在未来,基于线阵探头的多波束并行发射在参数优化以及硬件实现方面依旧需要更加细致的研究。尽管如此,随着研究的不断深入和工业技术的不断发展,多波束并行发射的潜力还将得到进一步的挖掘。
本研究基于线阵超声探头,实现了多波束并行发射,并将之用于颈动脉血流的多点频谱多普勒检测。仿真和仿体实验中,单波束发射、多波束并行发射和平面波发射三种发射模式的误差相当;在体实验表明,较于传统的单波束发射,在不牺牲原有准确性的基础上,多波束并行发射可以通过一次操作同时获得颈总动脉和颈内动脉的频谱多普勒图像。因此,基于线阵超声探头的多波束并行发射是一种有效且便捷地进行颈动脉血流多点频谱多普勒分析的方法。
[1]Organization WH.World health statistics 2016: monitoring health for the SDGs sustainable development goals[J].Geneva Switzerland WHO,2016,41:293-328.
[2]中国心血管病报告编写组.《中国心血管病报告2016》概要[J].中国循环杂志,2017,32(6):521-530.
[3]周永昌,郭万学.超声医学[M].6版.北京:人民军医出版社,2012:689-694.
[4]张武.现代超声诊断学[M].北京:科学技术文献出版社,2008:405-406.
[5]Barry B.Goldberg,John P.McGahan.超声测量图谱[M].2版.张缙熙,译.北京:人民军医出版社,2008:311-314.
[6]Roger C.Sanders,Tom Winter.超声诊断临床实践指南[M].4版.曹铁生,段云友,袁丽君,译.北京:人民军医出版社,2009:460-466.
[7]Tong L,Ramalli A,Tortoli P,et al.Wide-angle tissue Doppler imaging at high frame rate using multi-line transmit beamforming: an experimental validation in vivo[J].IEEE Trans Med Imaging,2016,35(2):521-528.
[8]Santos P,Tong L,Ortega A,et al.Acoustic output of multi-line transmit beamforming for fast cardiac imaging: a simulation study[J].IEEE Trans Ultr Ferroel Freq Control,2015,62(7):1320-1330.
[9]Ortega A,Provost J,Tong L,et al.A comparison of the performance of different multi-line transmit setups for fast volumetric cardiac ultrasound[J].IEEE Trans Ultr Ferroel Freq Control,2016,63(12):2082-2091.
[10]Nguyen MM,Ding X,Leers SA,et al.Multi-focus beamforming for thermal strain imaging using a single ultrasound linear array transducer[J].Ultrasound Med Biol,2017,43(6): 1263-1274.
[11]胡广书.现代信号处理教程[M].2版.北京:清华大学出版社,2015:60-61.
[12]齐敏超.全数字超声多普勒血流测量系统研究[D].北京:清华大学,2012.
[13]Jensen JA.FIELD: a program for simulating ultrasound systems[J].Med Biol EngComput,1997,34:351-353.
[14]Tong L,Ramalli A,Jasaityte R,et al.Multi-transmit beam forming for fast cardiac imaging—experimental validation and in vivo application[J].IEEE Trans Med Imaging,2014,33(6):1205-1219.
[15]Forsberg F,Oung H,Needleman L.Doppler spectral estimation using time-frequency distributions[J].IEEE Trans Ultr Ferroel Freq Control,1999,46(3):595-608.
[16]Evans DH,Jensen JA,Nielsen MB.Ultrasonic colour Doppler imaging[J].Interface Focus,2011,1(4):490-502.
[17]Poelma C.Ultrasound imaging velocimetry: a review[J].Exp Fluids,2017,58(1):3.
[18]Jensen J,Hoyos CAV,Holbek S,et al.Velocity estimation in medical ultrasound[J].IEEE Signal Proc Mag,2017,34(3):94-100.
[19]何琼,罗建文.超高速超声成像的研究进展[J].中国医学影像技术,2014,(8):1251-1255.
[20]Shattuck DP,Weinshenker MD,Smith SW,et al.Explososcan: a parallel processing technique for high speed ultrasound imaging with linear phased arrays[J].J Acoust Soc Am,1984,75(4):1273-1282.
[21]Park S,Aglyamov SR,Emelianov SY.Elasticity imaging using conventional and high-frame rate ultrasound imaging: experimental study[J].IEEE Trans Ultr Ferroel Freq Control,2007,54(11):2246-2256.
[22]Bercoff J,Montaldo G,Loupas T,et al.Ultrafast compound Doppler imaging: providing full blood flow characterization[J].IEEE Trans Ultr Ferroel Freq Control,2011,58(1):134-147.
[23]Saris A,Hansen H,Fekkes S,et al.A comparison between compounding techniques using large beam-steered plane wave imaging for blood vector velocity imaging in a carotid artery model[J].IEEE Trans Ultr Ferroel Freq Control,2016,63(11):1758-1771.
Multi-Point Spectral Doppler Analysis of Carotid Artery Using Multi-Line Transmission with Linear Array Ultrasound Probe