不同滤波方法对脑部PET图像质量和SUV值的影响
引言
神经内分泌肿瘤(Neuroendocrine Neoplasms,NENs)是一组起源于肽能神经元和神经内分泌细胞的异质性显著肿瘤,68Ga-DOTA-NOC PET/CT显像已成为诊断NENs的重要手段[1-3]。高质量PET图像是精确诊断NENs的基础,PET图像质量主要由注射剂量、病人体格、探测器性能、重建参数等因素决定[4-5]。在临床工作环境中,病人体格和探测器性能是固定的,且一般商业配置的68Ga-DOTA-NOC剂量不易根据病人体重进行调整,此时调整重建参数可作为提高PET图像分辨率的一个重要补偿手段。
PET重建参数包括重建算法、迭代次数、子集数量、矩阵大小、滤波处理等,其中有序子集期望最大(OSEM)+飞行时间技术(TOF)+点扩散技术(PSF)重建算法已被证实优于滤波反投影(FBP)算法,且有TOF技术迭次数设置为2,无TOF技术迭代次数设置为3,子集数量均为20。矩阵大小一般由探测器性能决定,体部采集采用256×256,脑部图像为128×128。我科采用的是上海联影112环数字光导PET/CT,滤波函数包含非局部均值滤波、高斯滤波、Metz滤波,其中非局部均值滤波是在一个目标像素周围区域平滑取均值的方法[6],主要基于像素灰度相关性和几何结构相似性,平滑噪声的同时不丢失细节信息;高斯滤波函数属于低通滤波器,平滑噪声性能优越[7];Metz是一种恢复型滤波函数,属于高通滤波器[8]。
目前国内外对68Ga-DOTA-NOC PET/CT的神经内分泌肿瘤临床诊断价值研究较多[9-11],而忽略不同重建方法对PET图像质量影响研究,尤其滤波方法对PET脑部图像质量的影响未见报道。2017年欧洲核医学学会颁布的68Ga-DOTA-NOC PET/CT显像指南仅给出注射剂量、显像时间和重建算法,并未给出具体的参考重建参数[12]。至今国内开展68Ga-DOTA-NOC PET/CT显像项目的医疗单位屈指可数,采集协议多基于经验主义,并无统一的指导标准。因此,本研究旨在探讨不同滤波方法对68Ga-DOTA-NOC PET图像和SUV值的影响,以期为68Ga-DOTA-NOC PET/CT脑部采集协议提供参考依据。
1 材料与方法
1.1 模体和病人资料
模体实验采用美国国家电气制造者协会标准的国际电工委员会模体,内含直径10、13、17、22、28、37 mm六个热球,本研究仅在直径37 mm热球内注射68Ga-DOTANOC,模体腔体内放射性活度为5.31 kBq/mL,热球与腔体放射性活度比值为4:1。
临床实验选取2017年12月至2018年8月于南京市第一医院核医学科行68Ga-DOTA-NOC PET/CT显像的39例患者进行回顾性分析,其中男18例,女21例,年龄5~75(50.10±15.33)岁。所有患者均经手术或活检明确病理,包括胃肠胰神经NEN 23例(胰腺NEN 15例,食管NEN 2例,胃NEN 3例,直肠NEN 3例),肺NEN 5例,恶性嗜铬细胞瘤8例,原发灶来源不明NEN 3例。患者体重为17~85(59.70±12.45)kg,身高为 1.06~1.80(1.63±0.12)m,体质量为15.13~30.48(22.12±3.23)kg/m2。本研究获本院伦理委员会批准,患者签署知情同意书。
1.2 图像采集与重建
所有患者检查前无需禁食及控制血糖,68Ga-DOTA-NOC采用德国ITG公司的自动化标记模块在本科室净化实验室完成标记,患者注射剂量为38.00~127.43(71.05±19.19)MBq,每公斤体重注射剂量为0.50~2.99(1.27±0.51)MBq/kg,休息45~60 min后行PET/CT全身加脑部扫描。采用112环数字光导PET/CT(上海联影科技公司uM780)进行数据采集,该款PET/CT包含101920块晶体,轴向视野为30 cm,孔径为70 cm,时间符合窗为4 ns,系统灵敏度为16 cps/kBq,时间分辨率为520 ps。64排128层螺旋CT提供衰减校正:管电压为120 kV,管电流为100 mA,层厚3 mm,螺距为0.5 s。模体和临床患者脑部图像采集视野均为1个床位,时间为10 min和2 min。PET图像重建算法采用OSEM迭代(3次迭代,子集数20)+飞行时间(TOF)技术+点扩散(PSF)技术,图像大小128×128,层厚2.68 mm,滤波方法包括无处理(None)、平滑 1(Smooth1)、平滑 2(Smooth2)、平滑 3(Smooth3)、增强1(Enhance1)和增强2(Enhance2),具体滤波函数选取,见表1。
表1 不同滤波方法选用的滤波函数
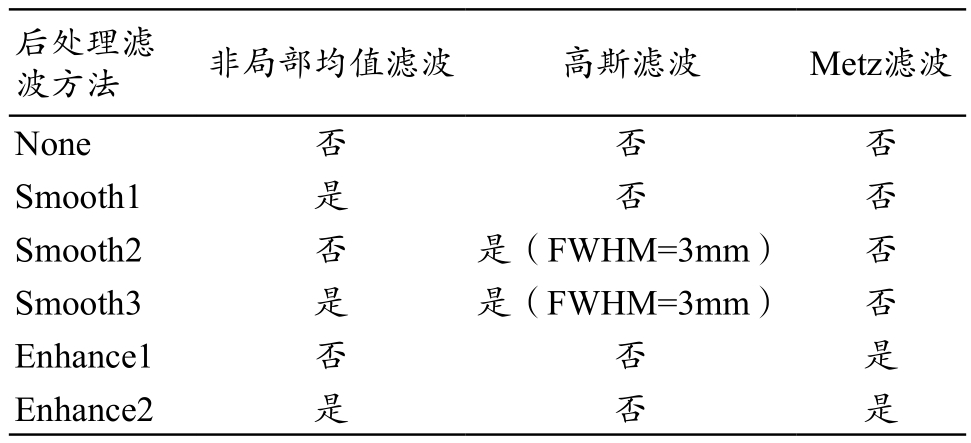
注:FWHM表示高斯半高全宽。
后处理滤波方法 非局部均值滤波 高斯滤波 Metz滤波None否 否 否Smooth1是 否 否Smooth2 否 是(FWHM=3mm) 否Smooth3 是 是(FWHM=3mm) 否Enhance1否 否 是Enhance2是 否 是
1.3 图像分析
模体PET图像质量采用变异系数(CV值),对比度(Contrast)和信噪比(SNR)评估[13],CV值越小,对比度和信噪比越大,表示图像质量越佳,如公式(1)~(3)所示,其中BG代表背景感兴趣区ROI(直径5 mm)的平均放射性计数率,SD代表背景ROI放射性计数率标准差,Signal代表热球ROI内最大计数率。临床PET图像质量采用垂体SUVpeak、SUVmax、SUVmean、和 SUVsd评估 [14],垂体感兴趣区(VOI)由工作站自动勾画。
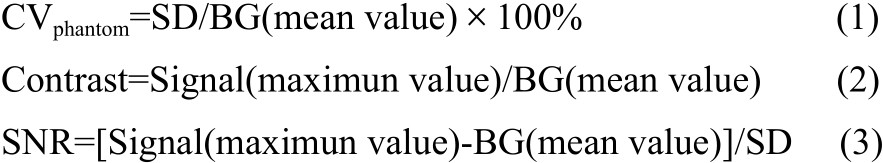
1.4 统计学分析
不同滤波处理对应的模体PET图像CV值、对比度和信噪比采用柱形图分析,临床脑部PET图像中垂体SUVpeak、SUVmax、SUVmean、和SUVsd得分比较采用单因素方差分析。P<0.05时差异具有统计学意义。
2 结果
2.1 每床位不同采集时间对模体PET图像质量的影响
不同滤波方法的模体PET图像,见图1。从图1可以看出,热球均清晰可见,无滤波处理(None)的图像背景噪声最明显;其次是Smooth2、Enhance1和Smooth1,Smooth3和Enhance2对应的图像噪声较低。不同滤波处理对应的CV值、对比度和信噪比,见图2。由图2可知CV值从小到大排序分别是Smooth3(16.57%)、Smooth1(18.61%)、Enhance2(20.00%)、Smooth2(25.98%)、None(30.62%)和Enhance1(33.62%),对比度(Contrast)从大到小排序为 Enhance1(46.09)、Enhance2(44.78)、None(44.27)、Smooth1(43.27)、Smooth2(42.00) 和Smooth3(41.16)。信噪比(SNR)从大到小为Smooth3(242.32)、Smooth1(227.10)、Enhance2(218.88)、Smooth2(157.83)、None(141.31)和 Enhance1(134.13)。
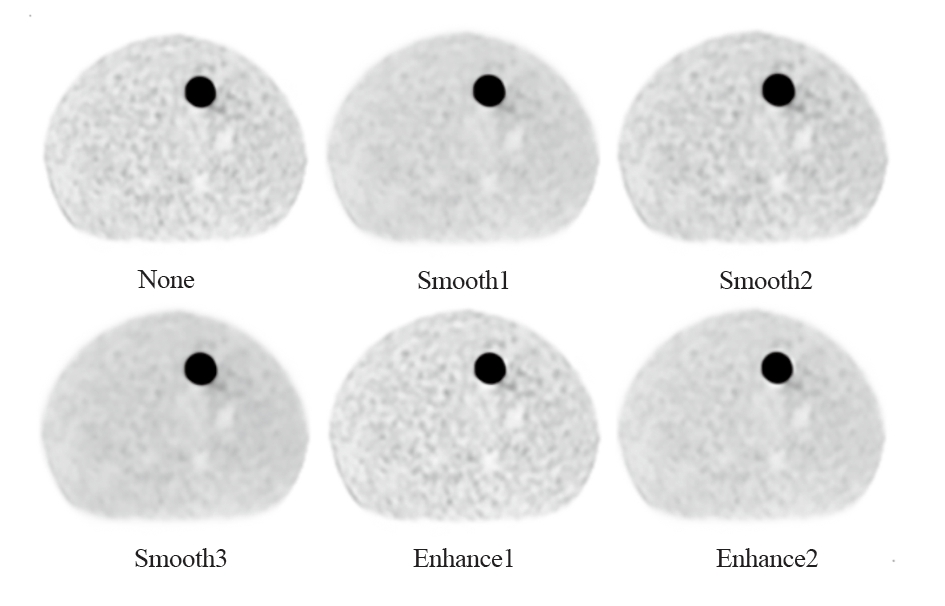
图1 不同滤波方法应的模体PET图像
2.2 不同滤波方法临床PET图像质量和SUV值影响
图3表示不同滤波方法对应的临床脑部PET图像,容易看出不同滤波方法获得的脑部PET图像垂体均清晰可见,其中None和Enhance1获得的脑部PET图像噪声水平相当,图像质量肉眼判读无明显差别,噪声水平次之的是Smooth2、Smooth1和Enhance2,噪声水平最低的是Smooth3。定量分析结果如图4所示:① 垂体SUVpeak从大到小分别为:Enhance1(8.47±5.27)、None(7.78±4.83)、Enhance2(7.66±5.42)、Smooth1(7.17±4.91)、Smooth2(7.05±4.29)和 Smooth3(6.50±4.36);② 垂体 SUVMax从大到小分别为:Enhance1(3.68±3.02)、None(3.63±3.13)、Enhance2(3.51±3.36)、Smooth1(3.37±3.12)、Smooth2(2.63±1.92) 和 Smooth3(2.57±2.11);③ 临 床 脑 部PET图像的垂体SUVmean从大到小分别为:Enhance1(8.47±5.27)、None(7.78±4.83)、Enhance2(7.66±5.42)、Smooth1(7.17±4.91)、Smooth2(7.05±4.29)和 Smooth3(6.50±4.36);④ 垂体SUVsd从大到小分别为:Enhance1(3.68±3.02)、None(3.63±3.13)、Enhance2(3.51±3.36)、Smooth1(3.37±3.12)、Smooth2(2.63±1.92)和 Smooth3(2.57±2.11);单因素方差分析显示,6组之间SUVpeak、SUVMax、SUVmean和SUVsd得分差异均无统计学意义(F=0.7354,P=0.5976;F=1.166,P=0.3270;F=1.725,P=0.1299;F=1.160,P=0.3301)。
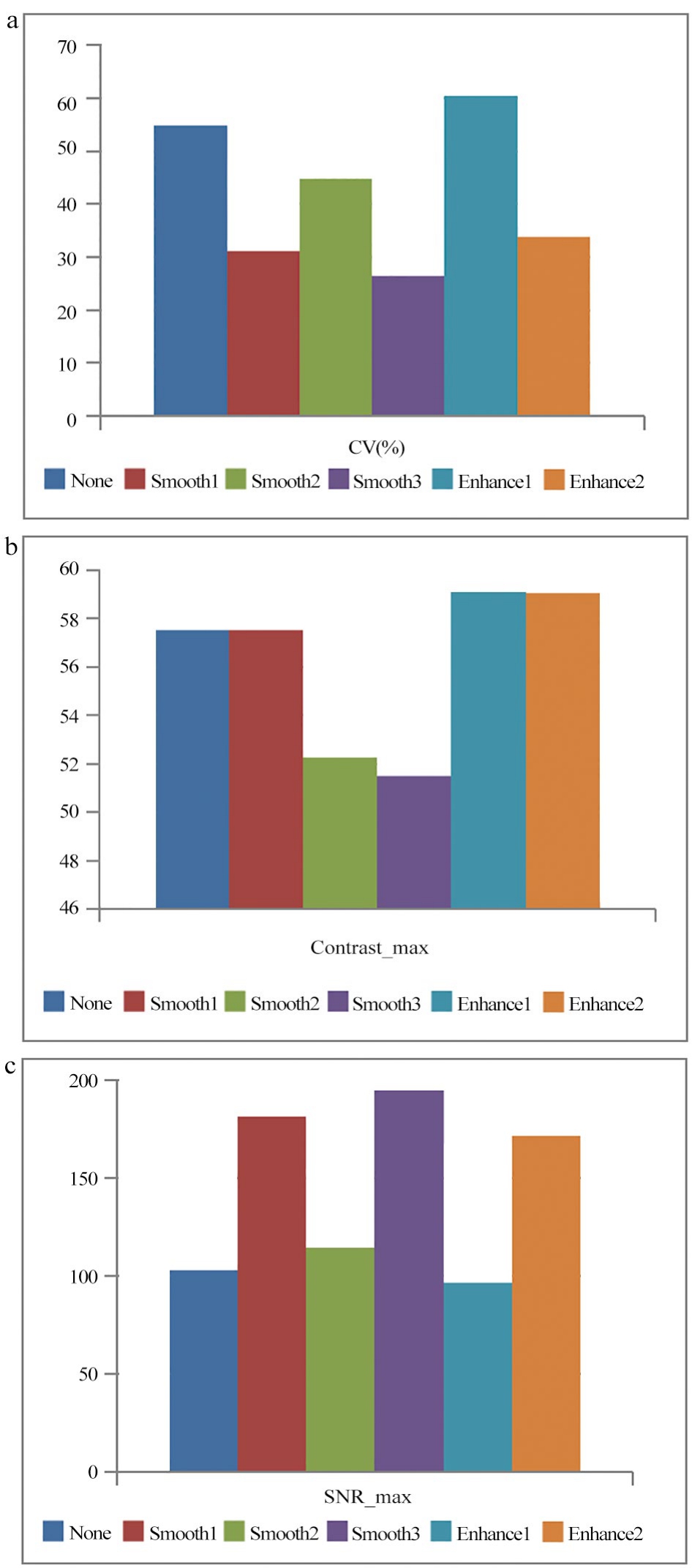
图2 不同滤波方法应的CV值、对比度和信噪比
注:a. 不同滤波处理对应的CV值;b. 不同滤波处理对应的对比度值;c. 不同滤波处理对应的信噪比值。
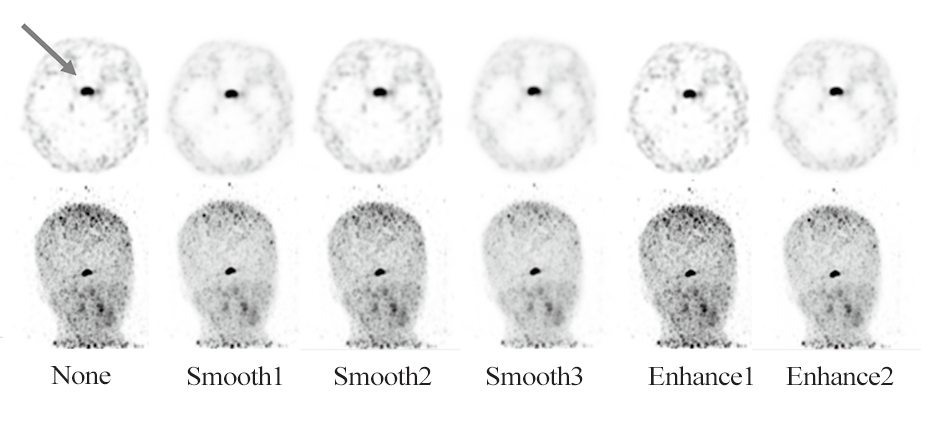
图3 不同滤波方法对应的脑部PET图像
注:胰腺神经内分泌肿瘤患者(女,48岁),箭头代表脑垂体。
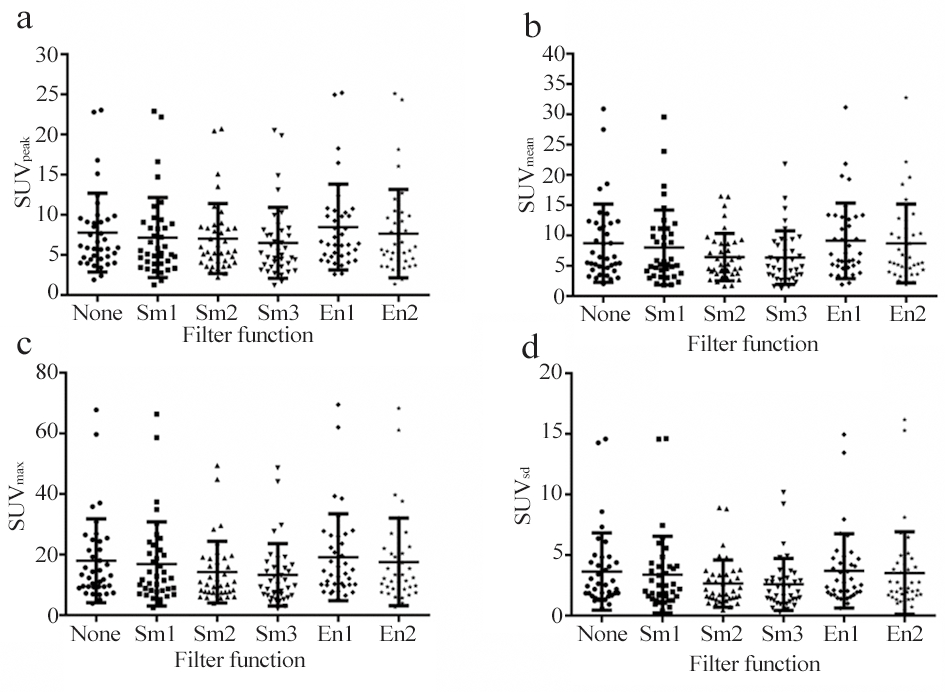
图4 不同滤波方法对应的垂体SUVpeak、SUVmean、SUVmax和SUVsd得分比较
注:None表示无滤波处理,Sm1代表Smooth1,Sm2代表Smooth2,Sm3代表Smooth3,En1代表Enhance1,En2代表Enhance2。
3 讨论
68Ga-DOTA-NOC PET脑部摄取较少,图像易受噪声影响,平滑处理是滤除噪声的有效手段[15-17]。目前上海联影PET/CT装机量较多,还未形成统一的采集协议与重建参数,本款PET系统提供6种滤波方法,包括1种无滤波处理,2种增强处理,3种平滑滤波,本研究探讨不同滤波方法对图像质量以及SUV值的影响。
从视觉上看,无滤波处理获得的图像噪声最显著,Smooth3和Enhance2的图像噪声水平最低,但两者图像质量肉眼分辨不出差别。定量分析显示:① CV值是衡量资料中各观测值变异程度的另一个统计量,可用来表征图像均匀度,模体图像CV值最小的是Smooth3,表明图像背景均匀度最佳;CV值最大的是Enhance1,表明图像背景均匀度最差;② 对比度可表征图像目标与背景的灰度差别,Enhance1对应的对比度最大,表明图像目标最易分辨,Smooth3对应的对比度最小,但模体中热球与背景放射性浓度比值较大,热球均清晰可见,表明对比度对图像质量评估效果不显著;③ 信噪比表征图像信号与噪声的比值,信噪比最大的是Smooth3,最小的是Enhance1,表明Smooth3对噪声抑制能力最强,Enhance1最弱。综上可知,Smooth3的平滑效果最佳,能保证图像高均匀度和信噪比,主要由于Smooth3滤波处理包含非局部均值滤波和高斯滤波函数,平滑噪声性能优越,又保存图像细节;Enhance2图像增强效果最佳,主要得益于Mety滤波函数的高通滤波特性,高频信号和噪声均被保存。
不同滤波方法获得的脑部PET图像均伴随着一定程度噪声,噪点最不显著、图像质量最优的是Smooth3,噪声最显著的是None。定量分析可知,不同滤波方法所得SUV值差异较大,Smooth3对应的垂体SUVpeak、SUVmax、SUVmean和SUVsd在不同滤波方法中均最小,Enhnace1对应的SUV值均最大,但差异均无统计学意义(P>0.05),主要由于Smooth3滤除高频信号和噪声,使得图像整体平滑均匀;Enhnace1增强了垂体信号强度,但同时背景噪声水平也被增强。以Smooth3所得SUV值为参考目标,其他滤波方法所得SUVpeak、SUVmax、SUVmean和SUVsd涨幅分别为8.5%~30.3%,6.6%~43.5%,1.4%~43.8%,2.3%~43.2%。
不同滤波方法的PET脑部图像差异较大,模体实验图像与临床实例图像均显示Smooth3所得PET图像质量最佳,因此本机型PET脑部滤波方法采用Smooth3为宜,为建立和推广国产PET脑部采集协议提供参考依据。
[1] 崔碧霄,卢洁,王曼,等.TOF-PET图像重建技术评价小肿瘤病灶的临床价值[J].医学影像学杂志,2016,26(7):1237-1239.
[2] 王娇,朱佳研,徐文贵,等.比较TOF和PSF PET图像重建技术对肿瘤病灶定量参数的影响[J].中国临床医学影像杂志,2017,28(8):580-583.
[3] Kuhnert G,Boellaard R,Sterzer S,et al.Impact of PET/CT image reconstruction methods and liver uptake normalization strategies on quantitative image analysis[J].Eur J Nucl Med Mol Imaging,2016,43(2):249-258.
[4] Bousse A,Bertolli O,Atkinson D,et al.Maximum-likelihood joint image reconstruction/motion estimation in attenuationcorrected respiratory gated PET/CT using a single attenuation map[J].IEEE Trans Med Imaging,2016,35(1):217-228.
[5] Yoon H J,Yoo J,Kim Y,et al.Enhanced Application of 18F-FDG PET/CT in Bladder Cancer by Adding Early Dynamic Acquisition to a Standard Delayed PET Protocol[J].Clin Nucl Med,2017,42(10):749-755.
[6] Umeda T,Miwa K,Murata T,et al.Optimization of a shorter variable-acquisition time for legs to achieve true whole-body PET/CT images[J].APESM,2017,40(5):1-8.
[7] Lois C,Jakoby BW,Long MJ,et al.An Assessment of the Impact of Incorporating Time-of-Flight (TOF) Information Into Clinical PET/CT Imaging[J].JACC-Cardiovasc Imag,2015,8(8):873-884.
[8] 解小芬,牟甜甜,李珺奇,等.点扩散技术对FDG PET图像质量和SUV的影响[J].中华核医学与分子影像杂志,2017,37(8):475-477.
[9] Molina-Duran F,Dinter D,Schoenahl F,et al.Dependence of image quality on acquisition time for the PET/CT Biograph mCT[J].Zeitschrift Für Medizinische Physik,2014,24(1):73-79.
[10] Aoe S,Miyake M,Kabeya K.A gaussian filter for plate flatness evaluation system with 3-D scanner[J].ISIJ Int,2017,102(9):492-500.
[1 1] Beyer T,Antoch G,Blodgett T,et al.Dual-modality PET/CT imaging: the effect of respiratory motion on combined image quality in clinical oncology[J].EANM,2003,30(4):588-596.
[12] Jena B,Patel P,Sinha GR.An efficient random valued impulse noise suppression technique using artificial neural network and non-local mean filter[J].Int J Rough Sets Data Analy,2018,5(2):148-163.
[13] Suljic A,Tomse P,Jensterle L,et al.The impact of reconstruction algorithms and time of flight information on PET/CT image quality[J].Radiol Oncol,2015,49(3):227-233.
[14] 王渊恺,张光明,韩芳,等.不同采集矩阵与函数重建对SPECT影像质量影响[J].中国医学计算机成像杂志,2011,17(2):164-167.
[15] Akamatsu G,Ishikawa K,Mitsumoto K,et al.Improvement in PET/CT image quality with a combination of point-spread function and time-of-flight in relation to reconstruction parameters[J].J Nucl Med,2012,53(11):1716-1722.
[16] Budäus L,Leyh-Bannurah SR,Salomon G,et al.Initial Experience of 68 Ga-PSMA PET/CT Imaging in High-risk Prostate Cancer Patients Prior to Radical Prostatectomy[J].Eur Urol,2016,69(3):393-396.
[17] Abongwa C,Mott S,Schafer B,et al.Safety and accuracy of 68Ga-DOTATOC PET/CT in children and young adults with solid tumors[J].Am J Nucl Med Mol Imaging,2017,7(5):228-235.
Impact of Different Filter Method on Brain PET Image Quality and Standard Uptake Value