不同b值的磁共振扩散加权成像在评估食管癌同步放化疗疗效中的价值
引言
食管癌是世界范围内最常见的恶性肿瘤之一[1],对于中晚期食管癌患者,放化疗是主要的治疗方法[2]。近年来,磁共振扩散加权成像(Diffusion Weighted Imaging,DWI)在食管癌诊断、分期及放化疗领域方面都处于初步探讨中。扩散敏感系数(b值)是DWI成像技术中的一个重要参数,它影响图像信噪比及表观扩散系数(Apparent Diffusion Coefficient,ADC)测量的准确性和稳定性[3-4]。本文重点研究不同b值下食管癌患者放化疗前后的ADC值是否存在差异,旨在为临床评估及预测食管癌同步放化疗疗效时提供合适的b值。
1 材料与方法
1.1 临床资料
本研究得到医院伦理委员会批准,并获得患者知情同意书。患者纳入标准:① 内镜活检病理证实为食管癌;② 准备在南京鼓楼医院行食管癌同步放化疗且之前未行其他相关治疗;③ 准备通过磁共振评估疗效;④ 无磁共振禁忌症(体内有心脏起搏器、神经刺激器、胰岛素泵及幽闭恐惧症等)。排除标准:① 未完成同步放化疗治疗方案;② 未在规定时间完成磁共振扫描;③ 图像有伪影,影响病灶分析测量;④ 病灶体积小,无法清晰显示。
2015年12月至2017年10月前瞻性收集食管癌患者30例,其中有5例未完成全部磁共振检查(1例患者转院治疗,1例患者治疗期间去世,3例患者放疗结束时未复查磁共振),3例病灶无法测量(2例图像伪影大,1例病灶体积小),最终纳入22例患者入组。其中男15例,女7例,年龄40~81岁(中位数63岁),20例位于颈段或胸上段,2例位于胸中段或胸下段,所有入组患者为鳞状细胞癌。临床分期:Ⅱ期3例,Ⅲ期16例,Ⅳ期3例。
1.2 磁共振检查与方法
全部患者分别在接受同步放化疗前及放化疗结束时行MR检查,MR检查设备采用3.0 T扫描仪(Ingenia 3.0 T;Philips Medical Systems;Best,the Netherlands), 使 用32通道腹部线圈,检查前训练患者规律呼吸,嘱咐患者喝200 mL温水以排除食管中残留物,并告知患者扫描过程中保持平静状态,避免吞咽等动作。检查时患者取仰卧位,头先进,对肿瘤区进行扫描。扫描序列如下:轴位T2WI采用快速自旋回波(Turbo Spin Echo,TSE),TR 1000 msec,TE 80 msec;轴位 T2-weighted 压脂(T2-Weighted Spectral Presaturation Attenuated Inversion Recovery,T2-weighted-SPAIR),TR 1000 ms/585 ms,TE 70 ms; 轴 位DWI成像采用单次激发自旋回波平面成像(Single Shot Diffusion Weighted Echo Planar Imaging,SS-SE-EPI),TR 3000/8000 ms,TE 55 msec;三者的FOV(30 cm)、矩阵(130×159)、层厚(5 mm)及层间距(0.5 mm)一致,并采用呼吸触发门控技术采集原始图像,同时利用化学位移脂肪抑制技术采集DWI原始图像。DWI的弥散敏感梯度分别为b=0~500、0~800及0~1000 sec/mm2,激励次数分别为3、5、3。这3个b值在同一序列一次扫描完成,确保不同b值病灶位置的一致性。
1.3 图像分析
分别采用 b=0~500、0~800 及 0~1000 sec/mm2,将原始数据传到工作站(Extended MR Workspace 2.6.3.4;Philips Medical Systems;Best,the Netherlands)后自动生成 ADC 图。
ADC值计算公式如下:ADC=(lnSI0-lnSI)/(b-b0)
其中,SI0为b0(b0=0 sec/mm2)下的信号强度,SI分别为各个b值(b=500、800及1000 sec/mm2)下的信号强度,ln是自然对数。
感兴趣区(Region of Interest,ROI)选定原则:根据相应的T2WI、T2-weighted-SPAIR及DWI轴位图像,在ADC图上选取肿瘤最大横断面,在实性部分手动勾画圆形或椭圆形ROI,避开病灶边缘及液化坏死区,若放化疗后病灶显示不清时,将ROI放置在治疗前病灶所在位置。分别由两名放射科医生独立测量每例病灶图像的ADC值,包括最大ADC值(ADCmax)、最小ADC值(ADCmin)及平均ADC值(ADCmean),两名医师仅知道病灶位置,但对内镜及治疗等其他情况均未知。以上测量值均取两者平均值以减少误差。
1.4 治疗方案
所有患者均于本院行同步放化疗。放疗方案:全部患者均接受调强适形放疗,采用常规分割体外照射,每次2 Gy,放疗总次数30~33次,总剂量60~66 Gy,视患者一般情况而定。化疗方案:患者在放疗的同时接受同步紫杉醇(50 mg/m2)+奈达铂化疗(25 mg/m2),化疗周期为~6周期。
1.5 疗效评估标准
患者同步放化疗结束后一个月复查CT、上消化道钡剂造影及内镜检查,综合判断治疗疗效。肿瘤消退率=(治疗前长径-治疗结束后一个月长径)/治疗前长径×100%。依据RECIST标准[5],将疗效分为:① 完全缓解(Complete Response,CR)组:肿瘤病灶消失;② 部分缓解(Partial Response,PR)组:肿瘤最大径之和缩小≥30%;③ 疾病稳定(Stable Disease,SD)组:肿瘤最大径之和缩小率介于PR与PD之间;④ 疾病进展(Progress Disease,PD):肿瘤最大径之和增加≥20%或其绝对值增加至少5 mm,若出现新转移灶也视为PD。
1.6 统计学分析
所有数据采用SPSS 22.0统计学软件进行分析,计量资料先行正态性检验,如符合正态分布,参数值用均数±标准差(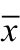 ±s)表示,并采用配对样本t检验比较不同b值下治疗前后病灶的ADC值(包括ADCmax、ADCmin及ADC+)是否存在差异,另外采用独立样本t检验比较不同疗效组间ADC值的差异;如不符合正态分布,则用中位数(四分位数间距)表示,并分别用Wilcoxon和Mann-Whitney U检验分析组间差异。应用受试者工作曲线(Receiver Operating Characteristic,ROC)分析ADC值在鉴别疗效方面的敏感性与特异性,通过约登指数法确定界。以P<0.05为差异有统计学意义。
±s)表示,并采用配对样本t检验比较不同b值下治疗前后病灶的ADC值(包括ADCmax、ADCmin及ADC+)是否存在差异,另外采用独立样本t检验比较不同疗效组间ADC值的差异;如不符合正态分布,则用中位数(四分位数间距)表示,并分别用Wilcoxon和Mann-Whitney U检验分析组间差异。应用受试者工作曲线(Receiver Operating Characteristic,ROC)分析ADC值在鉴别疗效方面的敏感性与特异性,通过约登指数法确定界。以P<0.05为差异有统计学意义。
2 结果
2.1 一般情况
对纳入的22例患者进行疗效评价,CR 13例(59.1%)、PR 9例(40.9%)。不同b值下,治疗前所有病灶在DWI上呈高信号,ADC图上为低信号。治疗结束后,CR组病灶完全消失,ADC图上低信号消失,见图1。PR组残余病灶在DWI上呈浅淡稍高信号,ADC图上为稍低信号,见图2。
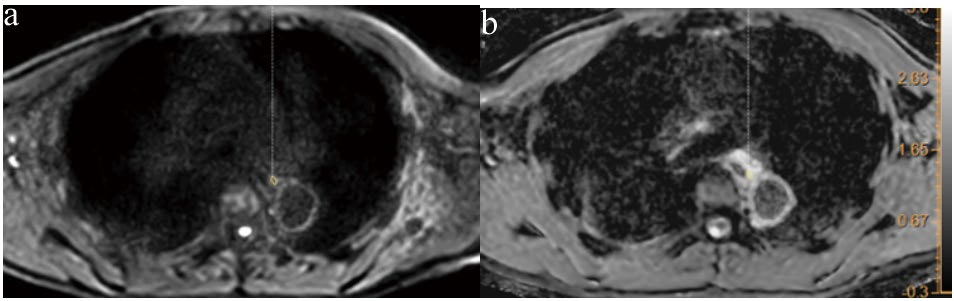
图1 CR组病灶在DWI与ADC图像上的表现
注:a. DWI图像;b. ADC图像。病灶在DWI上完全消失,在ADC图像上表现。
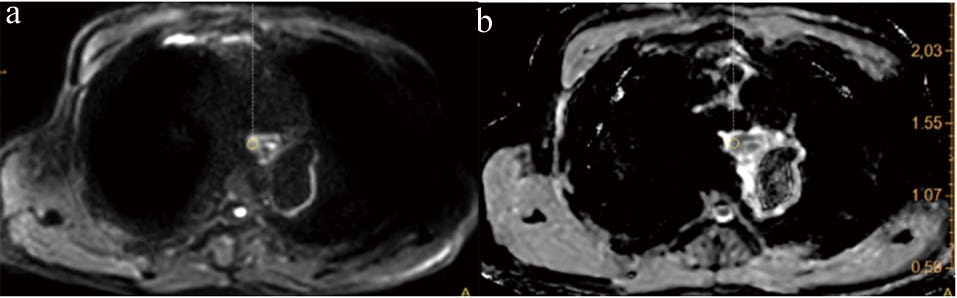
图2 PR组病灶在DWI与ADC图像上的表现
注:a. DWI图像;b. ADC图像。病灶在DWI图像上表现为稍高信号,在ADC图像上表现为稍低信号。
2.2 食管癌治疗前后及不同疗效组间ADC值的变化
所测ADC数据不符合正态分布,所以均用中位数表示。同步放化疗后ADC值较治疗前升高,当b=0~500及0~800 sec/mm2时,治疗后病灶ADC值(ADC2max、ADC2min及ADC2mean)在不同疗效组间均存在显著差异(P<0.05)。而当b值为0~1000 sec/mm2时,病灶的ADC值在不同疗效组间均无显著差异(P>0.05)。具体见表1。
2.3 ADC值预测食管癌同步放化疗疗效的效能
不同b值下各参数指标的ROC曲线分析结果,见表2。
3 讨论
近年来,功能MR发展日新月异,功能序列如DWI,已经被发现可以反映部分肿瘤的内部信息,如脑胶质瘤、肝癌等[6-9],而DWI在食管癌的应用相对较少。不同b值的选择可以影响DWI的图像质量及ADC值,头颈及部分体部肿瘤b值的选择已经有充足的研究,而在食管癌中研究较少,本研究通过不同b值的选择得到的ADC值,来评估食管癌放化疗效果。
不同b值下放疗前后所测量的ADC值的比较,治疗后ADC值较治疗前显著升高。当b=0~500及0~800 sec/mm2时,治疗后病灶ADC值(ADC2max、ADC2min及ADC2mean)在不同疗效组间均存在显著差异,而当b值为0~1000 sec/mm2时,病灶的ADC值在不同疗效组间均无显著差异。b值是DWI的弥散敏感因子,不同脏器选用的最佳b值可能存在差异[9-10],孙应实等[11]认为选择合适的b值既要使病变能够清晰显示且与周围结构可清楚分辨,也要能够有效抑制其他因素对DWI图像的影响,在此基础上尽量选择较高b值,使所测病变的ADC 值与其真实ADC值更贴近。高b值对于病灶的检出很有帮助,但是过大的b值会引起图像信号的衰减,图像质量较差。Wang等[12]以及刘辉等[12]均认为选取b值为0~500 sec/mm2时所得到图像变形和磁敏感伪影严重,图像边缘模糊,不适合作为评价食管癌放疗疗效的指标,与本研究的结果相符。
表1 三种不同b值下食管癌不同疗效组间ADC值的变化(sec/mm2)

注:ADC1max、ADC1min及ADC1mean分别为治疗前行磁共振检查时得到的最大ADC值、最小ADC值及平均ADC值。ADC2max、ADC2min及ADC2mean分别为治疗结束时行磁共振检查时得到的最大ADC值、最小ADC值及平均ADC值。*表示P<0.05(Mann-Whitney U检验)。
参数 b=0~500 b=0~800 b=0~1000 ADC1max(10-3mm2/s)CR 1.87 (0.97) 1.48 (0.63) 1.28 (0.44)PR 1.79 (0.82) 1.14 (0.54) 1.47 (0.49)P 0.794 0.974 0.896 ADC1min(10-3mm2/s)CR 1.00 (0.69) 0.92 (0.52) 0.87 (0.61)PR 1.06 (0.94) 1.08 (0.43) 1.10 (0.52)P 0.324 0.539 0471 ADC1mean(10-3mm2/s)CR 1.34 (0.78) 1.15 (0.54) 1.14 (0.54)PR 1.45 (0.88) 1.26 (0.47) 1.19 (0.55)P 0.262 0.539 0.431 ADC2max(10-3mm2/s)CR 3.44 (1.09) 2.67 (0.39) 2.39 (0.67)PR 2.34 (0.65) 1.95 (0.42) 2.58 (1.13)P 0.007* 0.001* 0.794 ADC2min(10-3mm2/s)CR 2.72 (1.06) 2.34 (0.49) 2.12 (0.74)PR 2.01 (0.54) 1.74 (0.36) 1.99 (0.87)P 0.002* 0.001* 1.000 CR 2.17 (0.91) 2.06 (0.45) 1.80 (0.84)PR 1.63 (0.52) 1.52 (0.33) 1.79 (0.74)P 0.007* 0.004* 0.984 ADC2mean(10-3mm2/s)
本研究显示,b值为0~800 sec/mm2时,ADC值(ADC2max、ADC2min及ADC2mean)在预测食管癌放化疗疗效时的曲线下面积为 0.893、0.829、0.897,较 b值为0~ 500 sec/mm2(0.817、0.817、0.865)大,说明放化疗后,利用b值为800得到的ADC值更能准确客观反映评价疗效。选取小b值时,DWI主要反映组织灌注的变化,所测得的ADC值不太真实。刘辉等[13]认为b值取0~800 s/mm2时所得到的DWI图像及ADC图更利于食管癌放射治疗疗效的评价,与本研究结果相符合。郑向东等[14]与张明等[15]认为b取0~600 sec/mm2时,食管癌病变的DWI图像效果最好、最稳定,能将病灶与组织扩散程度准确地反应出来。刘小静等[16]认为,食管癌DWI的b值选用0~500 sec/mm2,有利于食管癌病灶的检出和显示,与本研究的结果有异,这可能与选用设备的不同及血流灌注影响的差异等有关。且本文选取的食管癌灶均位于颈段,颈段食管癌由于位置特殊,通过手术方法治疗较难;放化疗能够缩小瘤体,提高患者的生存率[17],颈段及胸上段食管移动度不大;如果食管癌灶位于胸中段或胸下段,受呼吸及心脏搏动影响较大,气体的影响也较大,更需要选择较低b值来获得较高的信噪比,满足图像诊断要求。
表2 不同b值下各参数指标的ROC曲线分析结果
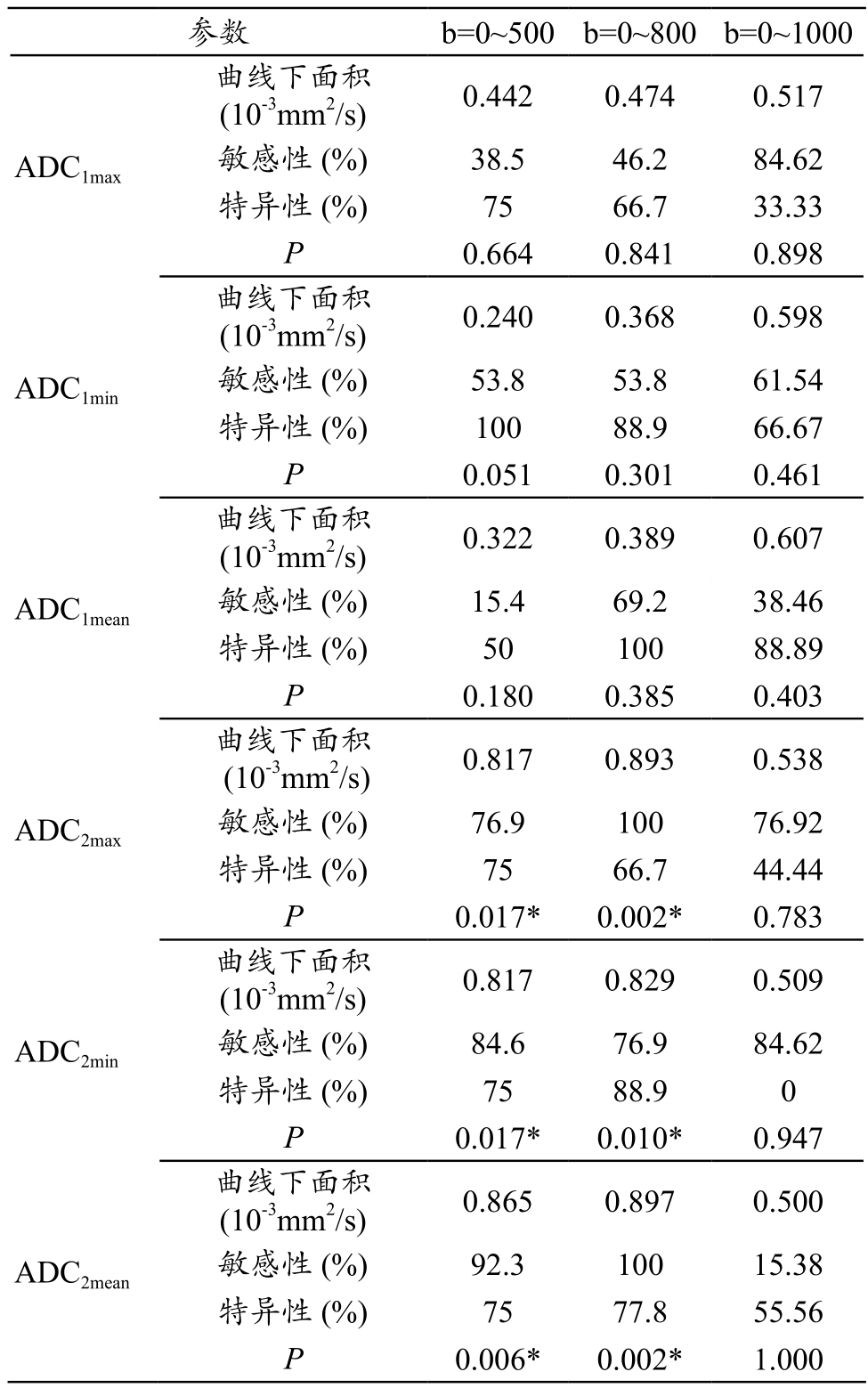
注:*表示P<0.05(ROC曲线分析)。b值区间(b=0~500及0~800 sec/mm2)时,治疗后病灶的ADC值(ADC2min、ADC2mean)的曲线下面积、敏感性、特异性在不同疗效组间存在统计学意义(P<0.05)。而当b值为0~1000 sec/mm2时,病灶的ADC值的曲线下面积、敏感性、特异性在不同疗效组间均无显著差异(P>0.05)。曲线下面积越大,敏感性与客观性越高越能准确客观的反应评价疗效。
参数 b=0~500 b=0~800 b=0~1000曲线下面积(10-3mm2/s) 0.442 0.474 0.517敏感性 (%) 38.5 46.2 84.62特异性 (%) 75 66.7 33.33 P 0.664 0.841 0.898 ADC1max曲线下面积(10-3mm2/s) 0.240 0.368 0.598敏感性 (%) 53.8 53.8 61.54特异性 (%) 100 88.9 66.67 P 0.051 0.301 0.461 ADC1min曲线下面积(10-3mm2/s) 0.322 0.389 0.607敏感性 (%) 15.4 69.2 38.46特异性 (%) 50 100 88.89 P 0.180 0.385 0.403 ADC1mean曲线下面积(10-3mm2/s) 0.817 0.893 0.538 ADC2max 敏感性 (%) 76.9 100 76.92特异性 (%) 75 66.7 44.44 P 0.017* 0.002* 0.783曲线下面积(10-3mm2/s) 0.817 0.829 0.509敏感性 (%) 84.6 76.9 84.62特异性 (%) 75 88.9 0 P 0.017* 0.010* 0.947 ADC2min曲线下面积(10-3mm2/s) 0.865 0.897 0.500敏感性 (%) 92.3 100 15.38特异性 (%) 75 77.8 55.56 P 0.006* 0.002* 1.000 ADC2mean
本研究表明,b值0~500、0~800 sec/mm2时ADC值作为预测食管癌放化疗效果的指标具有可行性。而本研究也存在不足,比如样本数目较少,且病理分型均为鳞状细胞癌,病理类型较为单一,需要收集更多病例来完成进一步的验证。
[1] 李丹.食道癌研究进展[J].吉林中医药,2012,32(9):970-972.
[2] 余小多,林蒙,欧阳汉,等.3.0 T MR扩散加权成像诊断肾脏恶性肿瘤[J].中国医学影像技术,2010,26(3):538-542.
[3] 黄薇园,余永强,钱银锋,等.MR扩散加权成像瘤周水肿区ADC值在脑肿瘤鉴别诊断中的价值[J].临床放射学杂志,2010,20(1):27-30.
[4] Lei J,Tian Y,Zhu SC,et al.Preliminary study of IVIM-DWI and DCE-MRI in early diagnosis of esophageal cancer[J].Eur Rev Med Pharmacol Sci,2015,19(18):3345-3350.
[5] Eisenhauer EA,Therasse P,Bogaerts J,et al.New response evaluation criteria in solid tumours: revised RECIST guideline(version 1.1)[J].Eur J Cancer,2009,45(2):228-247.
[6] 尚全良,肖恩华,贺忠,等.肝癌经导管动脉灌注化疗栓塞术疗效的M R扩散加权成像动态研究[J].中华放射学杂志,2006,(3):235-240.
[7] Lin Y,Li J,Zhang Z,et al.Comparison of intravoxel incoherent motion diffusion-weighted MR imaging and arterial spin labeling MR imaging in gliomas[J].Biomed Res Int,2015,1-10.
[8] 曾治民,廖琴,蔡婧,等.磁共振扩散加权成像及ADC值测量对非小细胞肺癌肺门纵隔淋巴结的鉴别诊断价值[J].中国肿瘤临床,2012,39(10):706-710.
[9] 陈欣,闫锐,康华峰,等.不同扩散梯度因子值的乳腺MR扩散加权成像对比研究[J].中华放射学杂志,2009,43(4):356-359.
[1 0] Shinmoto H,Tamura C,Soga S,et al.An intravoxel incoherent motion diffusion-weighted imaging study of prostate cancer[J].Ajr Am J Roentgenol,2012,199(4):496-500.
[1 1] 孙应实,张晓鹏,唐磊.直肠癌扩散加权成像b值选取及其对直肠癌显示能力的评价[J].中国医学影像技术,2005 21(12):1839-1843.
[12] Wang L,Liu L,Han C,et al.The diffusion-weighted magnetic resonance imaging (DWI) predicts the early response of esophageal squamous cell carcinoma to concurrent chemoradiotherapy[J].Radiother Oncol,2016,121(2):246-251.
[13] 刘辉,时高峰,邵娴,等.磁共振弥散加权成像在食管癌放疗疗效中的应用以及评价价值[J].中国现代医学杂志,2014,24(22):57-61.
[14] 郑向东,李天然,吴贵成,等.3.0 T MR弥散加权成像对食管癌放化疗的疗效评价[J].功能与分子医学影像学杂志,2015,(1):579-582.
[15] 张明,吴献华.磁共振弥散加权成像对食管癌患者同期放化疗前后表观弥散系数以及病变长度的影响[J].中国临床研究,2016,29(3):389-391.
[16] 刘小静,周胜利,陈伟,等.磁共振扩散加权成像在食管癌显示及恶性程度评估中的应用[J].临床放射学杂志,2016,(5):763-767.
[1 7] Baba Y,Watanabe M,Baba H.A review of the alterations in DNA methylation in esophageal squamous cell carcinoma[J].Surgery Today,2013,43(12):1355-1364.
Value of Diffusion-Weighted Magnetic Resonance Imaging With Different b Values in Evaluating the Efficacy of Synchronous Radiotherapy and Chemotherapy for Esophageal Cancer