利用kV级CBCT识别标记物研究
引言
现今,精确放疗已成为业内主流技术[1-2],图像引导放疗(Image Guide Radiotherapy,IGRT)能有效提高放疗精度[3]。多数放疗单位采用的是治疗前的图像引导,例如拍摄电子射野影像系统(Electronic Portal Imaging Device,EPID)平片和锥形束CT(Cone Beam CT,CBCT)扫描,并将结果同计划系统数据进行比较,从而修正摆位误差[4]。
未来IGRT的趋势是治疗中实时修正误差。这可通过实时定位靶区中预埋的标记物来获取靶区位置信息,从而反馈到治疗设备并实时调整其参数[1]。但治疗中如何实时获取标记物三维空间坐标尚未得到完全解决。
胡逸民[5]提出了双源加速器设想,可以解决之前的难题。该设想起初参考了双源CT的设计思路[6],即两个放射源安装在两个机头中并呈正交角度,类似双源CT球管设置,在治疗过程中一个源出束治疗,一个源配合实现治疗过程中的实时验证。本实验所利用的算法即是建立在该设想模型基础上的。之前的研究证明了在双源加速器模型基础上,利用两张EPID平片和所开发算法实时定位模体中内植标记物三维空间坐标的可行性。随着设备软硬件水平的发展和进步,胡逸民[5]进一步完善了双源加速器的设计思路,即尽量缩小两个源的角度间隔,使得两个源(治疗源和验证源)同时处于一个加速器机头内且围绕同一个治疗等中心,并处于相同旋转轨道上。验证源同治疗源间隔一定角度,射线中心轴同治疗源射线中心轴在治疗等中心处相交,如图1所示。该设想应用关键在于两个源之间最小角度间隔。
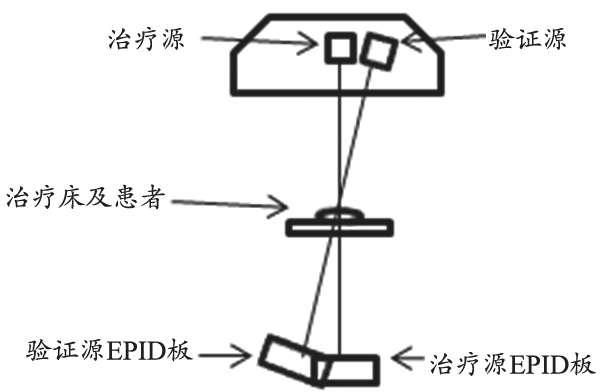
图1 双源加速器构想
本实验利用kV级CBCT扫描内植了标记物的模体,获得0°到359.96°球管(两个不同角度的球管位置代表了间隔的两个源)所拍摄的图像集合,并利用金球投影位置自动跟踪算法处理图像集合中任意两张图像,以期获得最小识别角度间隔。
1 材料和方法
1.1 试验器材
医科达Synergy Platform加速器及所载kV级CBCT系统(瑞典医科达公司生产);Random硅胶仿真模体盆腔段横断层8片(美国瓦里安公司生产);Visicoil helical线性金标记物[7]4枚,圆柱状,直径0.5 mm,长度5 mm三枚作为研究对象标记物,直径1 mm,长度5 mm一枚作为参考中心(比利时IBA公司生产)。本文所用试验器材,见图2。
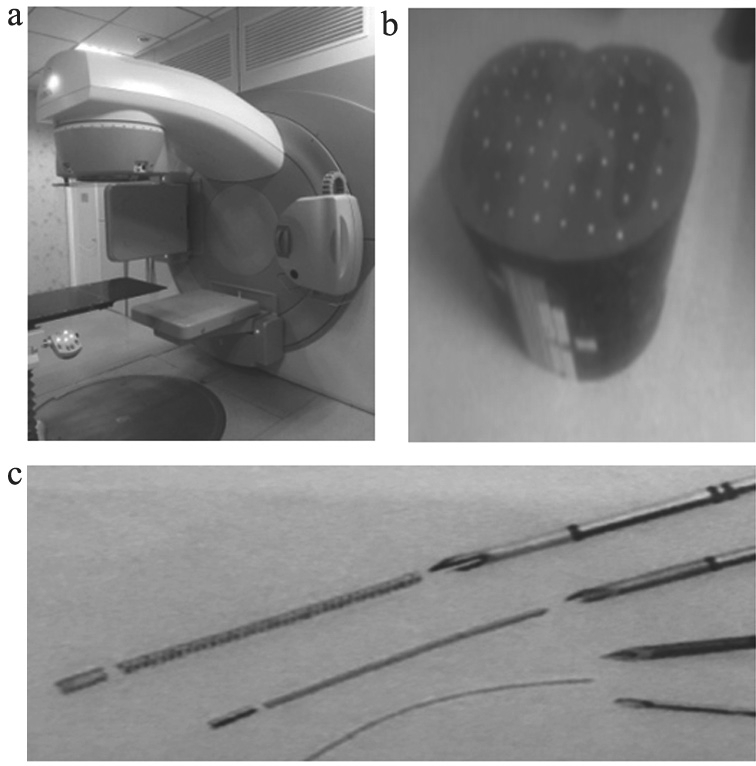
图2 本文所有试验器材实物图
注:a. 医科达Synergy Platform加速器及其所载CBCT成像设备;b. Random假体盆腔段;c. Visicoil金标记物。
1.2 试验方法
1.2.1 安装模体
截取Random假体盆腔段,将标记为A、B、C的三枚金标记物内植于模体膀胱部位不同层面中,任意两枚标记物之间距离大于15 mm。
1.2.2 确定标记物真实三维空间坐标
首先本实验将参考中心置于模体膀胱中间,同其他三枚标记物处于不同层面的固定标识位置处,然后使用最小刻度为0.01 mm的带表游标卡尺测量三枚标记物同固定标识处标记物实际三维距离(X、Y、Z方向,同加速器方向正负保持一致),之后在模体表面利用十字标记标识参考点,最后封装模体。之后使用大孔径CT对模体进行定位扫描,除膀胱部位外盆腔其他区域扫描层厚5 mm,膀胱区域3 mm,并将模体定位图像上传至计划系统。
最后,将模拟治疗等中心设置于参考中心处,使用XiO放疗计划系统,利用measure功能测量和记录重建后三枚标记物3D质心相对等中心(0,0,0)的真实三维空间坐标,并同带表游标卡尺实际测量数值相比较防止出现误差(误差允许范围±5 mm)。
1.2.3 设置kV级CBCT参数
CBCT球管到探测器距离设置为153 cm,球管到等中心距离设置为100 cm。选择快速扫描模式(机架旋转速度为180 deg/min),管电压为120 kV,总管电流为1689.6 mAs,kV板位置为Medium,FOV选择M10,kV滤过板选择F1。CBCT旋转一周共获得588幅投影图像,即从球管处于270°位置开始,约每0.52°获取一幅投影图像,并将角度标注于每幅投影图像上面,图3展示了球管于0°、60°和90°三个角度平片。

图3 kV级CBCT所获得不同球管角度平片
注:a为0°时刻;b为60°时刻;c为90°时刻。
1.2.4 图像处理
于图像集合中任意抽取两幅不同角度的投影图像,利用金球投影位置自动跟踪算法进行图像处理,并获得标记物的三维空间坐标。
为了便于表示,本实验将球管于0°所获取的投影图像设置为所有抽取的投影图像组合中的第一幅,即使用0°投影图像同其他587幅图像组成587个图像组合,并进行处理。每个图像组合会获得三枚内植标记物的三维空间坐标,共会获得587组,1761个结果。
1.2.5 统计学分析
将历次所选取图像组合的处理结果,即每个标记物的三维空间坐标同真实结果相比较,计算三个方向上位移d值,共获得3组1761个结果。并于每组结果中,找到差异绝对值最大的结果,同时确定第二幅投影图像的拍摄角度(第一幅均为0°)。
2 结果
通过带表游标卡尺和XiO放疗计划系统测量计算出的三枚标记物A、B、C的真实三维空间坐标分别为:A:(5.71,2.16,-2.51);B :(0.41,1.23,1.66);C :(1.48,-2.87,0.03)和 A :(5.75,2.19,-2.56);B :(0.46,1.28,1.69);C:(1.52,-2.91,0.01),在误差允许范围(±5 mm)之内,取平均值为 A:(5.73,2.18,-2.54);B:(0.44,1.26,1.68);C :(1.50,-2.89,0.02),单位为 cm。
本实验共获得了三组1761个结果,由于所编制算法逻辑以及设备精度限制、kV级CBCT平片图像质量限制,设置容差为±5 mm,即误差在±5 mm以内即认为标记物识别成功。为了方便展示,仅列出了0°同0.52°到13°投影图像配对组相对真实值在三个方向上位移d绝对值,见表1。二者d值三维空间向量随角度变化趋势如图4所示。
表1 0°同0.52°到13°投影图像配对组的结果三个方向上相对真实位移d绝对值(cm)
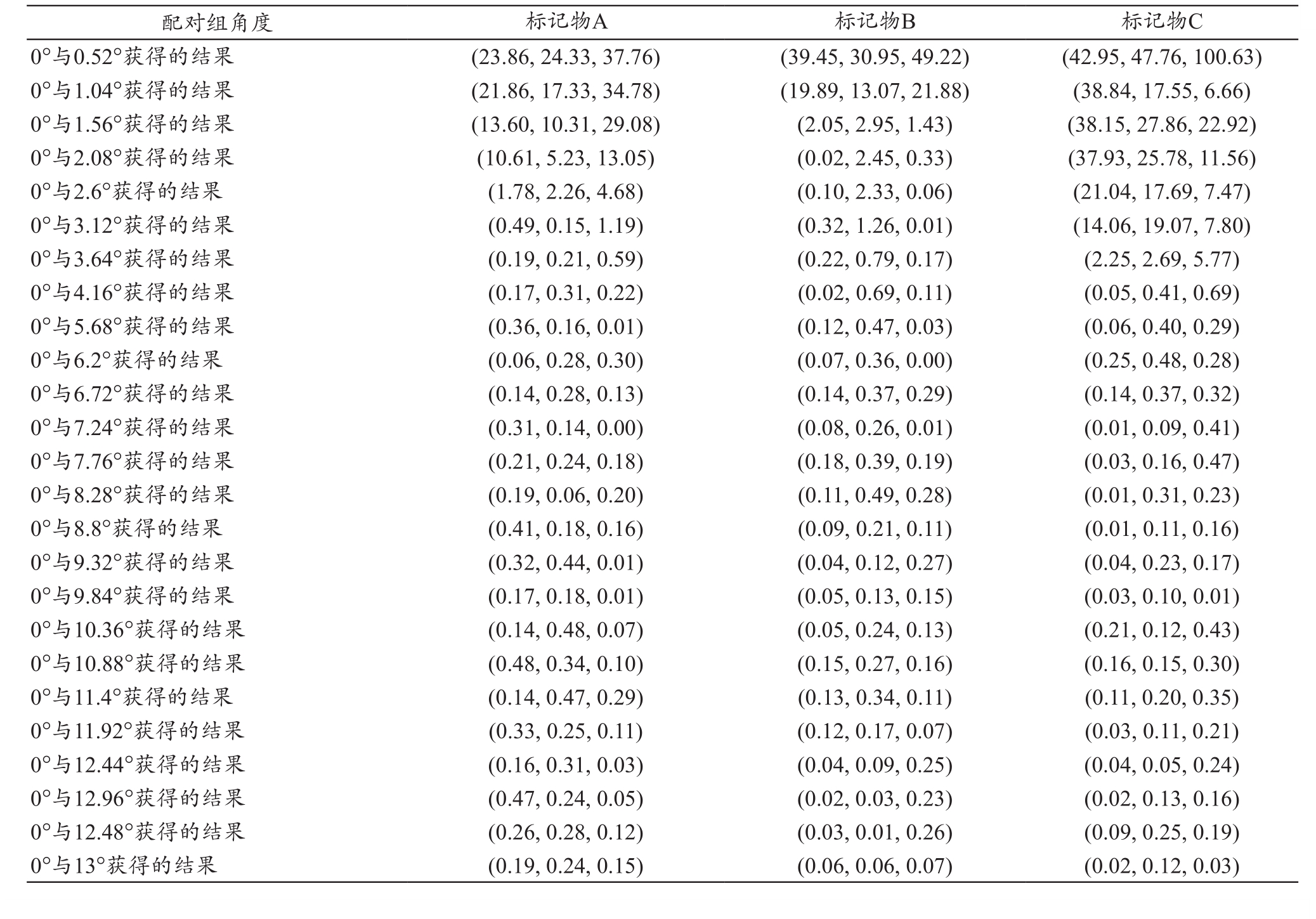
配对组角度 标记物A 标记物B 标记物C 0°与0.52°获得的结果 (23.86, 24.33, 37.76) (39.45, 30.95, 49.22) (42.95, 47.76, 100.63)0°与1.04°获得的结果 (21.86, 17.33, 34.78) (19.89, 13.07, 21.88) (38.84, 17.55, 6.66)0°与1.56°获得的结果 (13.60, 10.31, 29.08) (2.05, 2.95, 1.43) (38.15, 27.86, 22.92)0°与2.08°获得的结果 (10.61, 5.23, 13.05) (0.02, 2.45, 0.33) (37.93, 25.78, 11.56)0°与2.6°获得的结果 (1.78, 2.26, 4.68) (0.10, 2.33, 0.06) (21.04, 17.69, 7.47)0°与3.12°获得的结果 (0.49, 0.15, 1.19) (0.32, 1.26, 0.01) (14.06, 19.07, 7.80)0°与3.64°获得的结果 (0.19, 0.21, 0.59) (0.22, 0.79, 0.17) (2.25, 2.69, 5.77)0°与4.16°获得的结果 (0.17, 0.31, 0.22) (0.02, 0.69, 0.11) (0.05, 0.41, 0.69)0°与5.68°获得的结果 (0.36, 0.16, 0.01) (0.12, 0.47, 0.03) (0.06, 0.40, 0.29)0°与6.2°获得的结果 (0.06, 0.28, 0.30) (0.07, 0.36, 0.00) (0.25, 0.48, 0.28)0°与6.72°获得的结果 (0.14, 0.28, 0.13) (0.14, 0.37, 0.29) (0.14, 0.37, 0.32)0°与7.24°获得的结果 (0.31, 0.14, 0.00) (0.08, 0.26, 0.01) (0.01, 0.09, 0.41)0°与7.76°获得的结果 (0.21, 0.24, 0.18) (0.18, 0.39, 0.19) (0.03, 0.16, 0.47)0°与8.28°获得的结果 (0.19, 0.06, 0.20) (0.11, 0.49, 0.28) (0.01, 0.31, 0.23)0°与8.8°获得的结果 (0.41, 0.18, 0.16) (0.09, 0.21, 0.11) (0.01, 0.11, 0.16)0°与9.32°获得的结果 (0.32, 0.44, 0.01) (0.04, 0.12, 0.27) (0.04, 0.23, 0.17)0°与9.84°获得的结果 (0.17, 0.18, 0.01) (0.05, 0.13, 0.15) (0.03, 0.10, 0.01)0°与10.36°获得的结果 (0.14, 0.48, 0.07) (0.05, 0.24, 0.13) (0.21, 0.12, 0.43)0°与10.88°获得的结果 (0.48, 0.34, 0.10) (0.15, 0.27, 0.16) (0.16, 0.15, 0.30)0°与11.4°获得的结果 (0.14, 0.47, 0.29) (0.13, 0.34, 0.11) (0.11, 0.20, 0.35)0°与11.92°获得的结果 (0.33, 0.25, 0.11) (0.12, 0.17, 0.07) (0.03, 0.11, 0.21)0°与12.44°获得的结果 (0.16, 0.31, 0.03) (0.04, 0.09, 0.25) (0.04, 0.05, 0.24)0°与12.96°获得的结果 (0.47, 0.24, 0.05) (0.02, 0.03, 0.23) (0.02, 0.13, 0.16)0°与12.48°获得的结果 (0.26, 0.28, 0.12) (0.03, 0.01, 0.26) (0.09, 0.25, 0.19)0°与13°获得的结果 (0.19, 0.24, 0.15) (0.06, 0.06, 0.07) (0.02, 0.12, 0.03)
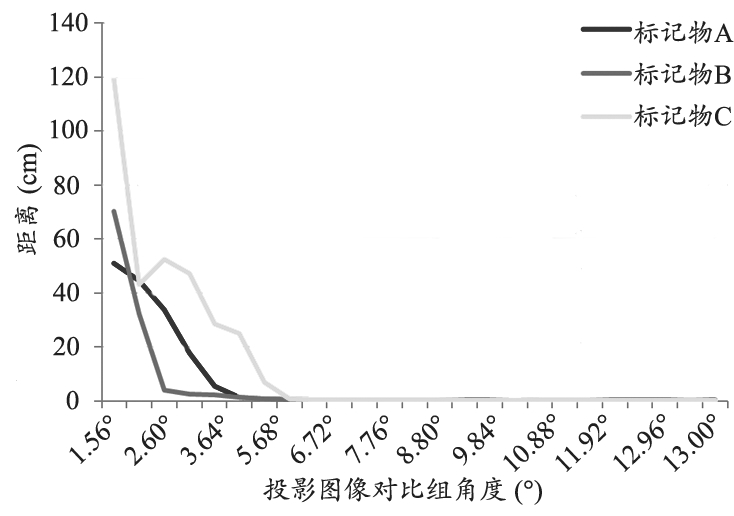
图4 以0°为首幅图像的对比组同真实值三维空间向量随角度变化趋势
另外,为了保证其他角度结果的可信度,试验又以90°为第一幅图像,同0.52°到13°依次组成配对组,同真实结果之间三维空间向量随角度变化趋势如图5所示。
通过以上结果可以发现,当第二幅投影图像拍摄角度为4.16°时,无论首幅图像为0°还是90°,三枚标记物三维空间坐标同其真实值相差均不大,当第二幅投影图像拍摄角度为3.64°时,A、B两枚标记物三维空间坐标同其真实值差异处于可以接受范围内,而C标记物差异较大。本实验以三枚标记物均准确定位为标准,故标记物最小识别角度为4.16°。
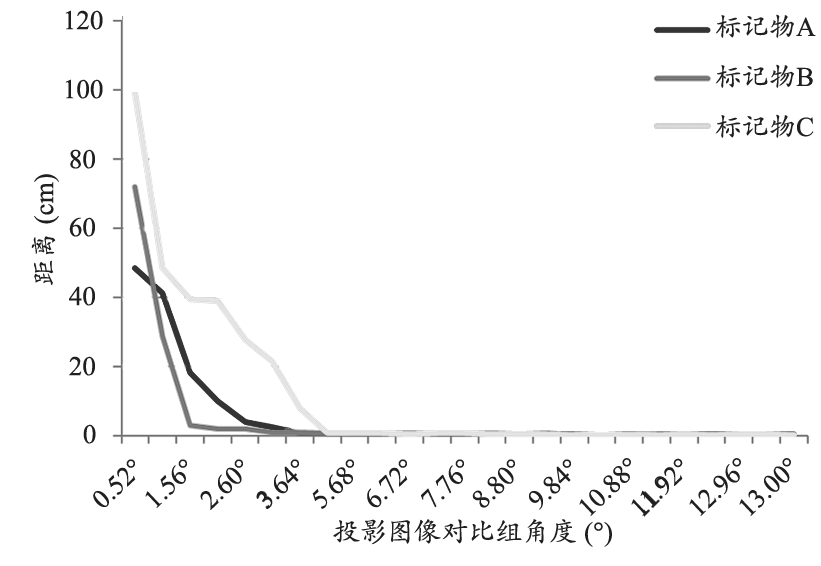
图5 以90°为首幅图像的对比组同真实值值三维空间向量随角度变化趋势
3 分析与讨论
本实验是在双源加速器设想基础上进行的。本实验提供给了设计者最小的源角度间隔数据,从而提高实现治疗中的实时验证的可行性。
之前研究解决了算法问题[1],在Park等[8]所编算法基础上,利用Matlab编程软件编制了算法,处理两张不同角度EPID所获得的MV级图像,采用相同试验方法,计算获得三枚标记物于三维空间坐标。事实证明,之前所编算法在处理两张不同角度kV级CBCT所获得的kV级图像时,表现也比较出色。另外,本试验参考了其他文献[9-13],在原有基础上缩减了图像读取和整合算法过程,优化了亮斑突出和边缘锐化算法结构,增加了算法处理kV级图像所必须的程序,从而使其对kV级图像的处理更加完美。另外,本实验算法阈值参数要求标记物之间距离必须大于15 mm,且处于不同层面中。从可视性上来说,标记物距离小于15 mm可能会导致标记物在某些角度图像上发生重叠,从而对计算结果产生严重影响。例如在Bernchou等[14]的试验中,有两例患者标记物之间距离小于15 mm,最终导致错误的标记物追踪;有一例患者两枚标记物被放置于同一层面上,导致24%的追踪失败率。
本实验存在一些未解决的问题。首先,是双源如何同时工作的问题,对此,胡逸民教授提出了旋转源的设想,目前专利正在申请中,有望解决治疗中如何同时产生治疗射线和验证射线的问题;其次,是EPID探测板的问题,由于试验中两个源间隔最小角度为4.16°,因此两块对应的EPID探测板的角度间隔角度非常小,如何安置两块EPID探测板尚未有解决思路。本实验设想是否可以采用一块曲面EPID探测板来实现同时接收两个源的射线,并产生两套相关EPID图像,但板面中心距离太近是否会造成重叠、失真或干扰尚不得知,仍需同加速器生产厂商联系沟通。
本实验所利用的算法和软件系统、设备水平还有待于进一步提高。算法方面,程序计算和图像处理速度有待提高,从而防止在治疗过程中可能会出现的图像处理滞后现象;软件方面,计划系统、CBCT系统软件需要由3D向4D跨越,Fujii等[15]实现了4D-CBCT软件的临床应用,为本实验指明了优化方向;硬件方面,kV级CBCT的图像分辨率高于MV级设备所拍摄的图像[16],而双源加速器设想是治疗过程中使用MV级射线获取图像信息。如何提高MV级图像的分辨率和图像处理能力也是关乎实现实时验证的关键。本实验结果可以接受且能够应用于临床实践当中,不过仍需提高软硬件水平从而获得更精确结果。
4 结论
在双源加速器设想基础上,之前试验所开发的算法对CBCT图像的处理结果可以接受,计算获得的两个加速器源最小间隔角度为4.16°,具有临床实际使用价值。但仍存在一些尚未解决的难题,例如EPID探测板的安置,以及软硬件水平,未来试验目标是同加速器厂家联系沟通,并提升算法及其他软件水平,从而获得更好实验结果并争取早日应用到临床中。
[1] 田龙,李明辉,胡逸民.利用EPID图像金球位置自动跟踪算法研究[J].中国医学物理学杂志,2014,31(4):5038-5042.
[2] 田龙,席强,赵鑫,等.膀胱癌图像引导放疗中基于软组织灰度值与基于内植标记物的锥形束CT校准比较[J].中国医学物理学杂志,2018,35(1):31-35.
[3] 钟秋子,李高峰,修霞,等.前列腺癌根治术后IGRT疗效分析[J].中华放射肿瘤学杂志,2016,25(6):583-587.
[4] 容贤冰,邓烨.CBCT和EPID在体部肿瘤放疗摆位的对比研究[J].影像研究与医学应用, 2017,1(11):48-49.
[5] 胡逸民.肿瘤放射物理学[M].北京:原子能出版社,2003.
[6] 张宗军,卢光明.双源CT及其临床应用[J].医学研究生学报,2007,4(20):416-418.
[7] 田龙,席强,宋晓.膀胱CBCT图像中标记物选取的研究[J].癌症进展,2016,10(14):4738-4744.
[8] Park SJ,Ionascu D,Hacker F,et al.Automatic marker detection and 3D position reconstruction using cine EPID images for SBRT verification[J].Med Phy,2009,36(10):4536-4546.
[9] Nederveen A,Lagendijk J,Hofman P.Detection offiducial gold markers for automatic on-line megavoltage position verification using a marker extraction kernel (MEK)[J].Int J Radiat Oncol Biol Phys,2000,47(5):1435-1442.
[10] Mao W,Wiersma RD,Xing L.Fast internal marker tracking algorithm for onboard MV and kV imaging systems[J].Med Phys,2008,35(5):1942-1949.
[11] Mao W,Riaz N,Lee L,et al.A fiducial detection algorithm for real-time image guided IMRT based on simultaneous MV and kV imaging[J].Med Phys,2008,35(8):3554-3564.
[12] Keall PJ,Todor AD,Vedam SS,et al.On the use of EPID-based implanted marker tracking for 4D radiotherapy[J].Med Phys,2004,31(12):3492-3499.
[13] Wiersma R,Mao W,Riaz N,et al.SU-DD-A3-02: Real-time tracking of implantedfiducial markers using combined KV and MV imaging[J].Med Phys,2008,35(6Part2):2634-2634.
[14] Bernchou U,Agergaard SN,Brink C.Radiopaque marker motion during pre-treatment CBCT as a predictor of intra-fractional prostate movement[J].Acta Oncol,2013,52(6):1168-1174.
[15] Fujii T,Matsuura T,Takao S,et al.SU-F-I-11: Software development for 4D-CBCT research of real-time-image gated spot scanning proton therapy[J].Med Phys,2016,43(6):3389.
[16] Held M,Cremers F,Sneed PK,et al.Assessment of image quality and dose calculation accuracy on kV CBCT, MV CBCT, and MV CT images for urgent palliative radiotherapy treatments[J].J Appl Clin Med Phys,2016,17(2):279-290.
Study on Marker Recognition Using kV CBCT