磁锚定技术辅助内镜下胃空肠吻合
引言
我国是消化道恶性疾病高发国家,消化系统肿瘤是中国人群重要的癌症负担。消化道常见肿瘤如远端胃癌、十二指肠癌及壶腹周围癌中晚期患者常合并有恶性胃十二指肠输出道梗阻(Malignant Gastroduodenal Outlet Obstruction,MGOO)。多学科诊疗模式(Multi-Disciplinary Treatment,MDT)的开展使这类患者生存期得到明显延长,但仍有15%~20%的晚期MGOO患者由于肿瘤在消化道内的生长,导致胃肠内容物(食糜、胃液、胆汁)不能顺利通过梗阻部位,造成上腹部饱胀、恶心呕吐、无法经口进食等诸多问题,患者生存质量大幅度下降[1]。因此,解决MGOO造成的患者无法经口进食问题在临床上显得尤为重要[2]。
目前针对MGOO患者的治疗方法主要包括外科手术和内镜治疗,其中外科手术因创伤较大,治疗效果有限,逐渐被内镜治疗取代。而内镜下支架植入仅适用于轻度梗阻的患者,对重度MGOO患者应用受限。内镜下胃肠吻合能有效解决重度MGOO患者经口进食的问题,但其操作难度大、内镜技术水平要求高,在世界范围内仅有极少数消化内镜中心开展。分析其原因在于内镜下无法精准地对处于游离状态的胃肠道进行穿刺。胃肠道的游离状态使内镜下胃肠穿刺缺乏靶向性和安全性。十二指肠双球囊封堵固定装置可在一定程度上可对穿刺部位的肠道起到一定的约束作用[3],但胃肠道游离状态及胃肠穿刺的靶向性等根本问题仍无法得到解决,内镜下胃肠吻合的技术瓶颈依然存在。因此,探索一种既能给内镜下的胃肠穿刺提供靶向性,又能实现胃肠贴附以提高穿刺安全性的装置和方法具有重要临床意义。
基于磁体同极相斥、异极相吸原理和特殊形式的非接触性磁场力特点的磁外科(Magnetic Surgery,MS)技术发展迅速,并诞生了一系列颠覆性的临床新技术。磁锚定技术(Magnetic Anchor Technique,MAT)是磁外科学临床应用核心技术之一,它利用磁体与磁体或磁体与顺磁性物质之间的磁场吸引力,使一个磁体对另一磁体或顺磁性物质进行非接触性的空间锚定,其中作为MAT中主动部分的磁体称为锚定磁体(Anchor Magnet,AM),充当被动吸引角色的磁体或顺磁性物体称为靶磁体(Target Magnet,TM)[4]。MAT目前在临床上主要用于减戳卡腔镜手术[5-8]、ESD术[9-11]中。本文在团队前期MS研究基础上,首次提出了消化道腔内磁锚定穿刺理念,并设计了相关操作组件,拟用于辅助内镜下胃肠穿刺吻合,现介绍如下。
1 设计思路
内镜下胃肠吻合的关键操作技术是胃肠穿刺通道的建立。胃肠道在腹腔内处于游离状态,这导致穿刺过程中胃壁、肠壁受力后会发生滑动和移位,使穿刺缺乏靶向性。借助MAT基本原理和方法,内镜辅助下在胃内放置AM,在肠道内通过导管推注TM(液磁),在磁场力作用下AM和TM相吸,使欲穿刺部位的肠壁和胃壁紧密贴合在一起(图1)。这样可提高穿刺的可靠性,同时,AM中央的穿刺导管可使穿刺点位于相贴合的胃壁和肠壁的中心部位,增加了穿刺的靶向性。
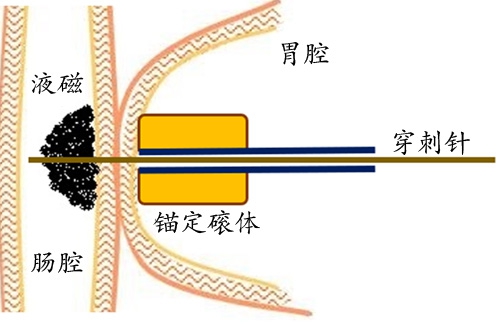
图1 磁锚定胃肠穿刺示意图
2 基本设计
2.1 AM的设计
本设计中AM属于主动施力部分,且要为胃肠穿刺针提供安全的穿刺靶点,因此,AM的基本结构设计为带有穿刺引导管的圆柱状电磁装置。该电磁装置需经口、食管进入胃内,因此,其直径限制在15~20 mm之间。其基本结构如图2所示。其中电磁体正中有通孔,穿刺导管的一端伸入电磁体的通孔内并牢固固定,电磁体引线紧贴穿刺导管牢固黏附固定。穿刺导管可采用造影导管,其作用一方面方便电磁体的置入,另一方面供胃肠穿刺针通过,可对胃肠穿刺针起引导作用。
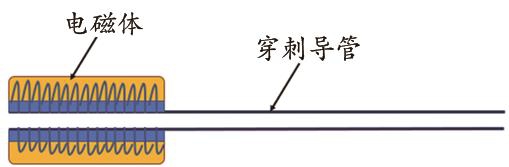
图2 AM的结构模式图
2.2 TM的设计
在严重的胃十二指肠输出口梗阻患者中,常规的圆环形、椭圆形、甚至长条形磁体也难以通过肠道狭窄段,往往仅允许细小的导管通过。因此我们采用了将液磁作为TM的方案,液磁兼备液体的流动性和磁体的特性。当导管放置到肠道后,可通过导管推注液磁。液磁由磁性纳米颗粒、液体和表面活性剂三部分组成,其磁性主要来源于磁性纳米颗粒。近年来研究显示纳米Mn-Zn铁氧体(MnxZn1-xFe2O4)具有良好的稳定性、生物相容性、毒性小且合成加工工艺成熟[12]等特点,从而被广泛应用。
2.3 配套组件
斑马导丝、液磁输送导管、胃肠穿刺钢针、胃肠穿刺道扩张球囊及双蘑菇头胃肠吻合支架均为临床上常见的医疗器械,可直接使用。
3 操作步骤
MAT辅助内镜下胃肠穿刺步骤如下(图3):① 经口下胃镜至梗阻部位近端,经活检孔置入斑马导丝,X线监测下,推送导丝使其穿过梗阻部位,导丝头端到达空肠起始段,沿斑马导丝经胃镜活检孔送入液磁输送导管,使其头端到达梗阻部位远端;② X线监测下保持液磁输送导管头端位置不变,缓慢退出胃镜及斑马导丝;③ 胃镜辅助下利用固定在电磁铁一端的穿刺导管将电磁体送至胃体部,经液磁输送导管注入造影剂至十二指肠,经电磁装置的穿刺导管注入造影剂至胃内,X线下动态观察十二指肠末端位置及其与胃的空间关系,胃镜及X线监测下调整胃内的电磁装置和液磁输送导管的头端,使其分别位于胃和空肠欲吻合部位;④ 接通电磁体电源,经液磁输送导管推注液磁,X线下观察液磁在空肠起始段被电磁体吸附情况,并使其达到饱和吸附量,观察欲穿刺部位胃壁和肠壁贴附情况;⑤ 经穿刺导管送入胃肠穿刺针,穿刺针头端达胃壁后在X线监测下缓慢旋转推送穿刺针使其进入空肠起始段,再次经液磁输送导管推注造影剂使空肠起始段显影,以明确穿刺针头端位置;⑥ 确定穿刺针头端进入空肠起始段后,沿穿刺针置入球囊导管至空肠起始段,断开电磁装置电源,缓慢退出电磁体和液磁输送导管,球囊导管再次经胃镜送至胃内,球囊扩张胃壁和肠壁的穿刺道,然后沿球囊导管于胃肠穿刺部位植入双蘑菇头支架,胃镜及X线观察支架位置,胃内注射造影剂,观察造影剂有无腹腔渗漏。退出球囊导管和胃镜,术毕。
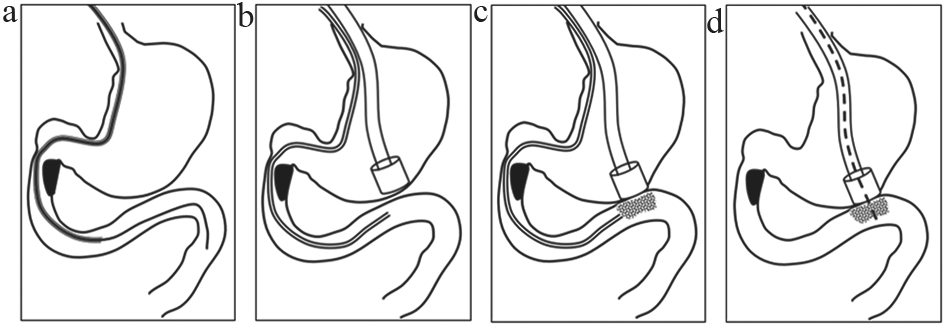
图3 MAT辅助内镜下胃肠穿刺示意图
注:a. 内镜下将液磁输送导管置入梗阻部位远端;b. 胃内置入电磁装置;c. 经液磁输送导管推注液磁,液磁被胃内电磁装置相吸;d. 胃壁肠壁锚定贴附后经穿刺导管送入胃肠穿刺针,建立胃肠穿刺道。
4 体外模拟实验
在本设计中胃肠穿刺能否成功取决于以下几个力之间的关系。要使肠壁和胃壁贴附在一起,需要克服胃壁和肠壁之间的组织牵拉力及胃肠道蠕动力,其中以组织牵拉力F牵拉力为主,穿刺过程中穿刺针穿透肠壁时存在穿刺摩擦力F穿刺摩擦力,而克服这些力的只有锚定磁体和液磁之间锚定力F锚定力,所以,只有当F锚定力>F牵拉力+F穿刺摩擦力时,穿刺才能顺利进行。在体外模式实验中,我们选用离体犬的胃和肠管为模型,在胃内置入锚定磁体,在空肠内注射液磁,当空肠壁和胃壁锚定贴附一起后,进行胃肠穿刺,结果显示在整个穿刺过程中,空肠壁与胃壁紧密贴附,未出现分离,穿刺过程顺利。
5 讨论
内镜技术发展迅速,诸多传统消化外科手术目前已经能够在内镜下完成,这一方面归因于内镜操作水平的不断提高,另一方面得益于内镜下配套器械的不断创新和研发。内镜下胃肠吻合在内镜中属于技术难度非常大的一项操作,其手术风险和术后并发症也非常高。尽管如此,由于其巨大的临床价值,如何降低内镜下胃肠吻合的操作难度和手术风险,成为众多消化内科医生探索的焦点。剖析内镜下胃肠吻合的关键性操作是胃肠穿刺道的建立,而胃肠穿刺道建立的难点在于如何使游离的胃壁和肠壁固定在一起,减少盲目性穿刺,即如何提高穿刺的靶向性。
MS技术利用特殊形式的“非接触性”磁场力特点,在临床疾病的诊疗中发挥着越来越大的作用。在MS五大技术中,目前比较成熟且在临床上应用最做的是磁压榨技术(Magnetic Compression Technique,MCT) 和 MAT。MCT可用于消化道吻合重建[13-18]、血管吻合[19-23]、空腔脏器造瘘[24-26]、直肠阴道瘘闭合修补[27-30]等领域。MAT主要用于减戳卡腔镜手术和内镜下辅助ESD术。我们团队早期在进行犬胃造瘘实验中将MCT和MAT联合起来实现了超微创胃造瘘,并尝试了MAT辅助下的穿刺操作,取得了满意的效果。
前期研究表明MAT可大大提高穿刺的靶向性和安全性[24-25],为此,我们将其引入到内镜下的胃肠吻合操作中来。本设计中AM位于胃内,TM位于空肠内,与现有的MAT不同,属于腔内锚定的范畴。从磁性材料上来讲,既往绝大多数研究中使用的是永磁材料,而本设计中考虑到严重的MGOO患者狭窄处难以通过体积较大的磁体,所以首次创新性地将液磁用于MS技术中来;对于AM我们采用了具有高度可控性的电磁铁,通过对电流的调节可以改变电磁铁的磁力,同时当锚定穿刺完成后,切断电磁体的电流可方便解除对液磁的吸引,这是永磁体无法完成的。所以本设计首次将可控性、智能化磁性材料应用到MS相关技术中来,丰富了MS技术的内涵。
[1] Lopera JE,Brazzini A,Gonzales A,et al.Gaetroduodenal stent placement: current status[J].Radiographics,2004,24(6):1561-1573.
[2] 崔真,白日星,宋茂民.姑息手术治疗恶性肿瘤致胃十二指肠输出道梗阻的现状与发展[J].中华外科杂志,2012,50(6):178-180.
[3] Itoi T,Ishii K,Ikeuchi N,et al.Prospective evaluation of endoscopic ultrasonography-guided double-balloon-occluded gastrojejunostomy bypass (EPASS) for malignant gastric outlet obstruction[J].Gut,2016,65(2):193-195.
[4] 严小鹏,商澎,史爱华,等.磁外科学体系的探索与建立[J].科学通报,2018.
[5] Shang Y,Guo H,Zhang D,et al.An application research on a novel internal grasper platform and magnetic anchoring guide system (MAGS) in laparoscopic surgery[J].Surg Endosc,2017,31(1):274-280.
[6] Scott DJ,Tang SJ,Fernandez R,et al.Completely transvaginal NOTES cholecystectomy using magnetically anchored instruments[J].Surg Endosc,2007,21(12):2308-2316.
[7] Rivas H,Robles I,Riquelme F,et al.Magnetic surgery: Results from first prospective clinical trial in 50 patients[J].Ann Surg,2018,267(1):88-93.
[8] Dominguez G,Durand L,De Rosa J,et al.Retraction and triangulation with neodymium magnetic forceps for single-port laparoscopic cholecystectomy[J].Surg Endosc,2009,23(7):1660-1666.
[9] Matsuzaki I,Hattori M,Hirose K,et al.Magnetic anchor-guided endoscopic submucosal dissection for gastric lesions (with video)[J].Gastrointest Endosc,2018,87(6):1576-1580.
[10] Matsuzaki I,Miyahara R,Hirooka Y,et al.Simplified magnetic anchor-guided endoscopic submucosal dissection in dogs (with videos)[J].Gastrointest Endosc,2014, 80(4):712-716.
[11] Matsuzaki I,Isobe S,Hirose K,et al.Magnetic anchor-guided endoscopic submucosal dissection for colonic tumor[J].Gastrointest Endosc,2017,85(5):1111-1112.
[12] Qu Y,Li J,Ren J,et al.Enhanced magneticfluid hyperthermia by micellar magnetic nanoclusters composed of MnxZn1-x-Fe2O4 nanoparticles for induced tumor cell apoptosis[J].ACS Appl Mater Interfaces,2014,6(19):16867-16879.
[13] An Y,Zhang Y,Liu H,et al.Gastrojejunal anastomosis in rats using the magnetic compression technique[J].Sci Rep,2018,8(1):11620.
[14] Ma F,Ma J,Ma S,et al.A novel magnetic compression technique for small intestinal end-to-side anastomosis in rats[J].J Pediatr Surg,2018.
[15] Bai J,Huo X,Ma J,et al.Magnetic compression technique for colonic anastomosis in rats[J].J Surg Res,2018,231:24-29.
[16] Leroy J,Perretta S,Diana M,et al.An original endoluminal magnetic anastomotic device allowing pure NOTES transgastric and transrectal sigmoidectomy in a porcine model: proof of concept[J].Surg Innov,2012,19(2):109-116.
[17] Gonzales KD,Douglas G,Pichakron KO,et al.Magnamosis III: delivery of a magnetic compression anastomosis device using minimally invasive endoscopic techniques[J].J Pediatr Surg,2012,47(6):1291-1295.
[18] Ryou M,Cantillon-Murphy P,Azagury D,et al.Smart selfassembling magnets for endoscopy (SAMSEN) for transoral endoscopic creation of immediate gastrojejunostomy (with video)[J].Gastrointest Endosc,2011,73(2):353-359.
[19] 严小鹏,吕毅,马佳,等.基于磁压榨技术的介入下肝外门腔分流器械的研制[J].中国医疗器械杂志,2013,37(6):421-422.
[20] Yan X,Fan C,Ma J,et al.Portacaval shunt established in six dogs using magnetic compression technique[J].PLoS One,2013,8(9):e76873.
[21] Yan XP,Liu WY,Ma J,et al.Extrahepatic portacaval shunt via magnetic compression technique: a cadaveric feasibility study[J].World J Gastroenterol,2015,21(26):8073-8080.
[22] Klima U,MacVaugh H 3rd,Bagaev E,et al.Magnetic vascular port in minimally invasive direct coronary artery bypass grafting[J].Circulation,2004,110(11Suppl1):Ⅱ55-60.
[23] Wang HH,Ma J,wang SP,et al.Magnetic anastomosis rings to create portacaval shunt in a canine model of portal hypertension[J].J Gastrointest Surg,2018.
[24] 严小鹏,任冯刚,刘雯雁,等.磁压榨技术联合内镜实施犬胃造瘘术[J].中华胃肠外科杂志,2015,18(8):832-834.
[25] 严小鹏,任冯刚,刘雯雁,等.磁锚定技术联合磁压榨技术实现超微创胃造瘘[J].中华实验外科杂志,2016,33(2):291-294.
[26] Uygun I,Okur MH,Arayici Y,et al.Magnetic compression ostomy for simple tube colostomy in rats-magnacolostomy[J].Adv Clin Exp Med,2012,21(3):301-305.
[27] 严小鹏,高燕凤,邹余粮,等.基于磁压榨技术的直肠阴道瘘一期修补装置[J].生物医学工程学杂志,2015,32(5):1096-1099.
[28] Yan XP,Zou YL,She ZF,et al.Magnet compression technique: a novel method for rectovaginalfistula repair[J].Int J Colorectal Dis,2016,31:937-938.
[29] 付珊,马佳,赵广宾,等.磁压榨直肠阴道瘘闭合修补装置的改良设计[J].中国医疗设备,2018,33(4):46-49.
[30] She ZF,Yan XP,Ma F,et al.Treatment of rectovaginalfistula by magnetic compression[J].Int Urogynecol J,2017,28:241-247.
Magnetic Anchor Technique Assisting Endoscopic Gastrojejunostomy