医疗设备质控检测与预防性维护规范探讨
引言
随着人民生活的提高,卫生健康需求也在逐年增加。据Evaluate MedTech发布的《World Preview 2018, Outlook to 2024》显示,2017年全球医疗器械市场规模已经突破4000亿美元大关,初步测算2018年全球医疗器械市场规模为4278亿美元,到2019年预计这一规模将进一步超过4500亿美元[1]。而中国的医疗器械市场规模从2013年的3559亿元人民币增长到2017年的6500亿元人民币,一直保持高速增长[2]。医疗器械产业作为国民经济的重要组成部分,政府在加大对该产业政策扶持力度的同时不断优化和简化审批流程,资本对医疗器械的投资热情高涨,国产新产品不断涌现。
但是,就当前医疗器械全生命周期管理而言,很多国内医疗器械生产企业在新产品研发和销售等方面投入了重金,却忽视了产品投入使用后医疗设备应该开展的预防性维护和定期质控检测项目的制定与研究。另外,原国家食品药品监督管理总局18号令《医疗器械使用质量监督管理办法》和国家卫生与健康委员会发布的《医疗器械临床使用管理办法》都提到了医疗机构对需要定期检查、检验、校准、保养、维护的医疗器械,应当按照产品说明书的要求进行检查、检验、校准、保养、维护并予以记录,及时进行分析、评估,确保医疗器械处于良好状态[3-5]。为此,医疗机构肩负医疗器械管理职能的医学工程部门将直接面临这样的困惑:“如果产品的说明书上没有这方面的内容规定,对该医疗产品是否需要开展及怎么开展检测与质控工作?”
不管是从医学工程师(以下简称医工)专业角度考虑还是参考同类产品使用说明,医疗设备都需要有质控检测和预防性维护的内容要求。在医疗设备全生命周期管理中,如果没有或无法有效的开展质控检测和预防性维护,又如何保证医疗产品能安全有效地为病人及医务人员服务?为此我们尝试从理论、实践及医疗机构的实际情况出发,建立一个医疗设备通用的质控检测和预防性维护规范模式。该研究有如下两方面意义:① 为医疗设备生产企业和医疗机构提供切实可行的参考依据;② 依托当前大数据时代背景,制定统一的检测项目和评估标准,为不同产地不同品牌的同类医疗设备进行可靠性、稳定性、使用寿命等方面的评价打下坚实的数据规范化基础。
1 方法
1.1 规范的制定原则
医疗设备质控检测和预防性维护内容的制定应该遵守以下几个原则按照重要性先后排列如下:① 该类产品相关的国家法律或法规要求;② 该类产品的国家标准、行业标准、国际标准等,尤其是强制性的标准;③ 该产品的计量检定规程;④ 企业制造标准或产品技术手册;⑤ 同类进口产品的质控检测和预防性维护方法;⑥ 工程师根据产品的工作原理及特殊性能做出的合理评估;⑦ 结合医疗机构的实际情况所作的适当调整。
生产企业或者医疗机构可参考上述原则,充分考虑医疗设备工作原理、制造工艺和组成结构的特异性,科学有效的制定相关医疗设备的质控检测与预防性维护内容。
1.2 规范的组成
医疗设备质控检测和预防性维护规范应包括设备名称、参考依据、检测设备要求、检测项目及要求和检测周期等五个部分组成,根据具体设备这些内容可以用规范性文件或者图表进行详细描述。下面以除颤仪为例介绍该规范的组成。
1.2.1 设备名称
设备名称可参考医疗器械注册证产品名称一栏,也可用行业通用名表述,如“除颤仪”。
1.2.2 参考依据
参考依据是制定医疗设备质控检测和预防性维护规范的原则指导,参考范围和参考顺序可依照本文第1部分“医疗设备质控检测和预防性维护规范的制定原则”内容执行。如除颤仪的参考依据有:GB9706.1-2007《医用电气设备 第1部分:安全通用要求》[6];GB 9706.8-2009《医用电气设备 第2-4部分 心脏除颤器安全专用要求》[7];YY/T 0841-2011《医用电气设备 医用电气设备周期性测试和修理后测试》[8];YY 0784-2010《医用电气设备医用脉搏血氧仪设备基本安全和主要性能专用要求》[9];JJF1149-2014《心脏除颤器校准规范》[10];JJG 760-2003《心电监护仪检定规程》[11]以及产品说明书。
1.2.3 检测设备要求
检测设备要求是指要对该医疗设备既定检测项目进行检测所需要用到检测设备的说明。如:除颤仪检测所需的检测设备有电气安全测试仪、除颤仪能量分析仪、生命体征模拟器、电池性能测试仪等。
1.2.4 检测项目及要求
检测项目及要求包括外观及功能性检查、电气安全检测、校准项目、维护保养和其他,各项目有自己的标准要求和限值范围,除颤仪质控检测与预防性维护内容,见图1。
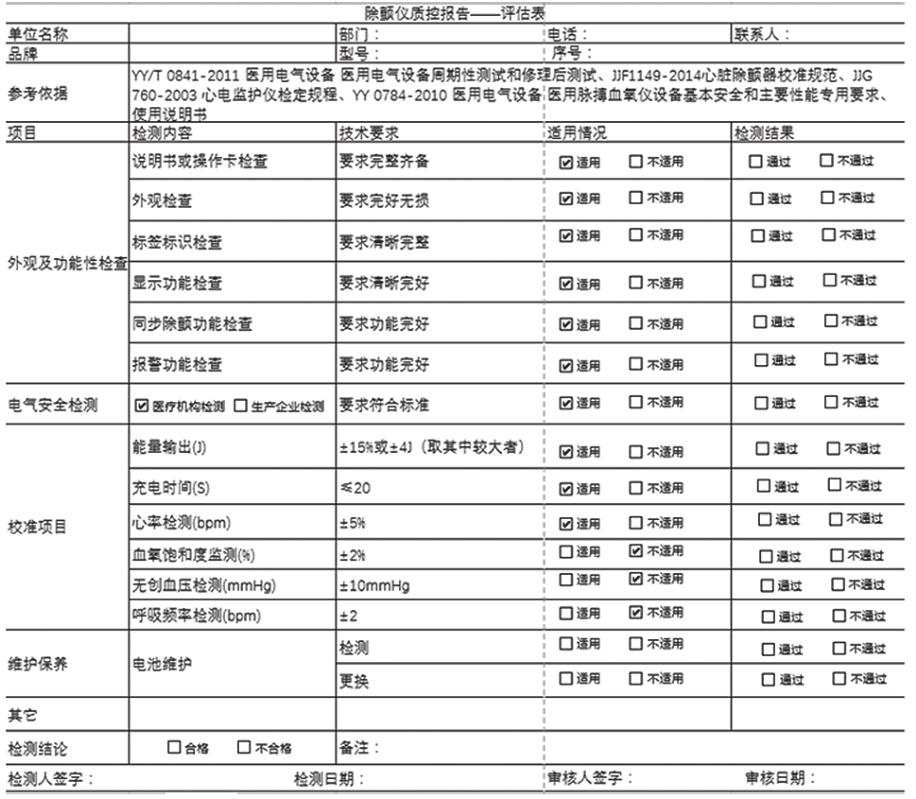
图1 除颤仪质控报告——评估表
注:此表用于被测设备合格与否的评价,全部项目检测结果通过检测结论判定为合格否则判定为不合格。
外观及功能性检查包括说明书或操作卡检查、外观检查:如外壳、电源线、电极板、心电导联线(如有配置)等、各类标签标识检查(如计量标签、预防性维护标签等)、功能检查。在制定功能检查项目类内容时,应提炼出某一类医疗设备通常具有的很多相同或类似功能的检查内容,但不同品牌的同类医疗设备除相同功能检查内容外,也应根据各自的特点进行个性化功能检查项内容的编制(图1)。
根据有源医疗设备的电气安全分类,医用电气设备通常可分为I类B、I类BF、I类CF、II类B、II类BF、Il类CF等,不同的类别就有不同的安全限值。制定医疗设备电气安全检测项目内容应根据设备标签、产品说明书或产品注册要求确定电气安全类别。对于电气安全检测项目参考值,鉴于医疗设备使用和生产环境的区别,医疗机构可以考虑采用YY/T0841-2011(等同于IEC62353-2007)作参照,生产企业生产产品应该采用GB9706.1-2007(等同于IEC60601-1)所规定的参考值。除颤仪电气安全检测项目限值的展示,见图2~3。
校准项目是指医疗设备的质控检测项目,是开展医疗设备质控检测最核心的内容。在制定校准项目内容时,需要从相关的国家标准、行业标准中选出能反映该类机器主要性能的通用指标,可以参考该类设备的计量检定规程内容来确定通用检测项目,当然也可以在通用检测项目的基础上增加一些不同品牌特有的检测项目,以满足不同设备有不同的检测需求[12]。不同的校准项目可能包含一个测量序列的多个检测值来检测,这些检测值应尽可能均匀分布及涵盖整个测量范围,每个检测值都需要各自的技术要求来评判设备是否需要校正或维修[13-14]。这里有一个非常重要的内容是每个检测项目都必须设定它的正常范围,超出这个范围就必须校正或维修。制定这个范围必须依据各种法规、标准、计量检定规程等要求,再结合临床实践可适当微调。它是判断一台医疗设备工作正常与否的标准,所以一定要认真、仔细、严谨地去设定这个正常范围。除颤仪必须开展校准项目的具体规程展示,见图4。
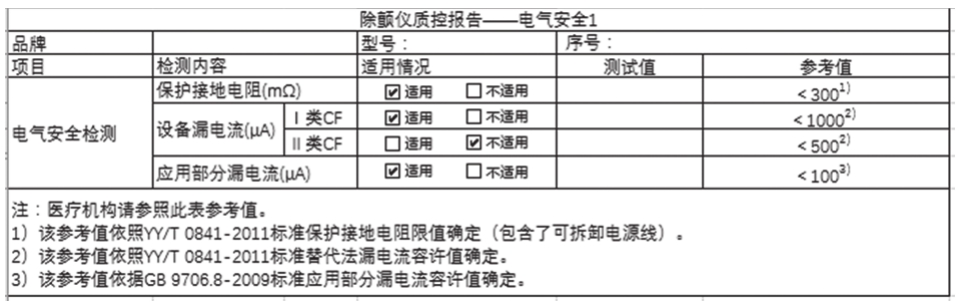
图2 除颤仪质控报告——电气安全1
注:此表适用于医疗机构医用电气设备电气安全性能检测。
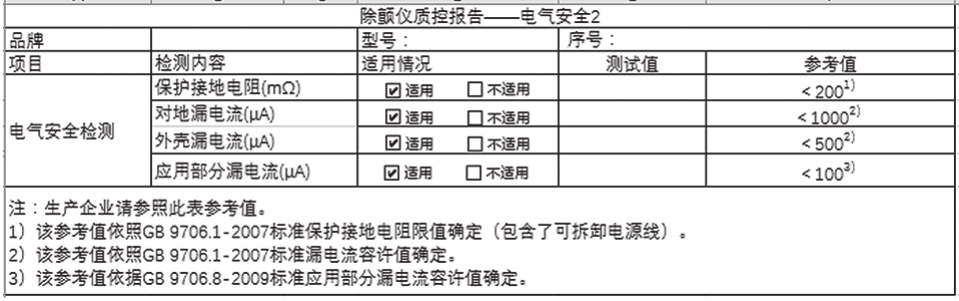
图3 除颤仪质控报告——电气安全2
注:此表适用于生产企业医用电气设备电气安全性能检测。

图4 除颤仪质控报告——校准项目1
注:此表描述了医疗设备校准项目内容,不同医疗设备项目不一。
维护保养项目主要指对设备使用过程中的易损易耗部件进行定期更换或保养,对设备进行定期清洁和润滑也属于维护保养的一部分,这里要特别关注各种过滤网和电池的定期清洗或更换。如除颤仪的电池就是关注重点。
其他项可包含不同品牌同类设备的个性化检测项目(图5)和维护保养内容。
1.2.5 检测周期
医疗设备质控检测与预防性维护周期项目也像规范中其他项目一样根据标准、规程和说明书的要求来制定,并强烈建议在具体实施过程中医疗机构应根据医疗设备功能、电气安全等级、故障危害、使用环境、使用频率、历史数据、医疗事故历史等进行优化,以提高医工人员的工作效率,节约人力、财力的投入。如除颤仪质控检测与预防性维护周期[15-16]如下:外观及功能性检查为每半年一次;电气安全检测为每半年一次;校准项目为每半年一次;维护保养中,电池性能检测为每半年一次,铅酸电池更换建议周期为每一年一次,锂电池更换建议周期为每三年一次。
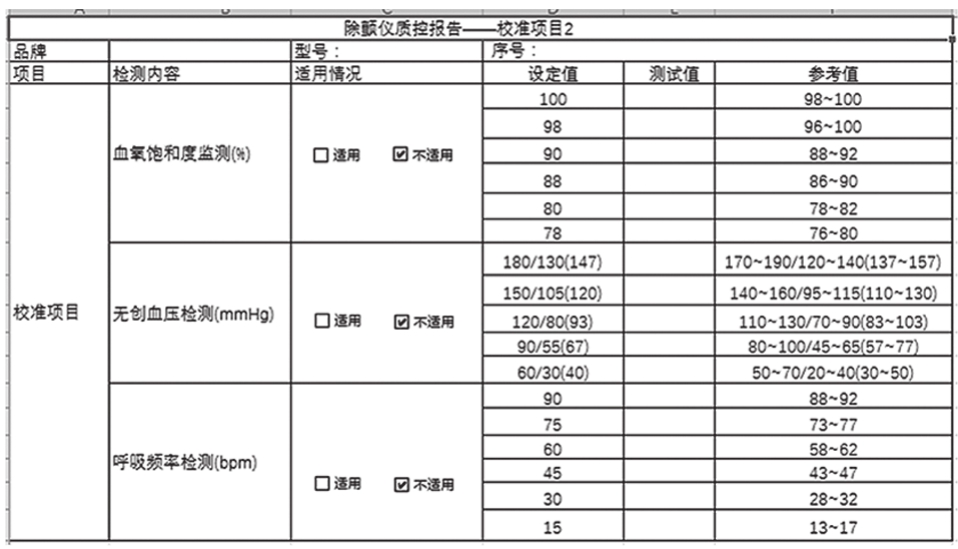
图5 除颤仪质控报告——校准项目2
注:此表描述了医疗设备校准项目内容,不同医疗设备项目不一。
2 结果
按此模式我院已制定出包括除颤仪、监护仪、计算机断层扫描成像系统、磁共振成像系统、B超、数字病理等医疗设备的质控检测和预防性维护内容模板20多种,质控数据借助医疗设备信息管理系统将其进行结构化。另外,开展医疗设备质控技术现场指导实践2场、培训近250人次、范围涉及杭州台州2地,医工据此开展相关医疗设备质控检测和预防性维护工作并取得了良好的应用效果。
3 讨论
大数据已成为国家重要的基础性战略资源,数据格式的标准化或规范化是数据资源充分利用的前提。该医疗设备通用的质控检测和预防性维护规范模式探究将倡导相关数据的标准化、规范化及数字化。在此之前相关医疗设备质控检测与预防性维护内容主要是厂家根据各自的生产标准来制定或零星关于具体医疗设备质控相关参考文献,存在同类医疗设备的质控检测项目、参数和正常范围等不相同的缺憾,彼此之间无法比较,影响到机器寿命、维护周期的预测[17-18]。本文探讨和实践的医疗设备质控检测与预防性维护规范就是在遵守各种法规、标准、经验等的基础上及在考虑不同品牌和不同医院环境需要保留的个性化需求前提下,提出某类医疗设备必须要检测的性能参数和范围,为今后分析、评价、预测、决策等积累非常有用的数据资源,为医疗设备的科学管理和医工队伍的发展建设提供助力。
医疗设备质控检测与预防性维护内容不能一成不变,要做到与时俱进适时调整,当相关医疗设备的国家法规、国家标准、行业标准、企业标准、计量规程发生变化或更新后,应及时修改相应的质控检测与预防性维护规程。
由于技术原理的区别,不同品牌的同类医疗设备除相同功能检查内容外,应具备符合自身特点的个性化功能检查项内容。这是医工从业人员应当考虑的一个重要方面,是难点需要付出更多的研究和努力。
关于项目具体实施由于医工人员和检测设备配置的不足,对于乡镇卫生院开展医疗设备质控检测与预防性维护工作还有一定的难度。但随着区域医联体建设的推进,可先开展知识宣教并结合地方质控中心资源定期开展工作。
4 结论
规范制定医疗设备质控检测与预防性维护内容是医疗设备生产企业和医疗机构的共同责任,医疗设备生产企业应当在其产品说明书中包含质控与预防性维护相关内容,内容制定可参照文中描述模式进行,力求做到有理有据和切实可行。医工根据说明书内容制定具体设备的质控检测与预防性维护规范,按规范对医疗设备开展质控检测与预防性维护工作,检测结果可借助医疗设备信息管理系统进行科学分析,依据分析结果对相应设备的质控检测与预防性维护规程进行改进,以更好地提高医疗设备的安全性和有效性。为保障医疗设备安全有效地使用,其质控检测与预防性维护规程的执行是不断持续改进的,规范内容也应该不断持续改进。
[1] 中商产业研究院.中商产业研究院.2019-2024年全球医疗器械行业前景及投资机会研究报告[R].
[2] 中国医学装备协会.中国医学装备发展状况与趋势(2018)[M].北京:人民卫生出版社,2018.
[3] 中华人民共和国全国人民代表大会.中华人民共和国标准化法[Z].2017-11-4.
[4] 国家食品药品监督管理总局.医疗器械使用质量监督管理办法[Z].2015-10-21.
[5] 国家卫生健康委.医疗器械临床使用管理办法(征求意见稿)[Z].2019-03-15.
[6] GB9706.1-2007,医用电气设备 第1部分:安全通用要求[S].
[7] GB 9706.8-2009,医用电气设备 第2-4部分 心脏除颤器安全专用要求[S].
[8] YY/T 0841-2011,医用电气设备医用电气设备周期性测试和修理后测试[S].
[9] YY 0784-2010,医用电气设备医用脉搏血氧仪设备基本安全和主要性能专用要求[S].
[10] JJF1149-2014,心脏除颤器校准规范[S].
[11] JJG 760-2003,心电监护仪检定规程[S].
[12] 丁可.便携式医疗设备通信异常数据检测仿真[J].计算机仿真,2018,35(12):329-332.
[13] 顾丹萍,王文辉,谭申生.上海市医疗质量控制评价体系分析与思考[J].中华医院管理杂志,2017,33(3):222-224.
[14] 曹晗曦.做好预防性维修在医疗设备维修中的应用[J].科技创新与应用,2017,(6):127.
[15] 桂朝伟,谭爱璐.除颤监护仪的工作原理与维护保养[J].临床医学工程,2008,(3):31-33.
[16] 鲍怀东.心电除颤仪工作原理及日常维护探讨[J].经营管理者,2017,(3):395.
[17] 洪毅姜.医用电气安全的质量控制及分析[J].中国医疗设备,2018,33(7):50-52.
[18] 石雷,杨贵超,王沙维.质量控制在多参数监护仪维护保养中的重要性[J].信息记录材料,2018,19(7):219-221.
Discussion on Rules Formulating About Inspection and Preventive Maintenance of Medical Equipment