基于阈值分割及模式分类器的硬性渗出自动检测方法对比研究
引言
目前,糖尿病已是一种严重威胁人类健康的顽疾。据预测,将来全球糖尿病患者将会占总人口的4.4%[1]。我国情况更为严峻,糖尿病患者已达9240 万,位居全球之首[2]。糖尿病还会带来一系列并发症,其中以糖尿病视网膜病变(简称“糖网”,Diabetic Retinopathy,DR)发生率最高。糖网影响视力,目前已成为成人致盲的首要原因[3]。因为糖尿病患者均面临着发展为DR 的高风险,且DR 具有进行性和不可逆性,故对于已患糖尿病的患者而言,如何在还未发生视力损伤的情况下及时准确地筛查出其是否患有DR,不仅为及早诊断、及早治疗从而挽救患者视力提供先机,还可节约大量宝贵的医疗资源[4]。目前,临床存在多种糖网筛查手段及方法[5-6],其中眼科医生普遍认为眼底照相检查最适合用于DR 的筛查和随诊[7]。但该方法现阶段基本依靠人工阅片,这严重制约了DR 筛查大规模的实施。故早在20 世纪七八十年代就有研究人员提出利用计算机采用数字图像处理与分析技术来实现这一任务,其中又以对硬性渗出(Hard Exudates,EXs)区域自动检测的研究最为广泛、深入。
最初,研究人员探求利用灰度级特征提取黑白眼底图像中的EXs 区域,不过这需依据直方图人为选择分割所需阈值[8];Philips 等[9]也提出了基于灰度值的EXs 分割方法,但需手动圈定ROI;后来,Gardner 等[10]利用BP 神经网络实现了EXs 的自动检测;Sinthanayothin 等[11]提出利用与“Moat Operation”结合的循环区域增长法实现EXs 的自动检测,但其检测结果很大程度上依赖所选取的种子点位置和停止准则;Osareh 等[12]利用FCM 算法分别结合神经网络与SVM 完成了EXs 的自动识别;Zhang 等[13]在Luv彩色空间利用改进的FCM 算法与SVM 完成了EXs 的自动识别;Niemeijer 等[14]运用数学形态学以及K 近邻分类器实现EXs 的自动识别;Jaafar 等[15]提出的方法首先通过局部对比度获取EXs 候选区域,在此基础上利用拆分合并算法筛选出真正的EXs;Soares 等[16]提出采用尺度空间曲率以及动态阈值的方法自动分割眼底图像中EXs;Esmaeili等[17]所提出的方法通过曲波变换方法获取了眼底图像中的该病灶。目前,国内在该方面的相关研究报道不多,主要有林蔚[18]提出利用基于K 近邻图的区域合并算法实现眼底图像中EXs 的分割,高玮玮等[19]提出的基于数学形态学的EXs 自动检测方法。
筛查意味着所要处理的数据对象数量庞大,即在临床中要求筛查系统所使用的算法不仅具有很强的普适性,而且还得具有较高的效率。因此,糖网自动筛查系统中的算法应当具备较强的可靠性和高效性,为此充分利用训练好的模式分类器强大、高效的识别能力,提出一种基于阈值分割及模式分类器的EXs 自动检测方法,并结合建立基于眼底图像的糖网自动筛查系统这一应用背景,深入对比研究多种EXs 自动检测方法的性能,以期实现能应用于临床的糖网自动筛查系统。
1 材料与方法
源图像为126 幅由Canon CF-60 DSI 眼底照相机拍摄的分辨率为3504×2336 像素的JPG 彩色眼底图像,具体来源于苏省南京市某医院。在实际使用时,对原图进行了裁减并进行了压缩,即实际处理图像的分辨率为800×600像素。将这126 幅眼底图像交由眼科医师判定,其中早期DR 眼底图像有68 幅,均有EXs(图1)出现,其余为正常眼底图像。
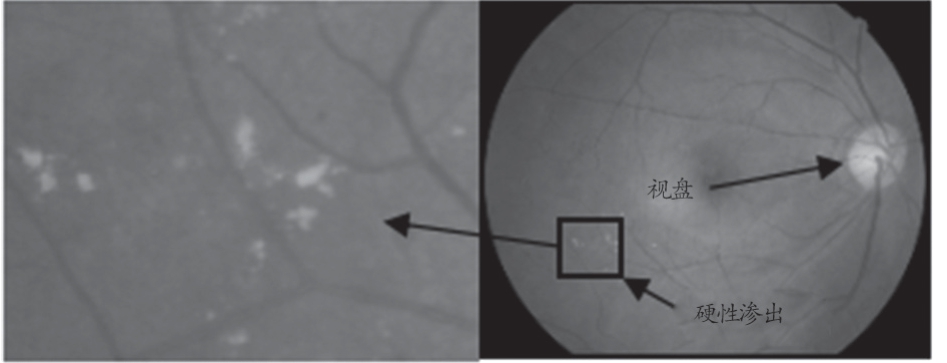
图1 彩色眼底图像及EXs细节
将这126 幅眼底图像随机分为两组,其中,第一组(包括40 幅早期糖网病人眼底图像和30 幅正常眼底图像)为分类器提供训练样本,确定分类器结构;第二组(共56 幅,分别为28 幅早期DR 病灶图像以及28 幅正常眼底图像)用来评测方法的自动检测性能。
实验采用Intel Core Duo E7500 CPU,6GB RAM 的计算机,MATLAB R2010a 的软件环境。
2 方法
基于阈值分割及模式分类器的EXs 自动检测方法首先利用阈值分割获取EXs 候选区域;然后,对候选区域的特征集进行优选;最后,利用优化后的特征集及相应人工判定结果分别建立RBF 神经网络分类器及SVM 分类器,从而实现对EXs 的自动检测,具体如图2 所示。

图2 基于阈值分割及模式分类器的EXs自动检测算法流程图
2.1 粗分割
阈值分割是一种最简单直接的图像分割方法,可实现对背景以及噪声的有效滤除。目前常用的有直方图法、最大类间方差法(Otsu)、迭代法等。其中Otsu 阈值法是基于类间方差最大的非参数、无监督的自适应阈值选择方法,运算速度快,是一种较好的阈值分割法。但不足的是它只考虑了类间距,没有考虑类的内聚性,故当图像的噪声干扰较大时,不能得到理想的分割结果,但它对类间方差为单峰的图像能产生较好的分割结果(通过分析多幅眼底图像G 通道灰度直方图发现,眼底图像G 通道的灰度直方图都近似呈单峰状,如图3c 所示。波峰对应背景像素,与波峰右侧相关的就是想要提取的白色区域,即EXs 候选区域),鉴于此,选用一种改进的二维Otsu 自适应阈值分割方法[20]来对眼底图像G 通道进行粗分割并“剔除”视盘(对于视盘的分割采用前期研究[19]中提出的方法)来获取EXs 候选区域。该方法在克服了传统Otsu 阈值分割信息不完备的同时还具有较强的抗噪性能,故对EXs 的分割效果好,图3a 的粗分割结果具体见图3d。
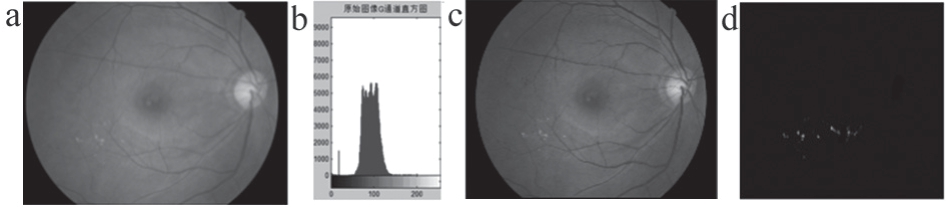
图3 眼底图像G通道直方图及粗分割结果
注:a. 原彩色眼底图像;b. G 通道;c. 直方图;d. 粗分割结果。
利用该阈值分割方法对作为训练样本的70 幅眼底图像进行粗分割,并从中去除视盘从而获取了2570 个EXs 候选区域(据眼科医师判断,其中1160 个为真EXs,1410个为假EXs)。
2.2 特征提取
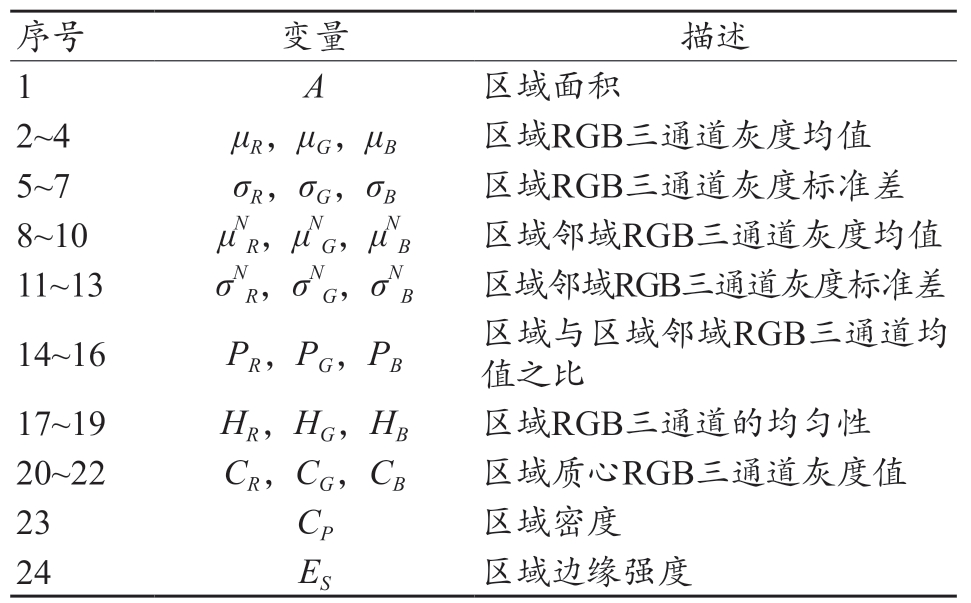
对上述获取的EXs 候选区域而言,为利用模式分类器将其中的真、假EXs 准确区分开来,需利用这些区域的特征作为模式分类器的输入对其进行训练。对EXs进行识别时,眼科医生往往会从亮度、面积、边缘等入手,而这些方面可通过以下24 个特征进行一定程度的表述[21-22],具体见表1。
表1 EXs特征集
序号 变量 描述1 A区域面积2~4 μR,μG,μB 区域RGB三通道灰度均值5~7 σR,σG,σB 区域RGB三通道灰度标准差8~10 μN R,μN G,μN B 区域邻域RGB三通道灰度均值11~13 σN R,σN G,σN B 区域邻域RGB三通道灰度标准差14~16 PR,PG,PB区域与区域邻域RGB三通道均值之比17~19 HR,HG,HB 区域RGB三通道的均匀性20~22 CR,CG,CB 区域质心RGB三通道灰度值23 CP 区域密度24 ES 区域边缘强度
2.3 特征选择
特征用来设计、训练模式分类器,但随着特征数量的增加,误分类的可能性亦会随之升高,故需对上述提取出的24 个特征进行选择。常规的特征选择算法——判别分析法(Discriminate Analysis,DA)要求数据呈多元正态分布以及满足方差齐性的要求。而另一种特征选择算法——逻辑回归分析法(Logistic Regression,LR)对数据的分布限制条件较少,当数据不为正态分布或者各类的协方差差别较大时,LR 性能更优[23]。利用软件SPSS 18.0 对粗分割阶段获取的2570 个EXs 候选区域的24 个特征进行分析,得到数据的具体情况是:对上述特征进行Kolmogorov-Smirnov 检验和Shapiro-Wilk 检验,发现均不符合正态分布;另外,Leven’s 方差齐性检验表明除μR、μG、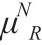 、CR、CG、CP 外的其它特征均不符合方差齐性要求。另外,是否为EXs 可概括为一个二分的分类变量,故此处采用LR 对提取出的24 个特征进行选择最为合适。
、CR、CG、CP 外的其它特征均不符合方差齐性要求。另外,是否为EXs 可概括为一个二分的分类变量,故此处采用LR 对提取出的24 个特征进行选择最为合适。
对粗分割阶段获取的2570 个EXs 候选区域的24 个特征,利用二项Logistic 回归模型采用“逐步回归”的方法进行选择(其中a进取0.05,a出取0.1),具体选择结果见表2。
表2 特征选择结果
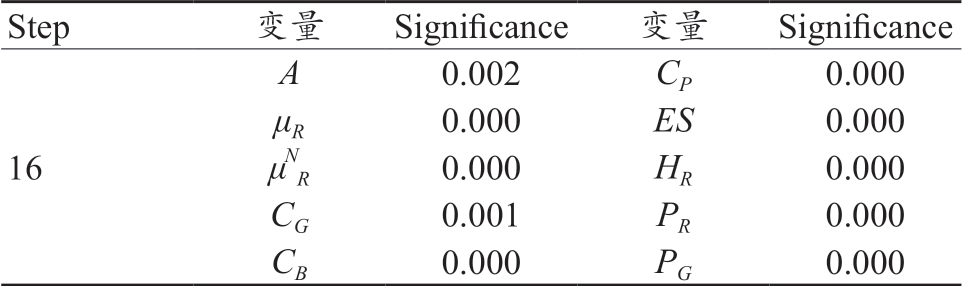
Step 变量 Significance 变量 Significance 16 A 0.002 CP 0.000 μR 0.000 ES 0.000 μN R 0.000 HR 0.000 CG 0.001 PR 0.000 CB 0.000 PG 0.000
模型建好后,采用-2对数似然值(对数似然比值乘以-2)来度量模型对数据的拟合度。经过优化的特征集与完整特征集对训练样本的拟合度(-2 对数似然值)为990.277,分类准确性为88.0%。可见,两特征集的拟合度相差无几;但就对训练样本的分类结果而言,明显优化特征集性能更优。
2.4 分类器训练及预测
将2570 个候选区域经过优化的特征参数与对该区域是否为EXs 的人工判定结果分别作为训练集的输入和输出,对RBF 神经网络以及SVM 进行训练及预测。
2.4.1 RBF神经网络分类器的训练及预测
RBF 神经网络分类器训练时,隐层节点个数Num 不断增加,直至网络输出误差小于所设定期望值goal。此外,还需对参数spread 进行合理设置。在利用“newrb”命令建立RBF 网络模型时,采用10 倍交叉验证(将2570 个EXs 候选区域随机分为10 组,依次将其中9 组做训练,1组做测试)对网络进行训练及预测。令扩展速度spread[1,5]在间以步长0.1 进行取值,对每一个取值进行上述10 倍交叉验证,分别得到网络在最不理想情况下的预测结果(图4)。图4 表明,当spread 为2.3 时,得到的网络在最不理想情况下的分类准确率最高,为93.27%,此时灵敏度为92.61%,特异性为95.13%。故当spread 选取此值时,无论采用何种样本对网络进行训练,预测结果均可达到令人满意的水平。
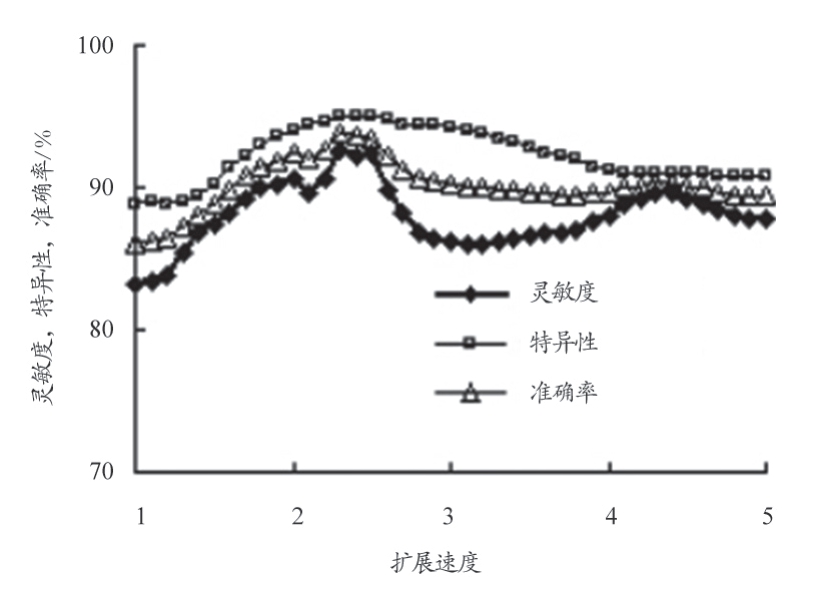
图4 扩展速度不同取值时10倍交叉验证情况下的网络最不理想预测结果
当训练结束后即可得到确定的RBF 神经网络结构,此时当输入新的样本时即可进行是否为EXs 的自动判别。
2.4.2 SVM分类器的训练及预测
在SVM 中常用的核函数中,高斯径向基核函数具有较强的非线性映射能力、较少的超级参数、数值实现也较为简单,故在本研究中选用基于高斯径向基核函数作为该方法中SVM 的核,在此基础上要得到结构确定的SVM 分类器需确定两个参数:惩罚参数和核函数参数。为获取分类性能最佳的SVM 模型,需得到最佳的惩罚参数和核函数参数。由于遗传算法(Genetic Algorithm,GA)具有很强的全局搜索能力,且这种搜索能力不依赖于特定的求解模型故采用GA 对SVM 的这两个参数进行优化,具体优化流程如图5 所示。

图5 GA优化C及γ的算法流程图
利用候选区域经过优化的特征集以及相应的人工判定结果分别作为训练集的输入和输出,对SVM 进行训练及预测,具体参数分别为C=2.39,γ=1.25。寻优结果显示SEval、SPval、ACCval 的 值 分 别 为95.13%、98.01%、96.72%。同样,训练完毕后即得到了确定的SVM 模型,即可对新的输入样本进行是否为EXs 的自动识别。
3 实验结果与分析讨论
作者此前研究并发表了一种基于数学形态学的EXs 自动检测方法[19],为探求最为满足实际需求的EXs 自动检测方法,有必要对包括数学形态学方法在内的多种EXs 自动检测方法进行对比研究。
利用数学形态学方法和建立好的RBF 神经网络分类器以及SVM 分类器分别来识别第二组眼底图像中的EXs,具体结果是:对于病灶图像(共28 幅),两种方法均检测到了EXs;对于健康眼底图像(共28 幅),数学形态学方法在2 幅中图像中检测到了EXs,而阈值分割及模式分类器方法则在3 幅图像(其中2 幅与数学形态学方法一致)中检测到了EXs。具体检测结果见表3,其中,同一眼底图像的EXs 具体检测结果如图6 所示。此外,文献[12]提出的FCM 结合BP 神经网络方法、文献[18]提出的基于K近邻图的区域合并算法对该组图像的检测结果也见表3。
表3 EXs具体检测结果
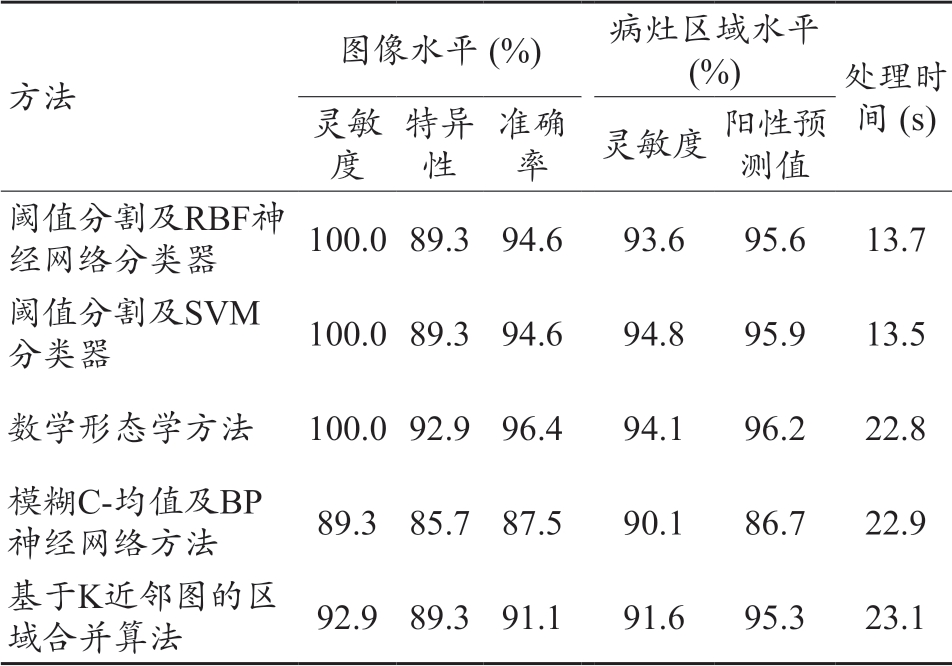
方法图像水平 (%) 病灶区域水平 (%) 处理时间 (s)灵敏度特异性准确率 灵敏度 阳性预测值阈值分割及RBF神经网络分类器 100.0 89.3 94.6 93.6 95.6 13.7阈值分割及SVM分类器 100.0 89.3 94.6 94.8 95.9 13.5数学形态学方法 100.0 92.9 96.4 94.1 96.2 22.8模糊C-均值及BP神经网络方法 89.3 85.7 87.5 90.1 86.7 22.9基于K近邻图的区域合并算法 92.9 89.3 91.1 91.6 95.3 23.1
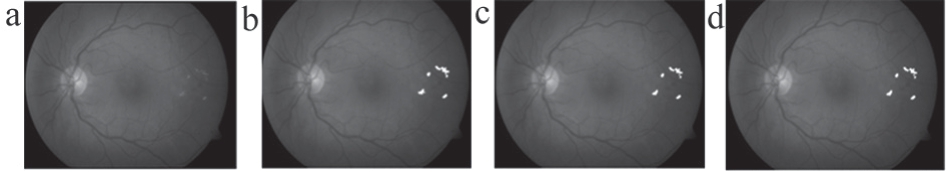
图6 EXs自动检测结果
注:a. 原彩色眼底图像;b. 数学形态学方法;c. 阈值分割及RBF神经网络分类器方法;d. 阈值分割及SVM分类器方法。
由表3 发现,所提出的两种EXs 分割算法均已达到英国糖尿病协会(British Diabetic Association)于1997 年提出的DR 病灶自动筛查算法标准[24]:灵敏度最低80%,特异性最低95%。此外,从表3 还可发现:基于阈值分割及模式分类器(包括RBF 神经网络分类器和SVM 分类器)方法的检测精度优于文献[12,18],略低于文献[19],但检测效率均优于文献[12,18-19];而对于这两种分类器之间而言,由表3 可发现(具体参见病灶区域水平评价指标),SVM 分类器的识别率明显较RBF 神经网络分类器更高。此外,对于糖尿病患者而言,其视网膜病变情况会受病情治疗、控制与病程等因素影响,故只有保证较高的检查频率才能及时、有效地发现视网膜的相关病变。因此就DR自动筛查的实际应用而言,基于阈值分割及SVM 分类器的EXs 自动检测方法性能更佳。
4 结论
眼底图像中EXs 的自动识别是构建糖网自动筛查系统的重要环节,直接影响系统的筛查性能。只有快速、有效的自动检测方法才能满足临床对筛查的要求。据此充分利用训练好的模式分类器强大、高效的识别能力,提出一种基于阈值分割及模式分类器的EXs 自动检测方法,并与包括基于数学形态学的EXs 自动检测方法在内的多种EXs 检测方法进行了对比研究。实验结果表明,与其他硬性渗出分割方法相比,基于阈值分割及模式分类器(包括RBF 神经网络分类器和SVM 分类器)方法在保证较高检测精度的同时效率也较高;而对于RBF 神经网络分类器和SVM分类器之间而言,明显SVM 分类器的性能更优。故就糖网自动筛查的临床应用而言,基于阈值分割及SVM 分类器的EXs 自动检测方法性能更优。该研究工作为构建基于眼底图像的糖网自动筛查系统提供了可靠的技术支持。对糖网自动筛查系统而言,在实现了高效的EXs 自动检测基础上,剩下的其他早期糖网病灶,如视网膜内出血等的高效自动检测则将是下一步的研究重点。
[1] Wild S,Roglic G,Green A,et al.Global prevalence of diabetes: estimates for the year 2000 and projections for 2030[J].Diabetes Care,2004,27(5):1047-1053.
[2] 蒲一民,杨君,杨田.糖尿病视网膜病变药物治疗的研究进展[J].国际眼科杂志,2011,11(12):2134-2137.
[3] Watkins PJ.ABC of diabetic retinopathy[J].Br Med J,2003, 7(2):105-107.
[4] Sánchez CI,Hornero R,López MI,et al.Retinal image analysis to detect and quantify lesions associated with diabetic retinopathy[A].Proceedings of 26th IEEE Annual International Conference on Engineering in Medicine and Biology Society[C].San Francisco:IEEE,2004:1624-1627.
[5] Villarroel M,Ciudin A,Hernández C,et al.Neurodegeneration: an early event of diabetic retinopathy[J].World J Diabetes, 2010,1(2):57-64.
[6] 彭金娟,邹海东,王伟伟,等.上海市北新泾社区糖尿病视网膜病变远程筛查系统的应用研究[J].中华眼科杂志,2010,46(3):258-262.
[7] 张蕾,许维强,谭荣强,等.糖尿病视网膜病变筛查方法探讨[J].国际眼科杂志,2010,10(3):482-484.
[8]Ward NP,Tomlinson S,Taylor CJ.Image analysis of fundus photographs. The detection and measurement of exudates associated with diabetic retinopathy[J].Ophthalmology,1989,96(1):80-85.
[9] Philips R,Forrester J,Sharp P.Automated detection and quantification of retinal exudates[J].Graefes Arch Clin Exp Ophthalmol,1993,231(2):90-94.
[10] Gardner G,Keating D,Williamson TH,et al.Automatic detection of diabetic retinopathy using an artificial neural network: a screening tool[J].Br J Ophthalmol,1996,80(11):940-944.
[11] Sinthanayothin C,Boyce JF,Williamson TH,et al.Automated detection of diabetic retinopathy on digital fundus images[J].Diabetic Med,2002,19(2):105-112.
[12] Osareh A,Mirmehdi M,Thomas B,et al.Automated identification of diabetic retinal exudates in digital colour images[J].Br J Ophthalmol, 2003,87(10):1220-1223.
[13] Zhang X,Chutatape O.Top-down and bottom-up strategies in lesion detection of background diabetic retinopathy[A].2005 IEEE Computer Society Conference on Computer Vision and Pattern Recognition[C].San Diego:IEEE,2005:422-428.
[14] Niemeijer M,van Ginneken B,Russell SR,et al.Automated detection and differentiation of drusen,exudates,and cotton-wool spots in digital color fundus photographs for diabetic retinopathy diagnosis[J].Invest Ophthalmol Vis Sci, 2007,48(5):2260-2267.
[15] Jaafar HF,Nandi AK,Al-Nuaimy W.Automated detection of exudates in retinal images using a split-and-merge algorithm[A].2010 18th European Signal Processing Conference[C].Aalborg:IEEE,2010:1622-1626.
[16] Soares I,Castelo-Branco M,Pinheiro AMG.Scale-space curvature detection of retinal exudates with a dynamic threshold[A].2011 7th International Symposium on Image and Signal Processing and Analysis[C].Dubrovnik:IEEE,2011:523-528.
[17] Esmaeili M,Rabbani H,Dehnavi A M,et al.Automatic detection of exudates and optic disk in retinal images using curvelet transform[A].IET Image Processing[C].Stevenage:IET,2012:1005-1013.
[18] 林蔚.基于K近邻图区域合并的视网膜硬性渗出自动检测研究[D].上海:上海交通大学生物医学工程系,2008.
[19] 高玮玮,沈建新,王玉亮.基于数学形态学的快速糖尿病视网膜病变自动检测算法[J].光谱学与光谱分析,2012,32(4):760-764.
[20] 周云燕,杨坤涛,黄鹰.基于最小类内离散度的改进Otsu分割方法的研究[J].华中科技大学学报(自然科学版),2007,35(2):101-103.
[21] Javitt JC,Canner JK,Frank RG,et al.Detecting and treating retinopathy in patients with typeⅠdiabetes mellitus. a healthy policy model[J].Ophthalmology,1990,97(4):483-494.
[22] 高玮玮,沈建新,王玉亮.RBF神经网络和阈值分割实现视网膜硬性渗出自动检测[J].中国图像图形学报,2013,18(7):859-865.
[23] 马林茂,富振英,王克安,等.2型糖尿病危险因素的Logistic回归分析[J].中华糖尿病杂志,1999,7(5):262-264.
[24] British Diabetic Association.Retinal photography screening for diabetic eye disease[R].London:British Diabetic Association,1997.
A Comparative Study on Automatic Detection Methods for Hard Exudates Based on Threshold Segmentation and Pattern Classifier