基于人工神经网络模型的肺癌CT图像分割算法
引言
肺癌是对人类生命健康威胁最大的肿瘤之一,近年来中国肺癌的发病率居全球首位且逐年递增[1-2],如何做到肺癌早期诊断是一个挑战。随着人工智能的兴起,基于计算机技术的医疗辅助诊断工具开始应用于肺癌鉴别,主要借助图像分割算法提取肺癌病变区域。图像分割是指把图像分成各具特性的区域并提取出感兴趣目标的技术和过程[3]。几乎所有的分割算法均是针对图像灰度的连续性或不连续性进行操作,比如传统的阈值法、区域分割法、边缘分割法,还有基于特定理论的聚类分析算法、模糊集理论、人工神经网络模型、遗传算法等。实验表明融合特定理论的分割算法优于传统算法的分割效果,其中聚类分析简单易行,但易受噪声与灰度不均影响较大,且串行处理能力有限;基于模糊集理论的分割精度较低;遗传算法稳定性强,时间复杂度较低,但容易过早收敛,陷入局部最优解;人工神经网络(Artificial Neural Network,ANN)是一种应用类似于大脑神经突触联结的结构进行信息处理的数学模型,提取图像的纹理具有较好的并行处理和数值逼近能力,非常适用于区分目标与背景。
人工神经网络模型已显示出对规则病灶较高鉴别率,其中Irianto等[4]采用基于纹理特征的ANN模型,得到肺癌鉴别准确率为80%;Kohad等[5]采用蚁群优化算法从250幅CT图像中选取显著纹理特征输入ANN模型,获得98.4%的准确度和96%的敏感度。当病灶区域不规则时,纹理分析不足以表征肺癌CT图像的特性。本研究采用基于分形特征的ANN模型提取肺癌病灶区域,并与纹理特征的分割效果比较。
1 方法
本研究提出的肺癌CT图像分割算法流程,见图1,其中图像预处理采用维纳滤波抑制图像噪声,模糊增强提高图像对比度,然后从预处理图像中提取纹理和分形特征,最后选取显著性的特征输入人工神经网络模型完成图像分割。
图1 肺癌CT图像分割流程
1.1 图像预处理
CT图像质量往往受噪声污染而下降,维纳滤波器是经典的线性去噪滤波器,常被用于从加性噪声中恢复有用信号,是一种综合退化函数和噪声统计特征进行复原处理的滤波方法。在滤波器输出与期望输出之间达到最小均方误差,维纳滤波可称作是一个最优滤波系统[6]。此外,肺部CT图像特征由灰度、尺寸、形状等差异构成,容易造成图像边界与区域模糊,传统的图像增强方法难以区分模糊边界区域。本研究采用模糊增强算法处理CT图像不精确和模糊信息,增强图像对比度。对于尺寸N×N的图像I,首先计算图像各像素模糊隶属度,将图像从空间域变换到模糊域,然后运用模糊增强算子回归调用修正隶属度,最后通过模糊域反变换将模糊隶属度转换成新的灰度级,映射到图像的空间域,分别由公式(1)~(3)给出,其中Fe、Fd为变换系数,pmax(i,j)图像像素最大的灰度值,p(i,j)为图像像素灰度值。u(i,j)表示p(i,j)的隶属度,取值0~1。
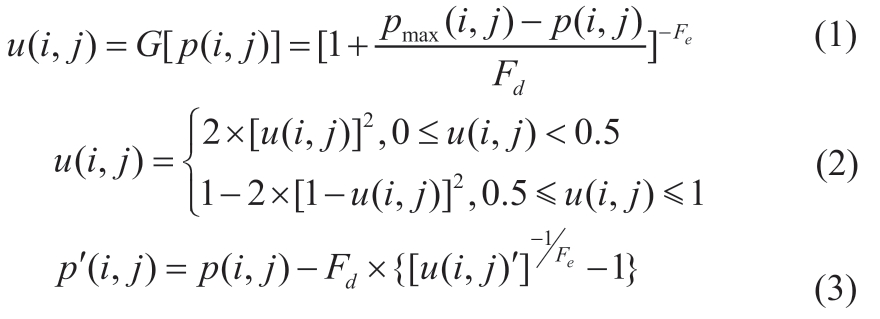
1.2 图像纹理特征提取
纹理是一种反映图像中同质现象的视觉特征,体现物体表面具有缓慢变化或者周期性变化的表面结构组织排列属性[7]。常用统计方法灰度共生矩阵描述图像像素灰度关于方向、相邻间隔、变化幅度的综合信息。由于纹理特征能提供独特的区域像素空间多样性信息,容易做到区分目标与背景,适用于肺癌病灶提取。本研究共提取14个纹理特征,但显著性特征仅有3个,分别为图像惯性、均值和熵特征,由公式(4)~(6)求得[8]。
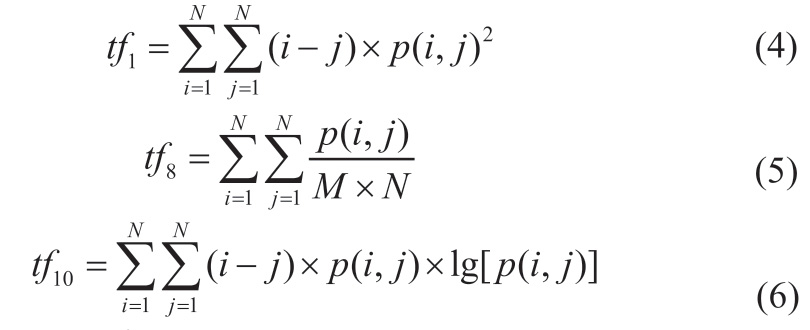
1.3 分形特征提取
分形特征常被用来描述复杂非规则的医学图像特征[9-10],其中分形维度是刻画非线性图像复杂程度、不规则程度和空间分布变化趋势的一个重要参数,由差分盒维数法计算所得。主要思想为:对于一个尺寸为N×N的灰度图像,把二维图像视作三维空间的一个表面(i,j,p(i,j)),其中(i,j)代表像素空间位置,p(i,j)代表对应位置灰度值,则图像灰度的变化情况将以空间立体表面的粗糙程度反映,使用不同尺度度量该立体表面,得到的维数即为图像分形维度。
具体步骤如下:将N×N图像分割成s×s块,2<s<N/2,令r=N/s,每个分块包含一列s×s×h的盒子,h为单个盒子高度。采用一个5×5窗口在图像上滑动,移动幅度为r,假设第(i,j)个分块中最大灰度值和最小灰度值分别落在第k和l个盒子中,则覆盖第(i,j)个分块所需盒子数由公式(7)计算,覆盖整幅图像所需盒子数由公式(8)给出,此时对应的分形维度FD由公式(9)给出。选取一组s,通过线性拟合即可求得分形维度FD。
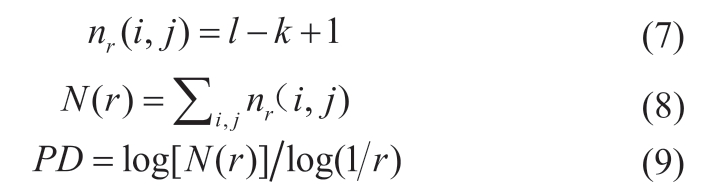
采用公式(7)~(9)可从模糊增强图像获得12个肺癌病灶CT图像分形特征ff1~ff12,其中10个分形特征具有显著性。
1.4 人工神经网络
被提取的纹理特征与分形特征存在冗余,需要从中选取显著性特征作为人工神经网络模型的输入。人工神经网络是由神经元相互连接组成的网络,是一种模拟动物神经网络行为特征,进行分布式并行数据处理的数学模型[11-12]。ANN具有自学习和自适应的能力,可以通过预先训练样本和预测样本来确定两者之间潜在的规律,利用训练阶段形成的规则对新输入样本数据进行推算。最常用的是后向传播神经网络模型,能运用输出结果产生的误差进行反向推敲,从而逐步优化网络结构和网络参数。结构如图2所示,最左边是输入层,中间是隐藏层,右侧是输出层,每个节点代表一种特定的输出函数,称为激励函数,每两个节点间的连接都代表一个对于通过该连接信号的加权值。
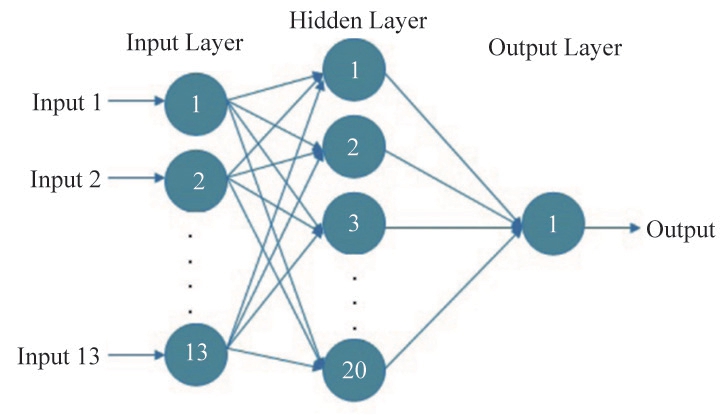
图2 向后传播神经网络模型结构
利用ANN对图像进行分割时,将待分割图像中的所有点聚类为目标和非目标的像素点,准确聚类后去除非目标像素点,从而得到目标图像。具体步骤如下。
(1)设有c层神经网络,如在输入层上加上输入模式P,并设第z层y单位输入的总和为![]() 输出为
输出为![]() 由z-1层的第j个神经元到z层的第x个神经元的结合权值为Wxy。各个神经元的输入与输出关系函数是f,则各变量间的关系见公式(10)~(12)。
由z-1层的第j个神经元到z层的第x个神经元的结合权值为Wxy。各个神经元的输入与输出关系函数是f,则各变量间的关系见公式(10)~(12)。
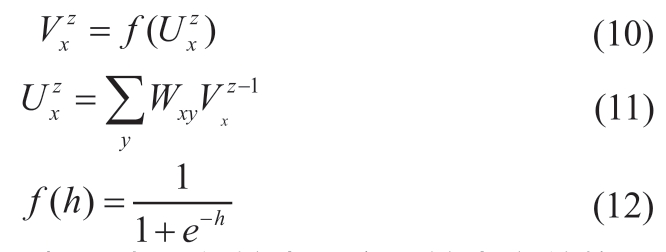
(2)定义误差函数E为期望输出与实际输出之差的平方和,见公式(13)。ANN学习过程即为求误差函数极小值,采用非线形规划的梯度下降法求得权值![]() 的更新量
的更新量![]() ,见公式(14),ε为学习率,取值0~1。
,见公式(14),ε为学习率,取值0~1。
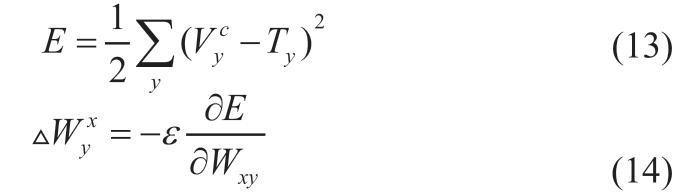
(3)经过较为复杂的求导运算,求得修正权值,见公式(15)和(16),完成算法收敛。
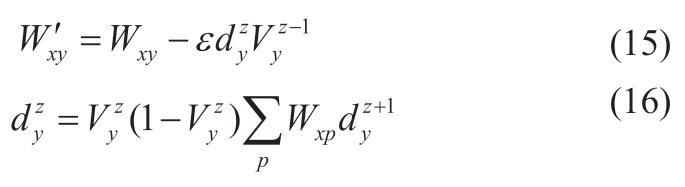
ANN性能主要取决于网络参数,包括输入层、隐藏层、输出层、学习速率和动量[13-14],其中低学习速率和高动量导致学习进展缓慢,相反高学习速率和地动量导致学习停止。隐藏层数量较低时,导致隐藏层不稳定,数量较高时,导致输出不稳定。为了避免过度拟合,采用公式(17)获取隐藏层数量上限Nh,其中Ni表示输入层神经元数量,No输出层神经元数量,Ns代表训练样本数量,α取值范围为2~10,输入和输出的平均值作为隐藏层下限值。
1.5 评价指标
采用平方根误差(Mean Square Error,MSE)、敏感度(Sensitivity)、特异度(Specificity)、准确度(Accuracy)评估本研究人工神经网络性能[15-17],见公式(18)~(21)。其中,target代表目标区域,actual代表实测区域,TN、TP、FN和FP分别代表组织真阳性、真阴性、假阳性和假阴性数量。

2 结果与分析
本研究CT图像源自46位男性与36位女性,其中包含48例肺癌患者和34例正常患者,提取出的背景、肺癌区域和边界数量总计1150个,图像尺寸大小为256×256×63个体素,所有的仿真实验均在MATLAB R2013a平台上实现。
2.1 预处理结果
图像预处理结果如图3所示,其中维纳滤波消除图像噪声,模糊增强后图像对比度显著提升。
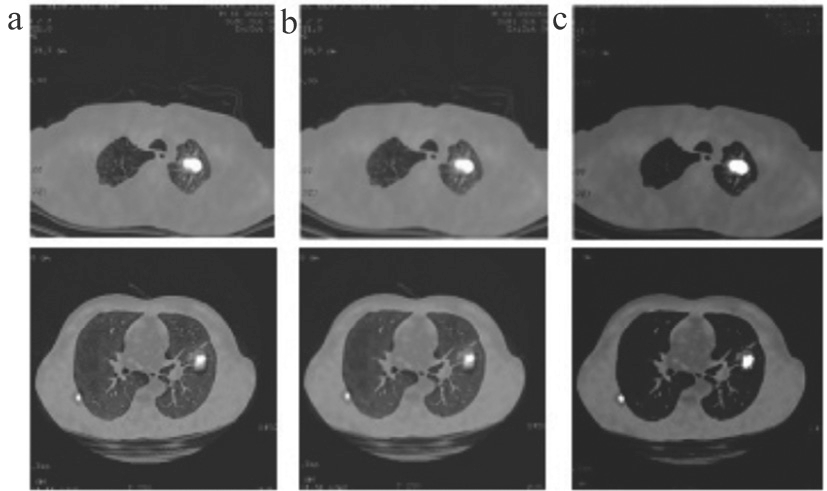
图3 图像预处理结果
注:a.灰度图像;b.维纳滤波结果;c.模糊增强结果。
2.2 图像特征提取
图4代表CT肺部图像纹理和分形特征的特征值,可以看出14个纹理特征中仅3个(tf1,tf2,tf3)正常肺部与肺癌特征值无重叠,12个分形特中有10个(ff11,ff12,ff21,ff22,ff41,ff42,ff51,ff52,ff61,ff62)无重叠特征值,可作为显著性特征。图5和图6分别为纹理特征与分形特征肺癌分类图像,可以看出病灶被完整地提取。
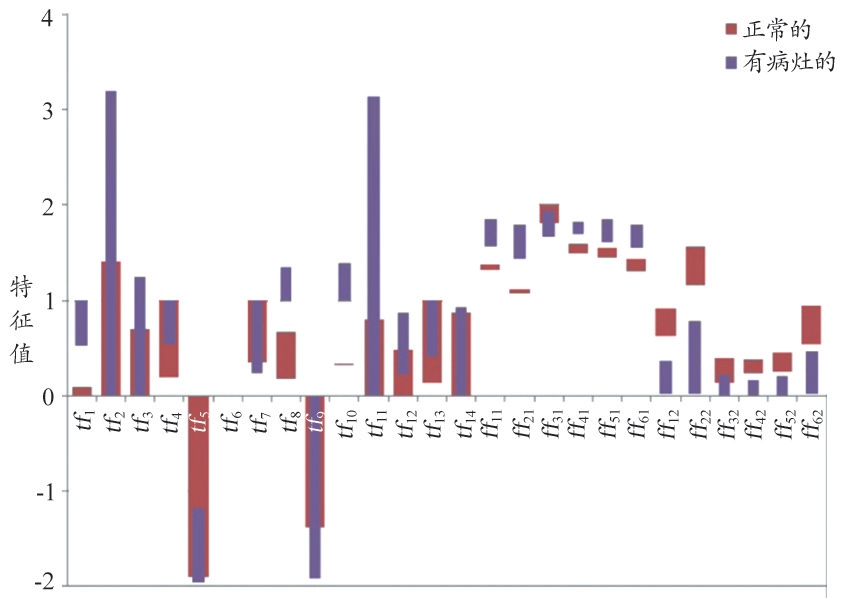
图4 正常肺部图像与肺癌患者的纹理和分形特征值

图5 显著纹理特征
注:a.惯性特征;b.均值特征;c.熵特征。
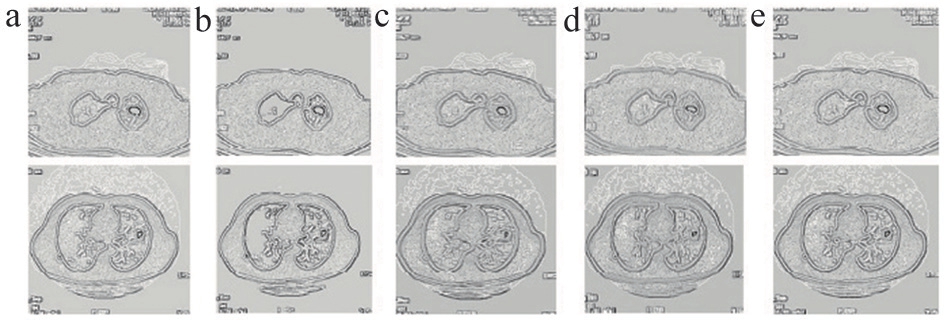
图6 分形显著特征
注:a~e表示不同分形特征图像。
2.3 神经网络参数确定
本研究获得的纹理特征与分形特征作为训练数据,选用多种训练函数,学习速率和动量范围0.3~0.9,带入公式(15),输入神经元数目13,包括3个纹理特征,10个分形特征,隐藏层数1,输出神经元1个,α=2,隐藏神经元数量范围7~38,采用平方根误差MSE评估各参数对ANN性能影响,结果显示训练函数为列文伯格-马夸尔特反向传播函数,隐藏神经元数量为20,学习速率为0.3,动量为0.9,最大数目为1000时,ANN性能最佳,供测试阶段使用。
2.4 算法性能结果
图7表示基于ANN的肺部病灶图像分割,表1表示基于不同特征定量分析。可以看出本研究提出的ANN算法能准确快速的提取出肺癌病灶区域。训练阶段灵敏度、特异度和准确度可达98.4%(联合特征)、100%(分形特征)和98.6%(联合特征),同时测试阶段对应指标分别可达90.9%(联合特征)、100%(分形特征)和95.1%(分形特征),可以看出基于分形特征和联合特征的定量指标优于纹理特征。
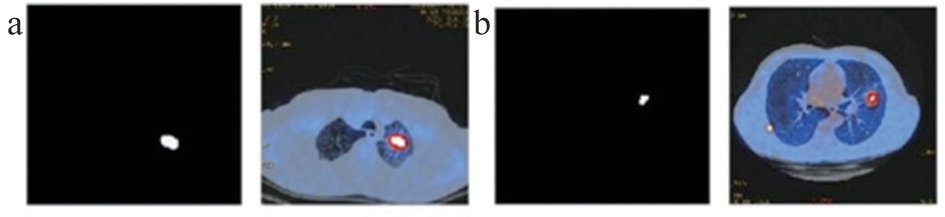
图7 CT肺部病灶提取结果
注:a.上肺病灶;b.中肺病灶。
表1 纹理特征、分形特征和联合特征分类的结果比较(%)

3 结论
本研究提出一种基于人工神经网络模型的肺癌CT图像分割算法,其中维纳滤波与模糊增强等预处理能有效地抑制图像噪声,提高图像对比度;特征值不重叠法能准确选取显著的纹理特征和分形特征,平方根误差能预测人工神经网络模型最佳参数,快速准确提取肺癌病灶区域,表明本研究提出的肺癌CT图像分割算法具有可行性和实用性,可作为肺癌辅助诊断。
[1]Bertolaccini L,Solli P,Pardolesi A,et al.An overview of the use of artificial neural networks in lung cancer research[J].J Thorac Dis,2017,9(4):924-931.
[2]Kannuswami P,Poobal S,Ramya MM.Artificial neural network based lung cancer detection for PET/CT images[J].Indian J Sci Technol,2017,10(42):1-13.
[3]Rodrigo H,Tsokos CP.Artificial neural network model for predicting lung cancer survival[J].JDAIP,2017,5(1):33-47.
[4]Irianto BG,Mak'Ruf MR,Titisari D.Identification of lung cancer using a back propagation neural network[J].J Sol-Gel Sci Techn,2015,74(3):734-739.
[5]Kohad R,Ahire V.Application of machine learning techniques for the diagnosis of lung cancer with ANT colony optimization[J].Int J Comput Appl,2015,113(18):34-41.
[6]Fan D,Wei L,Cao M.Extraction of target region in lung immunohistochemical image based on artificial neural network[J].Multimed Tools Appl,2016,75(19):1-18.
[7]Kannuswami P,Poobal S,Ramya MM.Artificial neural network based lung cancer detection for PET/CT images[J].Indian J Sci Technol,2017,10(42):1-13.
[8]Murali M,Singh KMV,Rajasekar B.Based on artificial neural network reconstructing fast X-ray and CT images[J].Res J Pharm Biol Chem Sci,2016,7(4):623-632.
[9]巩萍,王阿明.基于灰度共生矩阵和人工神经网络的肺癌CT图像的分类研究[J].生物医学工程与临床,2013,(6):552-556.
[10]王锦程,郁芸,杨坤,等.基于BP神经网络的脑肿瘤MRI图像分割[J].生物医学工程研究,2016,35(4):290-293.
[11]Taghadomisaberi S,Omid M,Emamdjomeh Z,et al.Determination of cherry color parameters during ripening by artificial neural network assisted image processing technique[J].J Agr Sci Technol,2015,17(3):589-600.
[12]Türky?lmaz ì,Kaçan K.License plate recognition system using artificial neural networks[J].ETRI J,2017,39(2):163-172.
[13]Wu S,Chen H,Bai Y,et al.The optimal band combination joint WCOMP+BPNN classification method for remote sensing image[J].J Comput Inform Syst,2015,11(8):2873-2884.
[14]Li D,Yang F,Wang X.Study on ensemble crop information extraction of remote sensing images based on SVM and BPNN[J].J Indian Soc Remote Sens,2017,45(2):229-237.
[15]曹俊贤,宋春林.分形维数的计算及改进[J].信息技术与信息化,2017,(10):19-23.
[16]唐思源,邢俊凤,杨敏.基于BP神经网络的医学图像分割新方法[J].计算机科学,2017,44(S1):240-243.
[17]王锦程,郁芸,杨坤,等.基于BP神经网络的脑肿瘤MRI图像分割[J].生物医学工程研究,2016,35(4):290-293.
An Algorithm of Lung Cancer CT Image Segmentation Based on Artificial Neural Network Model