一种间接免疫荧光实验封片印章的研制
许兴路1, 谭太昌2
1.黑龙江省医院 放射免疫特检科,黑龙江 哈尔滨 150036;2. 四川省医学科学院 四川省人民医院 检验科,四川 成都 610072
[摘 要]目的设计一种用于解决间接免疫荧光实验过程中快速准确滴定封片液的工具(简称封片印章)。方法根据普通印章的原理,采用聚甲基丙烯酸甲酯材料制成封片印章。结果该设计解决了封片液快速均匀滴定的问题,目前已试用于全国20家医院的间接免疫荧光实验中,并得到一致认可。该封片印章滴定封片液速度快,封片液滴大小一致,液滴距离均匀,与荧光片对应整齐,显著提高了封片效率和封片质量。结论该产品可以广泛应用于间接免疫荧光实验封片过程及具有同类封片需求的实验中,将来还可以应用在有封片需求的自动化仪器上。
[关键词]封片印章;间接免疫荧光实验;封片;封片介质
引言
间接免疫荧光实验(Indirect Immuno fluorescence Assays, IFA)[2]是自身抗体临床检测经典的不可或缺的实验方法,广泛应用于自身抗体的快速筛查、确立临床诊断方向及发现新抗体[3-6]。目前IFA通常采用手工操作,部分实验室已经采用了自动化仪器完成操作[6-8]。然而,无论是手工操作,还是自动化仪器操作,都无法回避滴定封片液进行封片的步骤。即使是自动化仪器,也没有给出完善的自动封片解决方案。两种方法都需要实验人员手持封片液滴定塑料瓶,一滴一滴地滴在盖玻片或基质片的特定位置,滴定若干封片液滴。并且,要求封片液滴大小均一,位置准确。然后盖上基质片(倒扣反应实验)或盖玻片[5,10-11]。所有这些操作,需要实验人员技术娴熟,耐心仔细。面对数以百计的实验量,对实验人员的耐性和耐力都是很大的挑战。封片印章的设计就是为了解决封片液滴定难题,简化滴定操作,提高封片质量和效率,减轻实验人员工作量,是实现封片自动化及标准化的最佳解决方案。
1 材料与方法
1.1 原理
采用印章的工作方式,制作有若干引脚的印章样工具即封片印章。用封片印章的引脚蘸取封片液,利用封片液粘稠的物理特性,引脚可以黏附一定量的封片液。当封片印章的引脚在盖玻片上按下并抬起后,会有部分封片液黏附在盖玻片上,从而实现封片液的滴定。
1.2 封片印章引脚携带封片液试验
1.2.1 实验目的
选出满足滴定量的滴定引脚规格及合适的封片液深度。间接免疫荧光实验封片过程中,封片液滴定量有严格的规定(10 μL)[11]。滴定量少则无法很好吸附盖玻片;滴定量过多,会使封片液溢出。封片液滴定量与引脚的直径及引脚在封片液中的浸入深度正相关。基于这两个因素,设计实验选出最理想的引脚直径和封片液深度范围。
1.2.2 实验设计
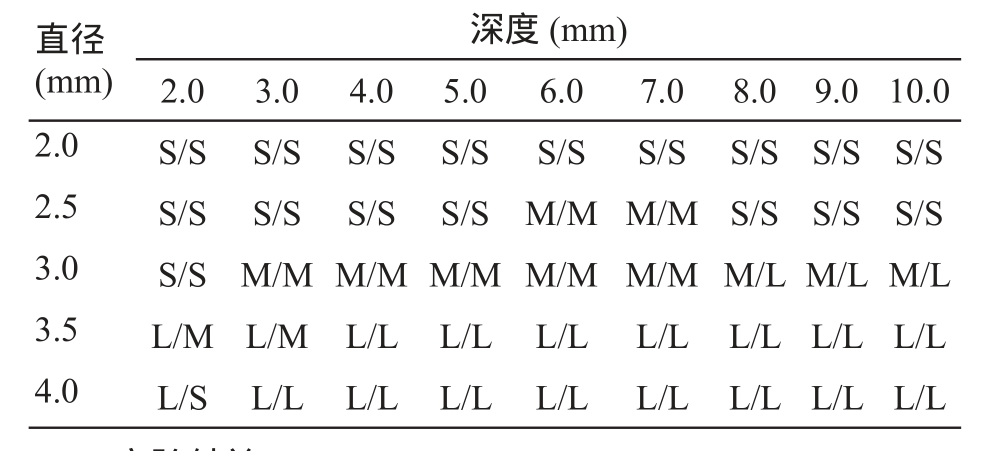
制作直径分别为2、2.5、3、3.5、4 mm的印章引脚,封片液深度分别准备2、3、4、5、6、7、8、9、10 mm;用不同直径的引脚分别蘸取不同深度的封片液,点在盖玻片上,要求每个规格的引脚要蘸取相同深度的封片液5次,用游标卡尺测量液滴的直径,取其均值;结果统计S表示液滴直径小或液滴量少;M表示液滴直径适中或液滴量适中;L表示液滴直径大或液滴量大。
1.2.3 实验结果
封片印章引脚直径及封片液深度遴选结果,见表1。
表1 封片印章引脚选择方案及结果
1.2.4 实验结论
直径2.5 mm和3.0 mm的引脚可以滴定出直径适中的液滴,封片液深度在3.0~7.0 mm的引脚可以滴定出封片液量适中的液滴。其中直径2.5 mm的引脚适合的封片液深度范围狭窄,只有封片液深度在6~7 mm时才可滴定出适中的液滴;而直径为3.0 mm的引脚是印章引脚最佳直径,封片液的深度控制在3.0~7.0 mm间均能得到适中的液滴,一次灌注封片液可滴定更多液滴。
1.3 封片印章的设计
(1)材质。为方便封片印章制造及滴定操作时定位,特采用 聚甲基丙烯酸甲酯(Polymethyl Methacrylate,PMMA)材质,PMMA俗称有机玻璃,材质透明,便于加工[12]。
(2)结构。封片印章由印章体和印章引脚组成,印章主体采用厚7.0 mm长宽50 mm×20 mm的PMMA块。根据以上试验结果,印章引脚是10个直径3.0 mm长度10.0 mm的PMMA圆柱体,圆柱体分两排,分布印章体纵轴两侧,根据实验基质片间距,每个引脚的中心点间距是9.0 mm,圆柱体距离宽边距离5.5 mm,距离窄边距离7.0 mm。引脚分布与基质片上基质分布相同,形成一一对应的关系。配合封片印章,还有一个印章盒,用于存放封片印章和蘸取封片液。封片印章设计结构图,见图1。
1.4 封片印章的使用
封片印章的使用,具体参照如下的步骤:
(1) 灌注封片液。向封片印章盒的封片液槽加注封片液,液面深度控制在3.0~7.0 mm为宜。
(2)蘸取封片液。右手拇指和食指从右侧捏住印章体窄边,保持印章引脚朝下,露出印章背面,便于观察印章引脚滴定位置。手持印章移动至封片印章盒的封片液槽处蘸取封片液,使印章引脚黏附足量封片液。
(3)滴定封片液。移动印章到达盖玻片上方,对齐位置按下印章后稍微停顿后抬起。抬起印章时注意,印章拇指或食指端先抬起少许,再垂直抬起,防止印章引脚带起盖玻片。
(4)结束封片。进行下一个盖玻片封片液滴定。

图1 封片印章设计结构图
注:1.封片盒底座;2.连接转轴;3.封片盒盖;4.封片液槽;5.放置槽;6.滴定引脚;7.印章体。
2 结果
2.1 应用及普及情况
截止到投稿时,封片印章已在全国多达20家医院实验室使用,其中包括北京协和医院、北京大学人民医院等全国知名医院。另外,还包括国外一家医疗机构在使用。使用该产品时间最长的单位黑龙江省医院已长达5年,累计封片10000余张。封片印章得到使用单位的一致好评。
2.2 产品优缺点
通过各家医院实际使用情况和反馈信息,可以得出如下结论。
2.2.1 封片印章优点
(1)创新性发明。封片印章的研制及在间接免疫荧光实验中使用,据调查属于全世界首例,是填补该行业空白的工具。
(2)效率高。封片印章滴定速度显著提高。封片印章具有10个滴定圆柱,一次可以滴定10个封片液滴,滴定速度比手持封片液滴定瓶一点一点滴定大大提升,减少实验人员的工作量,简化实验操作流程。
(3)质量保证。封片印章滴定质量显著改善。封片印章每个滴定引脚大小一致,位置固定,且与基质片位置一一对应。封片印章这些特点确保其滴定的封片液滴大小均一,间距相等。
(4)位置准确。封片印章滴定操作方便定位。封片印章采用透明PMMA材质,方便实验人员确定滴定位置,确保滴定液滴与基质片一一对应。
(5)方便自动化。封片印章已初步应用到自动化间接免疫荧光实验仪器上,解决了自动化仪器滴定封片液的难题,推动了间接免疫荧光实验的自动化进程。
2.2.2 封片印章缺点及改进意见
(1)操作不够方便。封片操作时需要拇指和食指捏住封片印章体窄边的两端,该手持方法不够方便。解决办法:给封片印章体顶部(见图1 注7)设计一个把手,操作时捏住封片印章的把手,提高操作的舒适度。
(2)封片印章盒过小。封片印章盒过小,使用过程中蘸取封片液不方便且容易侧翻,导致封片液外漏。解决办法:设计更大的封片印章盒,或为现有封片盒固定更大的底座。
(3)封片印章引脚数目固定。间接免疫荧光实验用到的基质片有3、5、10个基质3种规格,该封片印章只有10个引脚规格,不能满足其他规格的要求。解决办法:采用10引脚兼容其他两个规格,由于实验试剂盒配给的封片液足够多,使用10个引脚规格兼容3、5个基质的荧光片,封片液仍有剩余。而且如果3、5、10个引脚3种规格的封片印章同时使用,会给操作带来不便。
(4)盖玻片容易被黏附带走。封片印章按下抬起时容易将盖玻片黏附在封片印章引脚上,跟封片印章一起被带走。该问题是操作熟练程度不够导致,需要操作者遵守操作说明,经过简单的练习可避免。
3 讨论
间接免疫荧光实验是自身抗体检测的重要方法,被美国风湿病学会(ACR)、欧洲自身免疫标准化促进会(EASI)等专业学会推荐为参考方法[13]。国内的现状是:绝大部分实验室通过手工操作实现,少部分实验室采用了自动化操作仪实现。国际上自动化操作解决方案有5个,分别是:AKENOMI,Medipan; Zenit lite,A. Menarini Diagnostics;Sprinter XL,Euroimmun;Helmed,Aesku. Diagnostics;AFT3000™,Immuno Concepts[14-16],其中在国内应用的有Aesku的Helmed和Euroimmun的Sprinter XL。
间接免疫荧光实验手工操作适合实验样本少,检测项目少的实验室[7-9]。如果实验室样本过多,就存在实验每个步骤操作时间过长,前后样本反应时间不一致的问题,影响批内实验质量[5]。另外,过多的实验样本,由人工操作出现差错的概率也会增多。自动化解决方案的出现,很好的解决了以上问题,并且实验的质量也很好,完全达到手工实验的效果。但是现有的自动化仪器都没有对封片问题给出完善的解决方案,有的需要借助手工封片,有的省去封片步骤,失去封片液保护的基质片,荧光非常容易被淬灭。
自动化解决方案对自动封片的缺失是受封片液的理化性质影响导致的。封片液的主要成分是甘油,甘油是一种粘稠液体,在20℃的粘 度大约1500 cP,是水粘度的1000多倍[17]。使用常规柱塞泵或蠕动泵无法实现自动化滴定[5]。所以无论是手工操作的实验室,还是自动化操作的实验室,在封片问题上,都要靠实验人员手动滴定封片液完成封片操作。
封片印章弃常规移液方式,恰恰利用封片液粘稠的特性,采用粘液吸附的原理[18],实现封片液的滴定。并排的印章引脚阵列,一次可以滴定多个封片液滴,大大提高了操作效率,确保滴定质量。该封片印章可以应用在手工操作的间接免疫荧光实验及有同类需求的实验操作中,也可应用在自动化的仪器上,促进间接免疫荧光操作全面的自动化。
4 结论
总之,封片印章的设计,具有实际应用价值,有效解决了间接免疫荧光实验中封片液滴定问题。提高了滴定效率和质量,减少工作量,减化了实验步骤,为自动化封片提供完善的解决方案。全国范围的试用结果理想,可以进行全面的推广应用。
[参考文献]
[1] 许兴路.一 种新型荧光膜片的封片印章:中国,ZL20162008417 6.4[P].2016-06-15.
[2 李永哲.自 身抗体免疫荧光图谱[M].北京:人民卫生出版社,2014.
[3] 马东来,张少静,文夫瑞德 斯特克.自 身抗体及其免疫荧光模式[M].北京:北京科学技术出版社,2000.
[4] Tozzoli R,Bonaguri C,Melegari A,et al.Current state of diagnostic technologies in the autoimmunology laboratory[J]. Clin Chem Lab Med,2013,51(1):129-138.
[5] 王玮,罗静,崔丽艳.两种间接免疫荧光实验自动化操作平台的实测比对与分析[J].山西医药杂志,2015,44(21):2553-2558.
[6] Tozzoli R, Antico A, Porcelli B,et al.Automation in indirect immuno fluorescence testing: a new step in the evolution of the autoimmunology laboratory[J].Autoimmun Highl,2012,3(2): 59-65.
[7] 胡朝军,李永哲.重 视自身免疫性肝病相关自身抗体的规范检测与合理应用[J].中华检验医学杂志,2014,37(2):81-83.
[8] 谭太昌,王婷,张航烽,等.抗 双链DNA抗体检测策略研究[J].成都医学院学报,2014,9(2):128-133.
[9] 谭太昌,吴雅娟,腾飞鹏.抗核抗体检测策略研究[J].成都医学院学报,2013,8(5):517-520.
[10] Haack L,Selvaggi S.Back to basics: Validation of automatedas compared to manual slide staining in the cytopathology laboratory[J].Diagn Cytopathol,2008,36(4):199-201.
[11] 欧蒙医学诊断(中国)有限公司.抗核抗体IgG检测试剂盒(间接免疫荧光法)产品说明书[Z].2016-07-15.
[12] 黎永生.高透明韧性有机玻璃的研究[D].南昌:南昌航空大学,2011.
[13] 胡朝军,周仁芳,张蜀澜,等.抗核抗体HEp-2细胞间接免疫荧光模型及其结果报告方式国际共识解读[J].中华检验医学杂志,2016,39(11):804-810.
[14] Shovman O,Agmon-Levin N,Gilburd B,et al.A fully automated IIF system for the detection of antinuclear antibodies and antineutrophil cytoplasmic antibodies[J].Immunol Res,2015,61(1): 135-140.
[15] Bizzaro N,Antico A,Platzgummer S,et al.A utomated antinuclear immuno fluorescence antibody screening: a comparative study of six computer-aided diagnostic systems[J].Autoimmun Rev, 2014,13(3):292-298.
[16] Meroni PL,Bizzaro N,Cavazzana I,et al.Automated tests of ANA immunofluorescence as throughput autoantibody detection technology: strengths and limitations[J].BMC Med, 2014,12(1):1-5.
[17] 刘竹琴,刘艳峰,田蕾.甘油的粘度与浓度关系的实验研究[J].延安大学学报:自然科学版,2005,24(4):58-59.
[18] 刘丹丹,徐志成,等.阳离子和两性表面活性剂在聚甲基丙烯酸甲酯表面的吸附行为[J].物理化学学报,2013,29(3):569-575.
本文编辑 袁隽玲
Preparation of a Mounting Stamper in Indirect Immunoin fluorescence Assays
XU Xinglu1, TAN Taichang2
1.Department of Radioimmunoassay, Heilongjiang Provincial Hospital, Haerbin Heilongjiang 160036, China; 2.Department of Medical Laboratory, Sichuan Academy of Medical Sciences & Sichuan Provincial people’s Hospital, Chengdu Sichuan 610072, China
Abstract:ObjectiveTo design a tool for titrating sealing liquid (stamper for short) rapidly and accurately in indirect immunoinfluorescence assays (IFA for short).MethodsAccording to the principle of the common seal, the stamper was made by using polymethymethacrylate (PMMA).ResultsThis device had met the demand of titrating sealing liquid rapidly and equably. To date, the stamper had been used in IFA of 20 domestic hospitals, which had gained unanimous recognition. The stamper could improve the sealing ef ficiency and quality signi ficantly by its rapid titrating speed, equal droplet size, and uniform droplet distance.ConclusionThis device can be widely used in indirect IFA or other assays with similar demands of sealing and further applied to the automatic instruments with the need of sealing in the future.
Key words:stamper; indirect immuno fluorescence assays; sealing; mounting medium
[中图分类号]446.6
[文献标识码]A
doi:10.3969/j.issn.1674-1633.2017.09.013
[文章编号]1674-1633(2017)09-0056-03
收稿日期:2016-10-24
修回日期:2017-01-04专利名称:实用新型专利(ZL2016 2 0084176.4)。
通讯作者:谭太昌,副主任技师,主要研究方向为自身抗体检测的智能化及自动化。
通讯作者邮箱:hljria@126.com