基于医疗器械不良事件探讨我院的医疗器械使用质量控制
马娟
南通市第三人民医院 设备科,江苏 南通 226001
[摘 要]医疗器械广泛应用于疾病的预防、诊断、治疗和康复的过程中,医疗器械使用质量越来越受到重视。本文汇总了我院医疗器械不良事件(Medical Device Adverse Events,MDAE)监测工作,分别从医用耗材和医疗设备两个方面介绍了医疗器械使用质量控制方法和管理方式,同时由MDAE监测工作这一个点推及到我院医疗器械使用质量控制这一条线,建立完整的医疗器械使用质量控制体系。
[关键词]医疗器械;不良事件监测;质量控制;输液器
引言
医疗器械是医院诊疗活动的重要保障,医疗器械风险管理是现代化医院管理的重点内容之一[1]。在生产和流通环节,政府通过《医疗器械生产质量管理规范》、《医疗器械注册管理办法》等一系列措施保证了医疗器械的“先天有效性”,但是作为决定器械最终发挥其应有效能的质控管理主体的医院,却因缺乏明确的监督主体和具体实施细则,使在用医疗器械的质量监管成为整个医疗器械生命周期中薄弱的一环[2-3]。近年医疗器械不良事件监测工作稳步推进,逐步发挥其功效,为医疗器械使用质量控制打下基础。医院作为医疗器械的主要使用机构,在可疑医疗器械不良事件报告工作中的责任更显得突出,且具有不可替代的作用[4]。
我院在2012年全面展开MDAE监测工作,建立专门领导小组,铺设监测网络,并且以MDAE监测为切入点在院内逐步进行医疗器械使用质量控制,减少并尽可能避免医疗器械不良事件重复发生以及医疗器械故障的发生,提高医疗器械使用的安全性和有效性。
1 本院医疗器械不良事件监测状况
MDAE监测越来越受到社会各层的关注,我院也将其作为医疗器械使用质量控制的重要组成部分。我院自2012年开始开展MDAE监测工作以来从设备科拓展到临床的各个科室共分成38个小组,以小组为单位细化分工,明确职责。在2015年我院制定监测网络,采取宣传、讲座等措施,使MDAE监测工作重视程度加深,上报数量和质量得到显著提升。
将发生MDAE的医疗器械进行分类汇总,结果见表1。上报的不良事件涉及到的医疗器械总共为13个类别,院内监测的医疗器械较全面。表1中占比较大的为医用高分子材料及制品,手术室、急救室、诊疗室设备及器具,注射穿刺器械,其中高分子材料及制品和注射穿刺器械主要为Ⅲ类医疗器械,对其安全性、有效性必须严格控制的医疗器械,手术室、急救室、诊疗室设备在手术在急救的时候必须拿得出,打得响,不能影响急救和手术,此类设备必须保证可靠地运行。这三大类的医疗器械必须严格监测发生的不良事件,及时发现及时上报,并做好评价和控制工作。
Ⅲ类医疗器械发生不良事件的占比相当大,医院内对Ⅲ类医疗器械的管理和控制需要更加严格,以保证使用的安全性。Ⅰ类的医疗器械占比低,可能存在漏报或不报的情况,对Ⅰ类医疗器械的监测力度不够,往往会忽视其存在的风险,见表2。行政管理力度薄弱和医务人员对监测工作认识不足,是导致医疗机构上报工作开展的主要障碍[5]。
表1 医疗器械不良事件报告汇总表
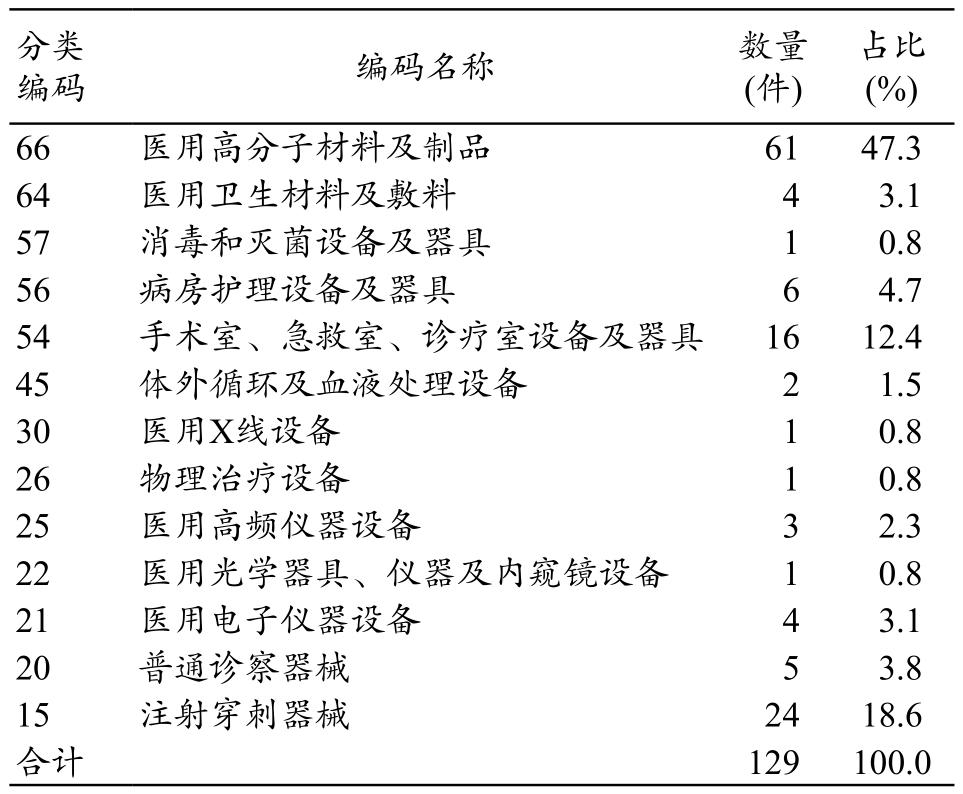
表2 发生不良事件的医疗器械管理类别

2 医疗器械使用质量控制
MDAE监测是我国对上市后医疗器械开展风险管理的重要手段[6],MDAE监测也是我院医疗器械使用质量控制的重要部分。通过对医疗器械不良事件的监测希望能够发现医疗器械的设计缺陷,生产材料缺陷,设备老化等固有风险。通过院内医疗设备的操作培训,设备维护保养等方式提高操作规范性和设备的可靠性。院内的医疗器械主要分为医用耗材和医疗设备,以下分别探讨其使用质量控制。
2.1 医用耗材使用质量控制
医用耗材入库时需经过核对验收,查看检测报告等基本流程,确保医用耗材“先天有效”就可进入临床使用。医疗器械不良事件监测是医疗器械置中和置后管理的重点[7]。
以输液器不良事件为例,医用耗材的MDAE控制流程。我院内一次性使用输液器(带针)共上报了47例漏水的不良事件,输液器在正常输液的情况下出现漏水现象,漏水的部位大多数在钢针与胶管的连接处。当临床科室向设备科反映此问题时,设备科材料采购员或者仓库管理员去现场查看具体情况,初步分析问题原因,采购员向供应商和产家反馈信息,经分析认定为热塑工艺问题在钢针与胶管的接口处没有固封紧密。最终该厂家的该种产品工艺改进无效,仍然出现漏液问题,采购员汇报领导更换了产品。
医用材料的不良事件监测能够起到一定的质量控制效果,在选择品质优良、信誉良好的生产厂家的同时应该注重医用材料的入库验收工作。仓库管理员必须核对材料的产地、规格、灭菌日期、有效期、以及检验报告等相关信息和资料。
从医用耗材的MDAE上报情况上也发现不足:重点监测的心血管支架、人工心脏瓣膜、心脏起搏器、骨科植入物等品种没有上报的案例。要提高医务人员的对MDAE监测的认识,加强重点品种的监测力度,做好这类医用材料的使用质量控制。
2.2 医疗设备使用质量控制
医疗设备在疾病诊断、治疗、康复等阶段都起到很大的作用,诊断器械发生系统故障会导致误诊和漏诊,治疗器械发生质量问题会导致治疗剂量无法按照设定值释放,严重时甚至会危及病人的生命。
以血液透析机为例。血液透析患者在透析过程中出现胸闷症状,并且静脉壶颜色发黑,机器却正常运行未报警,但是护士根据症状判断有可能是管路扭曲,立即重新安装管路。结束透析后送患者的血液标本化验,化验结果提示有溶血。血液净化中心立即通报设备科,设备科工程师对血透机进行检测,后又联系产家进行检测,并分批次对所有的血透机进行维护保养。血液灌流器、血液透析机等体外循环血液净化设备是MDAE的国家重点监测品种[8],一旦MDAE处理不好都会导致严重的后果。
输液泵、推注泵在正常使用的过程中出现滴速过快或过慢的问题,药物滴速过快过慢都有可能会对人体产生不可预计的影响和伤害。在滴速流量设定后怎么才能保证准确性,必须要借助相关的计量检测仪器。流量计量、血压计计量等相关的设备只依赖一年一次的计量局检测,但是在每次的维修之后是否能够符合计量要求不得而知,我院开始计划购买常用的计量检测仪器,确保维修的可靠性。
输液泵、推注泵、监护仪、呼吸机等很多相关的医疗设备需要预防性检查和维修,需要定时检测计量,不能仅仅停留在故障维修的阶段。平稳期的检查有助于更好地了解设备的状态,并指导我们针对随机性损害进行维修,寻找并确定设备劣化的源头,加以控制和消除[9-10]。医院管理层要加大对设备科的人员投入和资金投入,提高设备科的工作定位。
2.3 医疗器械使用质量控制管理
(1)对所用的医疗器械产品要实行追溯制度,重点提高可追溯性,使用的医疗器械产品要证照资料齐全。
(2)医疗器械材料入库要验收核对,包括品名、规格、型号、来源(生产厂商、供货单位)、批号、灭菌批号、有效期、批准文号、注册证号等。
(3)医疗设备以批量化、系列化采购为依托,建立麻醉机、呼吸机、手术室灭菌设备、急救设备等设备的标准化培训课程,实施全院医护人员的统一培训[11]。
(4) 医疗设备维修流程化责任制,工程师负责定期巡检,定期计量,保证正常运行状态。
(5)当发现、上报MDAE后,设备科及时分析事件发生的可能原因,详细记录有关监测情况,及时反馈信息至医疗器械生产和销售企业,对报告事件的临床科室进行调查[12]。
(6)关注医疗器械行业动态,及时通报医疗器械警示信息,及时发现医疗器械突发事件和召回事件。
3 讨论
就我院而言MDAE监测工作不断完善,MDAE上报的数量和质量都有很大提升,但是仍然存在一些问题。对植入性耗材应该加大监测力度,确保此类耗材的使用质量;在用医疗器械检测过程中,应该注重产品性能指标测量值变化规律的采集和把握,从而更好地了解设备的使用情况和工作状态[13]。建立一个科学合理的医疗器械使用质量控制体系至关重要,这也需要在工作中不断提高业务水平,不断积累经验。
虽然国际上的经验都已经证明,开展在用医疗器械检验和风险管理是必要的且有很大益处[14]。但是我国在用医疗器械的管理体系、制度的建立和完善[15],包括检验技术人员知识技能的培训以及在用医疗器械检验技术要求的完善,都还有待发展[16]。医疗器械使用质量控制工作任重道远。
[参考文献]
[1] 赵璨,刘静.浅谈医疗机构如何开展医疗器械不良事件监测工作[J].按摩与康复医学,2011,2(5):228-229.
[2] 赵明钢,柳琪林.加强我国医疗风险监管,确保病人医疗安全[J].中国医院,2005,9(5):24-26.
[3] 李晓.对医疗机构医疗器械监管的模式探讨[J].医学信息,2011,24(6):2520.
[4] 范雯怡,周利平,胥雪冬.某三甲医院可疑医疗器械不良事件上报情况分析[J].医院管理论坛,2014,31(1):14-15.
[5] 汤永刚,林国良.对医疗机构开展医疗器械不良事件监测工作的几点思考[J].中国药物警戒,2010,7(5):316-317.
[6] 王玲,周晶鑫,张学宁,等.医疗器械不良事件报告数据规整实践与提升报告质量的探索[J].中国医疗器械杂志,2014,38(5): 364-367.
[7] 邹萍,俞丽敏,于守丽.医疗器械不良事件监测管理探讨[J].中国医疗设备,2014,9(10):97-99.
[8] 国家食品药品监督管理局.国家重点监管医疗器械目录[EB/ OL].http://www.sfda.gov.cn/WS01/CL0845/40674.html.
[9] 李丹,何光彤,石磊,等.医疗设备的质量管理与控制[J].医疗装备,2013,26(7):44-45.
[10] 崔怡,崔骊,崔亮,等.医疗设备质量控制工作的问题及解决方案[J].中国医学装备,2013,(11):87-88.
[11] 程述森,石应康,金蓓,等.医疗器械的风险管理与质量控制[J].中国循证医学杂志,2010,10(6):754-755.
[12] 杜玮.我院医疗器械不良事件监测管理讨论[J].中国医疗设备,2013,28(11):101-103.
[13] 魏景锋,刘耀庭,崔泽实.医疗器械检测和校准实验室设备信息化管理的设计与开发[J].中国医学装备,2013,10(4):8-11.
[14] 邵建国,周子健,钱许峰.医疗设备风险管理的现状与对策[J].中国医疗设备,2012,27(6):107-108.
[15] 王良.在用医疗器械风险管理相关问题浅谈[J].科技与企业,2015,(16):5.
[16] 李澍,王权,张艳丽,等.在用医疗器械的检验技术要求[J].中国医疗设备,2014,29(10):58-61.
本文编辑 王博洁
Discussion on the Medical Device Quality Control in Use Based on Medical Device Adverse Events
MA Juan
Department of Equipment, Nantong Third People’s Hospital, Nantong Jiangsu 226001, China
Abstract:Medical devices are widely used in the prevention, diagnosis, treatment and rehabilitation of the disease, thus the monitoring of medical device adverse events has attracted much attention. The paper summarized the monitoring of medical device adverse events (MDAE) in our hospital, and introduced medical equipment quality control and management in aspects of medical supplies and medical equipment respectively. Meanwhile, the paper spread the line of medical device quality control from the point of MDAE monitoring, and established a complete quality control system for medical devices.
Key words:medical device; adverse event monitoring; quality control; transfusion
[中图分类号]R197.32
[文献标识码]C
doi:10.3969/j.issn.1674-1633.2017.08.043
[文章编号]1674-1633(2017)08-0163-03
收稿日期:2016-05-16
修回日期:2016-06-20
作者邮箱:997895141@qq.com